从初诊到康复...| 一文读懂乳腺癌
原文来源于知乎
关于彩超:
彩超评级3级需定期复查,4a及以上需穿刺活检,尤其是年龄40岁以上。恶性肿瘤有形态不规则、边缘不清晰、纵横比>0.7,后方回声衰减,弹性系数较硬、丰富血流信号、砂砾样强回声/钙化、动脉血流频谱、RI>0.7等特征,具备这些典型特征越多,恶性几率越大。恶性肿瘤确诊必须通过病理学检查,即穿刺活检和手术活检。任何影像学检查,包括彩超、钼靶、核磁共振这些均不能100%确诊。
关于钼靶:
钼靶检查不适合致密性乳腺,粗大、散在分布的钙化灶一般为良性钙化,段样、簇状分布、细线样的细小钙化灶为可疑恶性,需要穿刺活检。
最近遇到很多人彩超4a、4b、4c,甚至5类的,不去穿刺,回家吃中药。这种做法非常危险,极有可能拖延病情到不可挽回的地步。
【彩超评级3类需定期复查,4a、4b、4c、5类必须穿刺活检】
彩超是腋下淋巴结状态判断最主要的方式,淋巴结的转移与否与淋巴结结构关系很大,而与淋巴结大小关系不大。良性淋巴结一般呈扁椭圆,而恶性淋巴结形状不规则,或呈圆形;良性淋巴结可见皮髓质结构,且分界较清,可见淋巴门结构,而恶性淋巴结一般皮质增厚,髓质消失,皮髓质分界不清,淋巴门结构不可见;良性淋巴结一般无血流,或较少血流,门型血流,而恶性淋巴结血流丰富,非核心来源血流。
【淋巴结肿大不代表转移】
关于穿刺活检:
首先,穿刺活检对早期乳腺癌来说根本不会导致转移。而对于晚期乳腺癌患者来说,转移部位的穿刺是有针道转移的风险,但是由于患者已经是晚期转移,所以影响不是很大。
粗针穿刺活检采用影像学引导,取组织进行病理学检查。理论上来说:穿刺是癌,那就一定是癌,穿刺不是癌,极大可能不是癌,根据一项研究,这个可能性大约是在97%以上。穿刺医生一般要多穿几条组织以降低失败率和假阴性率。有人觉得穿刺了还要手术,不如直接手术,其实这种想法是不对的,术前穿刺明确肿块的性质对手术方式很重要,有些人可能还需术前新辅助治疗,即术前化疗±靶向。
【穿刺不会导致癌转移】
关于术前检查:
术前医生会根据彩超结果判断你的临床分期,如果腋下淋巴结转移较多,或锁骨上下窝淋巴结存在异常,或肿瘤标志物和生化项存在异常,可能会进行全身性的检查,包括胸脑核磁共振、肺部CT、腹部彩超及骨扫描。有研究表明,临床1期、2期和3期患者通过骨扫描发现转移的概率分别为5.1%、5.6%和14%,而3期患者肝和肺阳性者分别为6%和7%。有些医院会常规进行这类检查。
对于淋巴结存在异常的病人,医生可能会采取淋巴结穿刺活检以明确淋巴结的性质,决定是否进行前哨淋巴结探查术、术前化疗等等。
病理报告及免疫组化:
对于穿刺到的组织,或手术切除组织,病理科医生首先会进行镜下观察,确定病变类型,包括有无坏死、核异型、核仁、核分裂象,初步判断良恶性,对于良性病变,有时需加做免疫组化协助判断。若查见明显癌组织,会进行组织学分级和免疫组化染色,指导下一步治疗方案。需要注意的是,穿刺有可能会低估组织学分级、KI67等,最终病理结果以术后病理为准。
通常,拿到报告后需要重点关注以下几个点,对预后和治疗非常重要:是原位癌还是浸润癌,如果是浸润癌,是导管癌还是小叶癌,还是其他癌?肿瘤多大?组织学分级是I还是II还是III?淋巴结转移了多少?ER、PR、Her2是阴性还是阳性?对病理报告的解读应该是综合进行评判,而非通过某个单一指标,比如有的人看到自己是三阴性就很虚,完全忽略自己是导管内癌,或者只是T1a的浸润癌。病理学类型也极其重要,如果肿瘤较大,免疫组化是三阴性,但病理学类型是腺样囊性癌,这种预后也是较好。所以对病理报告的解读应该需要全面、综合的进行解读,没必要因为单个指标的不佳而恐慌。
我们通过一张典型的病理报告来解读:
这是一张典型的术后病理报告,肿块大小3*4*2.5cm,病理学类型是浸润性导管癌伴少量高级别导管原位癌,组织学分级为2级,未查见脉管侵犯和神经侵犯。免疫组化ER阴性,PR阴性,Cerbb2强阳性,提示为激素受体阴性her2阳性型乳腺癌。淋巴结检出13枚,查见一枚癌转移,分期为T2N1,2b期。
接下来对重点一一解读:
肿瘤大小:在T分期中一般取浸润部分最长径,若未标明,按肿瘤大小最长径计算。如上例中,T=4cm,属于T2分期,在原位癌伴微浸润中需详细标明浸润最大径。对于浸润癌来说,肿瘤越大,预后越差。
淋巴结转移情况:分母为检出淋巴结总数,分子为转移的淋巴结总数。淋巴结转移个数越多,预后越差,分子分母之比越高,预后越差。一般前哨淋巴结会检出3枚以上,腋窝清扫术会检出10枚以上。
病理学类型:乳腺癌病理学类型分为非浸润性癌(导管内癌和小叶原位癌)、浸润性癌非特殊型(即浸润性导管癌)及小叶癌、小管癌、粘液癌、化生癌、大汗腺癌等特殊性癌。绝大多数乳腺癌患者为浸润性导管癌。有些癌预后较好,治愈率很高,如:腺样囊性癌、筛样癌、小管癌等。有些癌预后比较差,如:化生癌、炎性乳腺癌、微乳头状癌、印戒细胞癌等。
小叶原位癌目前若不做处理,发展成浸润性癌的可能性也比较小,故现在小叶原位癌已不属于癌,而导管内癌(导管原位癌)就是货真价实的癌了。什么是原位癌,什么是浸润癌呢?这里我作一个简单的比喻,大家一看就懂:导管原位癌相当于监狱里面关了一群犯人,但是一个都没有越狱,虽然他们里面有盗贼(Luminal型),有杀人犯(Her2型),更有恐怖分子(三阴性),但是因为都关起来了,所以对社会(身体)的危害是0,更不用关注是什么分型,切除就完事了,无需做化疗。而浸润性癌就相当于监狱门被攻破了,有犯人跑出来准备对你的身体作恶,这个时候,需要分辨跑出来的是盗贼,还是恐怖分子,因为他们的严重性肯定不一样,对付他们的手段也肯定不一样。
组织学分级:浸润性乳腺癌中,组织学分级与预后明确相关,由病理科医生经镜下观察腺管结构、核异型性、核分裂象进行计分。3-5分为高分化(浸润性癌I级/G1),6-7分为中分化(浸润性癌II级/G2),8-9分为低分化(浸润性癌III级/G3)。分数越高,预后越差。
脉管及神经侵犯:脉管侵犯又称为脉管癌栓、脉管浸润,其诊断必须看到癌栓位于内衬内皮细胞的管腔中,且必须在肿瘤附近,而不是肿瘤内部。脉管包括淋巴管和血管,淋巴管浸润会增加局部复发率,血管浸润有可能导致转移。有些报告会报出神经侵犯,目前,对神经侵犯的临床意义不明。脉管癌栓的预后价值属于第二梯队,低于淋巴结状态、肿瘤大小、ERPR的阴阳和高低、HER2的状态、KI67、年轻、组织学分级等因素,脉管癌栓属于低权重信息,不必过于惊慌。
分子分型:乳腺癌的分子分型至关重要,对预后及治疗具有重要意义。任何乳腺癌免疫组化均需报告:ER、PR、Her2(Cerbb2)、Ki67这四个指标,并根据这四个指标将乳腺癌分为Luminal A(管腔A型,2阳1阴)、Luminal B(管腔B型,2阳1阴或3阳)、Her2过表达型(2阴1阳)和基底样型(三阴性型)。注:基底样和三阴有区别,普通病友不做细分介绍,这里统称为三阴性
Luminal A型:ER阳性,PR阳性且高表达(大于等于20%),Her2阴性,Ki67低表达(低表达为小于等于15%,高表达为大于等于30%,两者之间根据其他指标判断);
Luminal B型Her2阴性型:以上PR或Ki67不符合A型的,统一划入B型;
Luminal B型Her2阳性型:ER阳性,PR阳性,Her2阳性;
Her2过表达型:ER阴性,PR阴性,Her2阳性;
三阴性型:ER阴性,PR阴性,Her2阴性。
免疫组化:我在这里列举了一些常见的免疫组化指标,供查询。
ER:雌激素受体,表示患者可以接受内分泌治疗,阳性好,百分比越高越好,+号越多越好(越强越好)
PR:孕激素受体,表示患者可以接受内分泌治疗,阳性好,百分比越高越好,+号越多越好(越强越好)
HER2/CERBB2:-/0/1+阴性,2+需要做FISH进一步检测,3+阳性;若FISH检测为阳性和3+需要靶向治疗
HER2是一种原癌基因,过表达的患者需要进行针对HER2的靶向治疗。HER2过表达患者对含有多西他赛的化疗方案效果较好(NSABP-11研究),但可能容易对他莫昔芬耐药。HER2过表达患者一般肿瘤分级高较高,肿瘤体积较大,淋巴结转移较多。
KI67:肿瘤增殖指数,越低越好,治疗后可改变,越高分化越差,长得越快,对化疗越敏感。<15低表达,>30高表达,15-30之间根据其他指标判断
AR:雄激素受体,晚期三阴雄激素受体阳性者中可能应用抗雄激素治疗
P63:原位癌阳性,浸润癌阴性,部分基底样浸润癌可表达阳性
P53:抑癌基因蛋白,阴性/野生型好
野生型的P53基因能够抑制细胞恶变,控制细胞增长,而突变型的P53基因则能促进细胞恶性转化。正常的P53蛋白很快会被分解掉,染色较弱或阴性,而突变型P53蛋白存在于癌细胞的核内,免疫组化染色阳性。P53基因过表达与较差的肿瘤分化和较低的ER有关。目前对P53的预后价值存在争议,即一部分研究者认为P53突变影响淋巴结阴性患者的生存期,而另一部分研究者否认这之间的关系。
P16:抑癌基因蛋白,阳性好
P16能参与细胞周期的调控,通过抑制CDK4抑制细胞生长,若P16基因发生结构突变和功能缺失,导致细胞进入恶性增殖。
bcl-2:原癌基因蛋白,阳性好
bcl-2产物与细胞凋亡有关,其预后价值一直存在争议。多数报道认为bcl-2表达与组织学分级负相关,有人认为bcl-2虽抑制了肿瘤凋亡,但延长了细胞周期,延缓了肿瘤增殖,同时有研究者提出,bcl-2蛋白是由雌激素调节,故认为bcl-2高表达者预后良好,是因为患者能在内分泌治疗中获益更多。
CK5/6:细胞角蛋白,原位癌及基底细胞样三阴乳腺癌中呈阳性
E-cadherinE钙:钙黏附蛋白,表达越高可能预后越好。浸润性小叶癌表达阴性,
Calponin:鉴别原位癌和浸润癌,同P63
SMA:鉴别原位癌和浸润癌,同P63
EGFR:HER1,阴性好
EGFR是一种原癌基因,可引起细胞过度分裂和增殖。其表达率跟ER和PR负相关,表达越高预后越差,三阴性乳腺癌中表达率高。EGFR低表达或不表达患者对内分泌治疗效果较好。
P120:区分肿瘤的病理学类型,膜+为导管癌,浆/质+为小叶癌
VEGF:血管内皮生长因子,表达越高预后越差
GCDFP15:区分肿瘤的病理学类型,大汗腺癌表达阳性
GATA3:转录因子,表达越高可能预后越好
TOPOII:拓扑异构酶II,表达越高预后越差、对蒽环化疗越敏感。
CD31:证明肿瘤内内皮细胞存在,评估肿瘤血管生成和微血管密度,阴性好
CD8:鉴别复旦分型的三阴性免疫调节型,阳性越高越好,可能使用免疫治疗获益
Foxc1:鉴别复旦分型的三阴性基底样免疫抑制型,阴性好
Dclk1:鉴别复旦分型的三阴性间质型
Syn:鉴别是否存在神经内分泌化
CgA:神经内分泌标记物,同Syn
关于分期
目前最常用的是AJCC的TNM分期。T代表肿瘤大小,N代表淋巴结转移情况,M代表远处转移。珠玉在前,具体内容我就直接当搬运工了:
乳腺癌的T分期
Tis:原位癌。
T1(包括T1a、T1b和T1c):肿瘤最大直径小于等于2厘米。
T1a:肿瘤最大直径大于1毫米,但不超过5毫米。
T1b:肿瘤最大直径大于5毫米,但不超过10毫米。
T1c:肿瘤最大直径大于10毫米,但不超过20毫米。
T2:肿瘤最大直径大于2厘米,但不超过5厘米。
T3:肿瘤最大直径超过5厘米。
T4:长入胸壁或皮肤中的任何大小的肿瘤(溃疡或肉眼可见的结节)。这包括炎症性乳腺癌。
淋巴结病理分期pN分类标准如下。
pN0:未发现区域淋巴结转移或仅发现孤立的肿瘤细胞
pN1:1-3个腋窝淋巴结转移
pN2:4-9个腋窝淋巴结转移
pN3:10个或10个以上腋窝淋巴结转移
远处转移
MX:不能评估。
M0:未发现远处扩散。
M1:远处器官转移。
以上内容出自:
本人稍作整理
第八版AJCC分期将组织学分级,免疫组化指标ER、PR以及Her2的状态加入了预后分期中,并提倡使用。有心的病友可根据最新分期表分期,上文中有,我在这里就不再引述了。
对于分期,也可以按照上面的罪犯比喻来理解。如果跑出来的癌细胞作恶多端的恐怖分子(三阴性),在它对身体做大量坏事之前处理掉(手术+化疗),那么预后一样是极好的。如果跑出来的是盗贼,但已经做了很多坏事(分期较晚),那么预后是比较差的。最新的AJCC分期结合了分期及免疫组化,就相当于对罪犯的本质(是杀人放火还是小打小闹)以及已经做过的坏事(是江洋大盗还是偷鸡摸狗)进行综合评判,无疑,这种分期是更科学合理的。
【划重点】分期比分型更重要。
关于预后
乳腺癌的预后相信是大家最关心的话题了,乳腺癌的预后极其复杂,与多种基因表型及病情有关。目前判断预后四个最重要的指标为病理学类型、组织学分级、病理分期和分子分型。
以下图片是我自己制作的一张分期预后图,仅供各位参考:
不难看出,乳腺癌的复发率是比较低的,尤其是早期乳腺癌,即0期、1期和2期。即使到了中期,治愈率仍有一多半以上,如果不幸到了晚期,五年生存率也能达到一个可观的水平。尤其是骨转移,可以长期带瘤生存。值得注意的是,这些数据是08年到16年,当时的治疗条件跟现在不可同日而语,目前的治愈率在这个基础上肯定是会更加提高的。
由于第八版的AJCC才把分子分型加入预后分期,目前还没有一些TNM并分子分型的预后数据出来。大家可在上表中适当做加减法,比如预后比较好的luminal型可下调复发率,而预后相对比较差的三阴性乳腺癌可适当上调。
关于三阴性乳腺癌,我想引述一下上海市第一妇婴保健院成小林医生的文章:
很多患者非常紧张三阴性乳腺癌,三阴乳癌是指雌激素受体(ER)、孕激素受体(PR)和HER2均阴性的乳腺癌,有谣言三阴性乳癌5年复发率80%,据说是网上查的,我非常诧异有这样不负责任的数据在患者中流传。所以收集了近10余年一些肿瘤诊疗中心在专业杂志发表的相关数据给大家(数据可能不是十分全面,但能一定程度反应三阴性乳腺癌的生存状况。另外,可能因为各家统计的数据差异不大,所有不是所有诊疗机构都做相似统计发表论文)。
2000年1月-2004年12月中山大学肿瘤防治中心1280例乳腺癌,23.8%(305/1280)病例为三阴性乳腺癌,诊断时通常肿块较大、年轻、淋巴结阳性较多,有乳腺癌家族史的患者较多。截止至2007年6月,三阴乳腺癌组患者中位随访时间为52个月(28~89个月)。三阴乳腺癌患者的5年无病生存率和总生存率分别为73.7%和88.5%,低于非三阴乳腺癌患者(80.8%和92.8%)。
2003年-2010年海南医学院肿瘤研究所560例乳腺癌患者回顾性分析,三阴性乳腺癌患者的3年生存率及5年生存率为85.5%和73.3%,低于非三阴性乳腺癌患者(95.1%和88.0%,P<0.05)。
2002年1月~2002年6月天津医科大学附属肿瘤医院509例乳腺癌,21.4%(109/509)的病例为三阴型乳腺癌,其髓样癌、组织学Ⅲ级的比例以及复发转移率高于非三阴型乳腺癌(P<0.05)。三阴型乳腺癌和非三阴型乳腺癌5年无瘤生存率分别为78.9%和87.3%。
2004年1月-2005年1月天津医科大学附属肿瘤医院1264例乳腺癌,19.46%(246/1264) 病例为三阴性乳腺癌。与非三阴比较,三阴性乳腺癌患者小于35岁的患者所占比例大8.54%(21/246),有乳腺癌家族史者多8.13%(20/246),肿瘤直径≥5cm者多11.79%(29/246),腋窝淋巴结阳性者多58.13%(143/246),组织学分级较高,Ⅲ级占20.73%(51/246)。三阴性乳腺癌患者的5年无瘤生存率和总生存率分别为79.67%(196/246)和89.84%(221/246)。
2005年-2009年美国Lehigh Valley HealthNetwork机构回顾性研究,224例三阴性乳癌,年龄范围29至88岁,41例为0期,72例为1期,64例为2期,24例为3期,23例为第4期。总体5年生存率为78.6%。5年生存率阶段明显包括0期92.7%,1期95.8%,2期78.1%,3期54.2%和4期26.1%。其中基因检测的32个病例中,17个具有野生型,9个具有BRCA1突变体,6个具有BRCA2突变体。BRCA突变的患病率为三阴性乳腺癌病例的7.21%。低于其他文献中报道(预测值约为TNBC的20%)。这种变化的可能原因包括诊断时的年龄和患者拒绝接受检测。
2017发表的来自美国MD Anderson乳腺癌数据库的研究数据,873例5年以上的三阴性乳癌患者,中位随访时间为8.3年。10年无复发间隔(RFI)为97%,无复发生存(RFS)为91%,为92%;15年无复发间隔(RFI)为95%,无复发生存(RFS)为83%,远期无复发生存(DRFS)为84%。5年以上无复发的三阴性乳癌在随后的10年里再发生复发的概率非常低。
单因素分析显示淋巴结状态、肿瘤大小、临床分期、脉管瘤栓对患者总生存率有影响。多因素分析显示淋巴结状态和肿瘤大小是影响三阴乳腺癌总生存率的独立因素。患者年龄、病理类型、肿瘤大小、临床分期、组织学分级,特别是淋巴结状态对于判断预后有重要指导意义。另外还有个体的具体状况以及对治疗的敏感性,以上数据仅作参考,相信自己属于大多数能够治愈的群体,勿焦虑,勿听信谣言!
目前网络上充斥着许多谣言,希望大家科学的认识,不要听信谣言,对自己或者是家属朋友的病情抱有信心和期待,不要信百度,不要信百度,不要信百度,重要的事情说三遍。预后情况是本文的核心,也是病友最关心、最恐惧的,预后也涉及到很多问题,我将在接下来详细叙说,打了这么多字手快抽筋了,先写到这里,希望以上内容能够让大家对自己的病情有一个初步的了解。写的匆忙,疏漏以及错误的地方请大家指正。
接下来还有手术、化疗、放疗、内分泌治疗、分子靶向治疗等多个方面的内容,敬请期待。
这里对乳腺癌各个分型做一个简单的描述:
据中国乳腺癌多中心临床流行病学研究发现,我国Luminal A型,Luminal B型,Her2过表达型和三阴性型构成比例分别为:54.5%、14%、8.8%、22.7%。
基底样型乳腺癌(BLBC),特征为不表达ER、PR、HER2,不同程度的表达CK5/6、CK14、CK17以及P63、SMA和EGFR。可根据免疫组化ER(-)、PR(-)、HER2(-)、CK5/6(+)和FOXC1(+)来判断。本类型的乳腺癌多呈低分化,III级,多为浸润性导管癌,通常多数淋巴结阴性,但容易较早发生血道转移,主要治疗方式为化疗,具有高频BRCA1/2胚系突变。
根据复旦大学附属肿瘤医院发布的数据,早期和中期三阴性乳腺癌五年复发率大约16%。注:基底样型乳腺癌并不等同于三阴性乳腺癌,然大多数重叠,数据仍有参考价值,本文不为患者作深层介绍,遂将二者等同。
腔面型乳腺癌(Luminal 型),特征为基因表达谱上高表达ER、PR基因,可进一步分为腔面 A型和腔面 B型。根据2015、2017 St.Gallen专家共识,对于Her阴性的患者,激素受体(HR)阳性率高、低增殖活性、低肿瘤负荷及肿瘤分级低(I-II级)更倾向于A型,相反, HR阳性率低、高增殖活性、高肿瘤负荷以及肿瘤分级高(III)更倾向于B型。腔面 A型大多数仅需内分泌治疗,高危患者可加化疗,而腔面 B型在内分泌治疗的基础上,绝大多数药加用化疗。
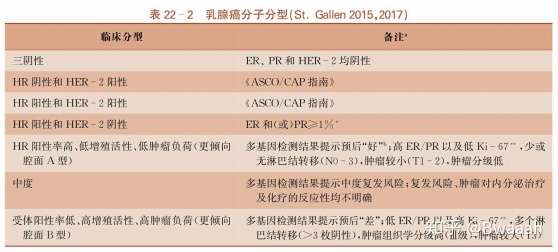
若存在Her2过表达,直接列入腔面 B型,且需要在内分泌治疗、化疗的基础上加用分子靶向治疗,也就是网上提到的豪华套餐,三阳性乳腺癌,此类患者一般增值指数较高,组织学分级多为3级或2级。
根据复旦大学发布附属肿瘤医院的数据,早期和中期腔面A型乳腺癌五年复发率大约为8%,腔面B型(Her2-)乳腺癌五年复发率大约为12%,腔面B型(Her2+)乳腺癌五年复发率大约为13%。
HER-2过表达型:HER-2全称为人表皮生长因子受体-2,属于原癌基因,该基因扩增的乳腺癌淋巴结转移率高,增值速度快,多为低分化。该类型乳腺癌免疫组化为:ER-,PR-,HER2 3+,或HER2 2+,FISH阳性。治疗以化疗+分子靶向治疗为主,随着曲妥珠单抗(赫塞汀)等靶向药物的出现极大的改善了该类型乳腺癌的预后,而在这些药物出现之前,该类型乳腺癌的预后是最差的。
根据复旦大学附属肿瘤医院发布的数据,早期和中期HER-2过表达型乳腺癌五年复发率大约为13%。
(以上数据均来自复旦大学附属肿瘤医院2008-2016年手术治疗的22581例0-3期患者)
忙了大半天,终于有点时间来更一下我的文章,感谢各位的支持。接着说。
关于治疗方式
乳腺癌目前有五大治疗方式:手术、化疗、放疗、内分泌治疗和分子靶向治疗。目前,原位癌的治疗以手术+放疗为主。浸润性癌则要视分子分型和其他情况而定。一般来说所有保乳患者均需放疗,淋巴结转移患者可考虑放疗,淋巴结转移较多患者均需放疗。
luminal型淋巴结没有转移,并且临床危险因素较低,比如年龄较大,肿瘤比较小,ki67比较低,组织学分级较低等,可以做一个21基因检测(Oncotype dx)。若复发风险较低,可考虑豁免化疗,仅行内分泌治疗。对临床高危患者,如年龄很小、肿瘤较大等,即使21基因检测结果复发风险很低, 对豁免化疗也需非常谨慎。而且国内21基因检测目前还尚有许多问题,因此建议早期淋巴结没有转移的,有高危因素的患者,在身体能够耐受化疗的情况下还是有必要直接做个4-6次低强度化疗。对于是铁了心就想逃化疗的,可考虑21基因检测看看有无机会。T1aN0可直接考虑内分泌治疗(参考2020 NCCN指南)。淋巴结转移1-3枚的患者,如果21基因检测是低危,那么化疗的获益可能很小。
her2过表达型患者,肿瘤大于5mm的,均需化疗+曲妥珠单抗靶向治疗。对于淋巴结有转移,或者淋巴结没转移但有肿瘤较大等危险因素者建议化疗+曲妥珠单抗+帕托住单抗,也就是双靶向治疗。肿瘤比较小的,如T1a患者,对于是否需要化疗和靶向治疗,目前有争议,视具体病理情况由主治医生来定。
三阴性患者在肿瘤比较小的情况下可视病理情况考虑豁免化疗,肿瘤大于5mm的均需化疗。
下面对这五种治疗做一些详细介绍,旨在帮助患者了解基本治疗方式,并在某些情况需要自主选择和决定时,做出可能更加正确的选择。
关于手术
手术是早期和中期乳腺癌最重要的治疗方式,从最开始的根治性手术(切除乳腺、胸大肌、清扫腋窝淋巴结)到现在的保乳+前哨探查术,切除范围一直在缩小,在保证治疗效果的同时对手术一步步做减法,改善患者的生存质量。乳腺癌患者不同于其他癌症,是可以长期长存的,因此生存质量显得尤为重要。
术前会对你全身情况做评估,包括体格检查,血常规尿常规,肝肾功能,心电图,钼靶,彩超,核磁共振,胸部CT等。通常,手术适应症为0期、1期、2期,以及部分3期患者,如有新辅助治疗指针,如肿块大于5厘米,淋巴结转移,her2阳性或三阴且肿块大于2厘米等情况,可考虑新辅助治疗后再进行手术。如果患者肿块较大并有保乳的意愿,也可考虑新辅助治疗,待肿块缩小后再手术。
需要注意的是,如果肿瘤位于内象限,要关注内乳淋巴结。
如果你满足保乳的条件,比如肿块距乳头比较远,没有广泛钙化,可进行术后放疗等,建议进行保乳。保乳+放疗的治疗效果跟全切是一样的,如果医生通知你可以进行保乳,那是一件非常好的事。对于brca胚系致病性突变患者,不建议保乳。对于保乳患者来说,根据复旦大学附属肿瘤医院发布的08-16数据来说,十年生存率达到91.5%,全切患者的十年生存率则是86.9%,这可能与保乳患者病情相对较轻有关,也有可能与接受放疗有关。侧面也反映了保乳手术的安全性,值得注意的是,这还是多年以前的数据。有时候手术中多次不能达到切缘阴性,也就是说多次切除后仍有癌细胞残留,那就很遗憾,只能进行全切手术。
当前我国保乳率偏低,不到20%,而发达国家保乳率在50%以上,与国内患者普遍分期较晚、观念认知、医疗条件及医患关系相关。根据多项研究显示,保乳+放疗和全切能达到一样的治疗效果。保乳后的局部复发率跟患者分子分型明显相关,Her2过表达型和三阴性的局部复发率显著高于Luminal型患者。
关于保乳+放疗和全切手术疗效的对比试验,有:WHO Milan研究、EORTC 10801、NCI、Danish DBCG-82TM临床研究等,得出的结论均为保乳手术与乳房全切具有相似的疗效,有兴趣者可以查阅相关资料进一步了解。
要说的另一个重要的事情就是腋窝清扫了。对于彩超及其他检查,没有发现异常淋巴结的,常规进行前哨淋巴结活检,如果有异常淋巴结并经过穿刺证实是癌转移,那就直接进行腋窝清扫。前哨淋巴结是癌细胞进行淋巴结转移的第一站,一般来说前哨淋巴结没有癌细胞,后面其他淋巴结也都是安全的,前哨淋巴结活检术可以安全有效的代替腋窝清扫术,极大的提高患者的生存质量。腋窝淋巴结有三组,前哨淋巴结属于第一组中的一部分,如果术前穿刺活检证实腋窝淋巴结转移,将对第一组和第二组腋窝淋巴结进行清扫,一般来说需要至少10枚。当第二组淋巴结或第三组淋巴结存在肉眼可见的病变时,会扩大至清扫第三组淋巴结。三组淋巴结如果都被清扫,患者水肿率高达50%。
前哨淋巴结活检术常规在术前及术中定位两次,以便尽量能全部检出。以往,前哨淋巴结如果发现癌转移,会常规进行腋窝淋巴结清扫术。但是近年,Z0011试验证明,如果前哨淋巴结只转移1-2枚,术后辅以放疗可代替腋窝淋巴结清扫术。但是也有适应症的,如果你前哨只检出1枚前哨淋巴结,1枚癌转移,那肯定要继续进行淋巴结清扫,常规至少要检出2-3枚。前哨淋巴结如果检出失败,会常规进行腋窝淋巴结清扫。
对于保乳和保腋窝,这两者之间没有内在关联,也就是说你的手术方式有四种组合:保乳+前哨,保乳+腋清,全切+前哨,全切+腋清,互不影响。对于可以保乳和保腋窝的患者来说,那是极其幸运的,尤其是腋窝,对生活质量影响很大,也说明病情比较轻,当然,对于全切和腋窝清扫的患者也不是说病情重,不能这样倒推。有些医院没有前哨的经验,没有术中病理的技术,只能进行全切和腋清。
目前的乳腺癌手术都是全麻,没有多大痛楚,眼睛一闭一睁等着康复就好了,有些人做完手术第二天就出院了。就痛苦而言,比起化疗那简直是跟吃饭一样轻松,只是心里负担大,觉得要动刀子。手术对大多数乳癌病人来说是进行的第一项治疗,对某些病情很轻的病人来说可能也是最后一项治疗,由确诊到手术这段时间是最恐惧、最令人不安的,一旦手术完毕,术后病理结果出来以后,你的病情及治疗方式就已基本确定。
关于手术还有很多可以说的,本文写的比较随性,没有什么系统性,只能想起什么说什么,难免有遗漏,以后根据情况再进行补充。手术部分目前就说这么多,有时间接着更。
关于新辅助治疗
术前进行的治疗叫新辅助治疗,术后进行的治疗叫辅助治疗。新辅助治疗里面包括新辅助化疗,新辅助内分泌治疗,新辅助靶向治疗等,新辅助内分泌治疗很少应用。新辅助治疗的目的是缩小肿瘤便于手术,降期(降低病人的分期)增加保乳机会,同时根据肿瘤的变化情况,了解肿瘤是否对方案敏感,以便确定合适方案,并且有助于判断预后。新辅助治疗更多应用于三阴性及her2过表达的患者,方案以TAC和TCbHP为主,关于化疗方案后面一章会详细说到。
新辅助化疗也有缺点,如:延长患者体内带瘤时间,如果治疗无效则会导致疾病进展,取材有限导致治疗误差等。总之,选择新辅助化疗或辅助化疗,依主治医师判断。
新辅助化疗前会对瘤床进行标记,如:文身标记、放置钛夹等,以便确定后续手术范围。腋窝淋巴结阳性的患者经穿刺证实,也可能会进行标记。
对her2阳性的患者来说,如果术后病理达到完全缓解(pCR),即经过新辅助治疗,术后已无浸润性癌细胞残留,推荐术后行1年单靶或双靶治疗。如果术后病理没有达到pCR,还有浸润性癌残留,推荐使用T-DM1进行治疗,此药较贵,依经济条件选择。
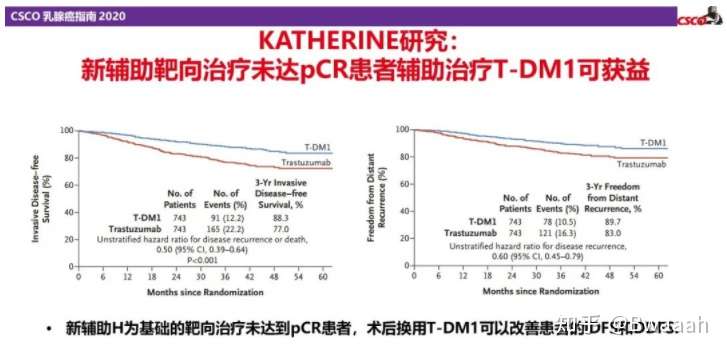
对三阴性患者来说,如果术后病理达到pCR,则术后无需继续化疗。如果没有达到pCR,推荐使用口服化疗药卡陪他滨辅助治疗6-8个周期。对于her2阳性和三阴性乳腺癌来说,新辅助治疗后,残留浸润癌越少,预后越好。如果肿瘤无变化,或进展,则预后不佳。对于Luminal类型患者来说,新辅助治疗无论是否达到pCR,预后都不错。
一句话概括,术前新辅助治疗达到pCR者与预后良好的相关性,以三阴性最为明显,HER2阳性患者次之,激素型最弱。
【划重点】对于三阴型和HER2阳性患者,新辅助治疗后,癌残留越少,预后越好。
关于辅助化疗
大多数乳腺癌患者在就诊时可能已经存在血道转移,而目前的手段并不能检出这些已经存在于全身的微小癌细胞,局部手术切除也不能杀灭这些已经转移的癌细胞,因此,只有通过全身性的治疗,如化疗、内分泌治疗、分子靶向治疗等,才有可能杀灭体内残存的癌细胞,降低患者的复发风险。大多数乳腺癌患者均需辅助化疗。癌细胞呈指数性生长,根据一级动力学原则,一定剂量的化疗药物只能杀灭一定比例的癌细胞,因此化疗后肿瘤细胞数量也呈指数性下降,因此,切不可产生“化疗一次有效就全部杀完、只做一次化疗、做三次跟做四次一样”等错误想法,对于耐受的患者一定要坚持做够疗程。
辅助化疗的时间为术后四周以内,化疗前要充分评估患者的血常规、肝肾功能、心电图等,术后辅助化疗一般不与内分泌治疗和放疗同时进行,可跟靶向治疗同时进行。辅助化疗的给药方式一般是静脉注入,患者一般需要植入PICC或输液港,PICC价格便宜、维护麻烦,输液港价格昂贵、维护简便、需做小手术植入,具体可百度查询,酌情自由选择。化疗药物的剂量与体表面积有关,可根据身高体重计算自己的体表面积,在向医生报身高体重时必须准确。化疗一般需住院进行,常见的副作用有:呕吐、脱发、骨髓抑制(白细胞、中性粒细胞下降)、疲乏、头晕、过敏、手脚变黑、口腔溃疡等,每个人每次反应均不同,症状出现前无法预测。化疗开始上药后需多喝水,结束后多休息保存体力,少食多餐。化疗的疗效如何,在辅助治疗阶段无法评估,不可根据病人的副作用来反映化疗疗效,这两者没有关系。
化疗开始前,使用肚皮针(戈舍瑞林或亮丙瑞林)抑制卵巢功能,可以降低化疗药物对卵巢的损害,防止卵巢衰竭。推荐有生育需求的患者考虑使用,或进行冰冻胚胎和卵细胞等。
蒽环类药物对心脏损伤不可逆,有心血管疾病者可考虑使用右雷佐生预防蒽环类药物的心脏毒性,多柔比星脂质体可能会减少蒽环类药物的心脏毒性。
化疗止吐药首选5-HT3受体阻断药(司琼类)联合地塞米松,如呕吐严重,可在此基础上加nk1受体拮抗剂,如阿瑞匹坦,商品名为意美。
骨髓抑制可预防性打升白针,有短效和长效,轻微骨髓抑制可观察,3度骨髓抑制(白细胞小于2,中性粒细胞小于1)必须打针。
目前乳腺癌的化疗以蒽环类药物和紫杉类药物为主,这里把目前早期常用方案做一个简单介绍,分为含曲妥珠单抗方案和不含曲妥珠单抗方案。
用于乳腺癌的常用化疗药物有:
生物碱类:紫杉醇、长春瑞宾、多西他塞
代谢类:吉西他宾、甲氨蝶呤、5-FU、卡陪他滨
抗生素类:多柔比星、表柔比星、吡柔比星
烷化剂类:环磷酰胺
铂剂类:卡铂
以下只介绍常用辅助化疗方案
A:多柔比星;E:表柔比星;T:多西他赛;C:环磷酰胺;P:紫杉醇;Cb:卡铂
(A和E均为蒽环类药物,以下方案中的A同指E)
不含曲妥珠单抗方案
TAC:多西他赛、多柔比星、环磷酰胺,21天为一个周期,共6个周期,此方案多用于HER-2阴性患者的新辅助化疗;
AC-T:多柔比星、环磷酰胺,21天为一个周期,共4个周期,结束后使用多西他赛,21天为一个周期,共4个周期,合计共8个周期;
AC-P:多柔比星、环磷酰胺,21天为一个周期,共4个周期,结束后使用紫杉醇,7天为一个周期,共12个周期,合计共16个周期;
TC:多西他赛、环磷酰胺,21天为一个周期,共4个周期;
AC:多柔比星、环磷酰胺,21天为一个周期,共4个周期,不推荐;
AT:多柔比星、多西他赛,21天为一个周期,共4个周期,不推荐;
高危患者可考虑AC-P密集型化疗;
注:
1、E1199试验表明,AC-T方案中使用多西他赛三周方案较紫杉醇三周方案明显改善DFS,故不推荐AC-T中使用紫杉醇三周方案。
2、BCIRG005试验表明,AC-T方案与TAC方案疗效相当,但前者血液毒性显著低于后者,故推荐术后化疗优先考虑AC-T方案。
3、US Oncology 9735试验表明,TC方案较AC方案显著改善患者DFS且耐受性较好(中位随访七年,81%对比75%),故推荐中低危患者术后化疗优先考虑TC方案。
4、三阴性BRCA突变患者可考虑加用铂类化疗。
含曲妥珠单抗方案
AC-TH(P):多柔比星、环磷酰胺,21天为一个周期,共4个周期,结束后使用多西他赛+靶向,21天为一个周期,共4个周期,合计共8个周期,靶向用满一年,或使用周疗紫杉醇12个周期,合计共16个周期,靶向用满一年;
TCbH(P):多西他赛、卡铂、靶向,21天为一个周期,共6个周期,靶向用满一年;
TCH:多西他赛、环磷酰胺、曲妥珠单抗,21天为一个周期,共4个周期,靶向用满一年;
TH:紫杉醇、曲妥珠单抗,周疗,共12个周期,靶向用满一年;
注:
1、使用单靶或双靶,在靶向治疗一章讨论。
关于辅助化疗的介绍就写到这里,有遗漏的后续再进行补充。
关于辅助内分泌治疗
雌激素是一种致癌原,控制细胞周期G1期至S期的转变,驱动细胞增殖。雌激素对乳腺上皮具有致癌作用,孕激素阳性的细胞可以进一步受到刺激。
ER(雌激素受体)和PR(孕激素受体)是患者重要的预后指标,也是内分泌治疗的依据,其检测至关重要,如果是阳性,则可以通过阻止癌细胞接收雌激素信号,抑制肿瘤生长,使肿瘤凋亡。ER和PR阳性的定义为大于等于1%。但是在1%至9%区间里,生物学行为可能更接近三阴,内分泌治疗效果欠佳。
一般来说,激素受体阳性的乳腺癌分化程度比较好,多呈双倍体,增值较低,化疗效果较差,内脏转移概率较低,激素受体阴性的则分化较差,常见异倍体,增值较高,化疗效果较好,更容易发生内脏转移和脑转移。
由于PR的表达也受雌激素的调节,所以PR阳性的乳腺癌,其ER大多数情况下也是阳性。ER和PR的免疫组化一般有百分比和强弱两个指标。百分比意味着有多少细胞着色,强弱意味着着色程度(见下图)。一般来说,一个+表示弱阳,两个+表示中阳,三个+表示强阳。ER和PR的百分比越高,阳性程度越强,提示内分泌治疗效果越好。
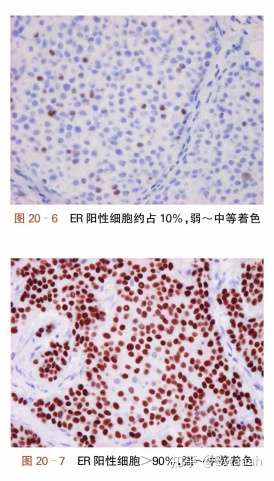
由上述可知,对于激素受体阳性的乳腺癌,有两种内分泌治疗策略。一种是降低激素水平,一种是与激素竞争结合癌细胞的雌激素受体,如何来理解这两种策略呢?我之前做过一个比喻:癌细胞相当于一名宅男,吃饭全靠外卖,那么就有两种办法杀死癌细胞,第一种就是把外卖员干掉,没人给它送外卖,它就会饿死,这种相当于降低激素水平。第二种办法就是把它门堵上,不让外卖员与它接触,也自然是饿死了,这就是竞争结合雌激素受体。
简单介绍一下绝经前后雌激素的产生,以便更容易理解方案:绝经前雌激素主要通过卵巢来产生,所以要降低激素水平,需要抑制卵巢功能(OFS),要么进行卵巢切除,要么打戈舍瑞林或亮丙瑞林(肚皮针)来抑制卵巢功能。绝经后雌激素主要通过雄激素经芳香化酶转化为雌激素,如果要降级激素水平,就需要AI药物(芳香化酶抑制剂)。
内分泌治疗的时间为辅助化疗之后,一般不与辅助化疗同步进行,以免可能出现的降低化疗疗效。内分泌治疗药物主要有两种类型,降低雌激素水平的AI类:来曲唑、阿那曲唑、依西美坦和不降低雌激素水平的受体拮抗剂:他莫昔芬(三苯氧胺)、托瑞米芬、氟维司群。以下方案中将他莫昔芬与托瑞米芬合称为TAM。
对于绝经前患者的内分泌治疗方案,主要有三种:TAM、OFS+TAM、OFS+AI。这三种方案疗效依次升高,适用于不同复发风险的患者,一般患者均为中危起步,需OFS。序贯方案这里不再介绍。绝经后患者的内分泌方案目前只有AI。
对于导管原位癌,需明确ER状态。根据一项乳腺癌预防试验提示,非典型增生患者接受他莫昔芬治疗后,浸润性乳腺癌的发生率可以降低75%。另有多项试验表明,内分泌治疗可降低ER阳性原位癌患者的复发率。基于此,推荐ER阳性的保乳患者使用他莫昔芬或AI进行内分泌治疗。
双膦酸盐在预防骨转移方面有明确作用,NCCN指南推荐接受内分泌治疗的绝经后患者考虑使用双膦酸盐辅助治疗。服用他莫昔芬药物期间,雌激素水平增高是正常现象。
对于内分泌方案另一个比较重要的就是治疗时间问题了,一般至少5年,推荐STEPP复发风险模型及CTS5复发风险模型来计算风险,并建议中高风险的患者延长内分泌治疗时间至10年,以及选择更高阶梯的治疗方案。
CTS5复发风险计算:
如果打不开网站,直接套公式计算:CTS5评分=0.438×阳性淋巴结个数+0.988×(0.0934×肿瘤大小-0.001×肿瘤大小平方+0.375×肿瘤分级+0.017×年龄)。以3.13和3.86分作为分界低危,中危和高危的cut-off值。
STEPP工具这里不提供了,留个作业,自己去小程序找,有两个版本注意鉴别。
关于绝经的定义,必须满足以下任意状态:1、双侧卵巢切除;2、年龄大于60岁;3、年龄小于60岁,停经大于1年,1年内未接受化疗、内分泌治疗等情况下,促卵泡激素和雌二醇在绝经后范围;4、年龄小于60岁,正在服用TAM的患者,连续两次测促卵泡激素和雌二醇在绝经后范围。
【内分泌药需要至少吃5-10年,哪里不舒服找医生咨询,切勿擅自停药,擅自停药后复发成晚期的例子太多了,到时候后悔莫及】
关于分子靶向治疗
广义的靶向治疗是指针对癌细胞的特异性靶点进行打击,而不会波及,或者较少波及正常细胞,包括针对HER2靶点的曲妥珠单抗、针对周期蛋白依赖性激酶4和6靶点的的CDK4/6抑制剂、针对VEGF靶点的阿帕替尼等等。狭义的靶向,即本节要讨论的靶向治疗,专指对HER2靶点的治疗。
原癌基因HER2属于EGFR家族,共有:HER1(EGFR)、HER2、HER3、HER4四兄弟,它们是存在于细胞膜,是跨膜的酪氨酸激酶受体。HER2的过表达或扩增使肿瘤恶性程度高,容易复发和转移,还可能会导致患者对某些药物耐药,如:某些化疗药、他莫昔芬、AI等。
HER2是乳腺癌重要的预后因子,预测价值甚至高于激素受体状态和淋巴结有无转移。如果没有有效的抗HER2治疗,那么HER2阳性的患者较阴性患者进展快、复发率高、预后差。目前,用于早期乳腺癌抗HER2治疗的药物有:曲妥珠单抗(赫塞汀)、帕妥珠单抗(帕捷特)、T-DM1(赫塞莱)、来那替尼。从临床病理学特征分析,HER2扩增的乳腺癌常表现为高级别、ER和PR低/不表达、KI67较高,病情进展较快等。对于HER2阳性的患者,如果能进行有效的抗HER2治疗,其预后不差于HER2阴性患者。
对曲妥珠单抗的使用时间探索主要集中在9周、6个月、1年和2年。HERA研究显示曲妥珠单抗2年的疗效并不优于1年,PHARE研究、Short-HER研究、FinHER研究均不能证明短疗程的曲妥珠单抗疗效不差于1年,根据目前证据,1年的曲妥珠单抗为标准治疗方案。由于心肌细胞也表达HER2,曲妥珠单抗有心脏毒性,故不可与蒽环类化疗药物一起使用,常跟紫杉类药物联合使用。靶向治疗一般在术后四周内,于化疗同时开始。
患者经常会面临单靶or双靶的选择,这里强烈建议淋巴结阳性的患者使用双靶向治疗,报销后的费用一般在10万以内。对于淋巴结没有转移,但具有高危因素,比如肿瘤较大,KI67较高等因素的患者来说,建议也使用双靶进行治疗。对于淋巴结转移的患者来说,使用双靶能将6年无浸润性癌复发率从单靶的83.4%提升到87.9%,绝对获益明显。
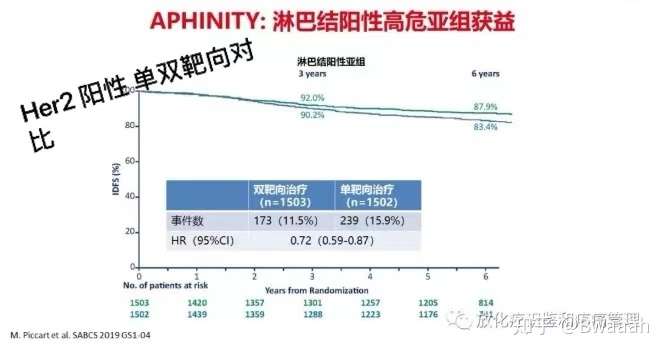
目前,抗HER2药物有曲帕双靶,T-DM1,拉帕替尼,吡咯替尼,来那替尼,以及尚未上市的DS8201、ONT-380等。这里对除赫塞汀外的其他药物做一个简单介绍。
帕托珠单抗:帕跟曲一样是生物大分子药,在中国仓鼠卵巢细胞中产生的,作用于HER2胞外区,曲妥珠和帕妥珠的作用方式是互补的。
T-DM1:赫塞莱是一种抗体-药物偶联物,将赫塞汀与化疗药物DM1偶联,通过赫塞汀的精准制导,将DM1释放于HER2阳性的肿瘤细胞上,相较于传统化疗更为精准,且具有抗HER2以及细胞毒双重功效。此药很牛批,但是价格较贵,希望早日纳入医保造福广大患者。
来那替尼:来那替尼是作用于EGFR、HER2和HER4的小分子TKI药物。小分子和大分子是分子质量和结构不同,对于脑转移患者来说,曲妥珠这种大分子药物很难透过血脑屏障,TKI的意思是酪氨酸激酶抑制剂。来那替尼目前可用于T2以上、淋巴结阳性4枚以上的高危患者标准化疗和靶向之后的强化治疗,此药对激素受体阳性的患者疗效较好,价格较贵。
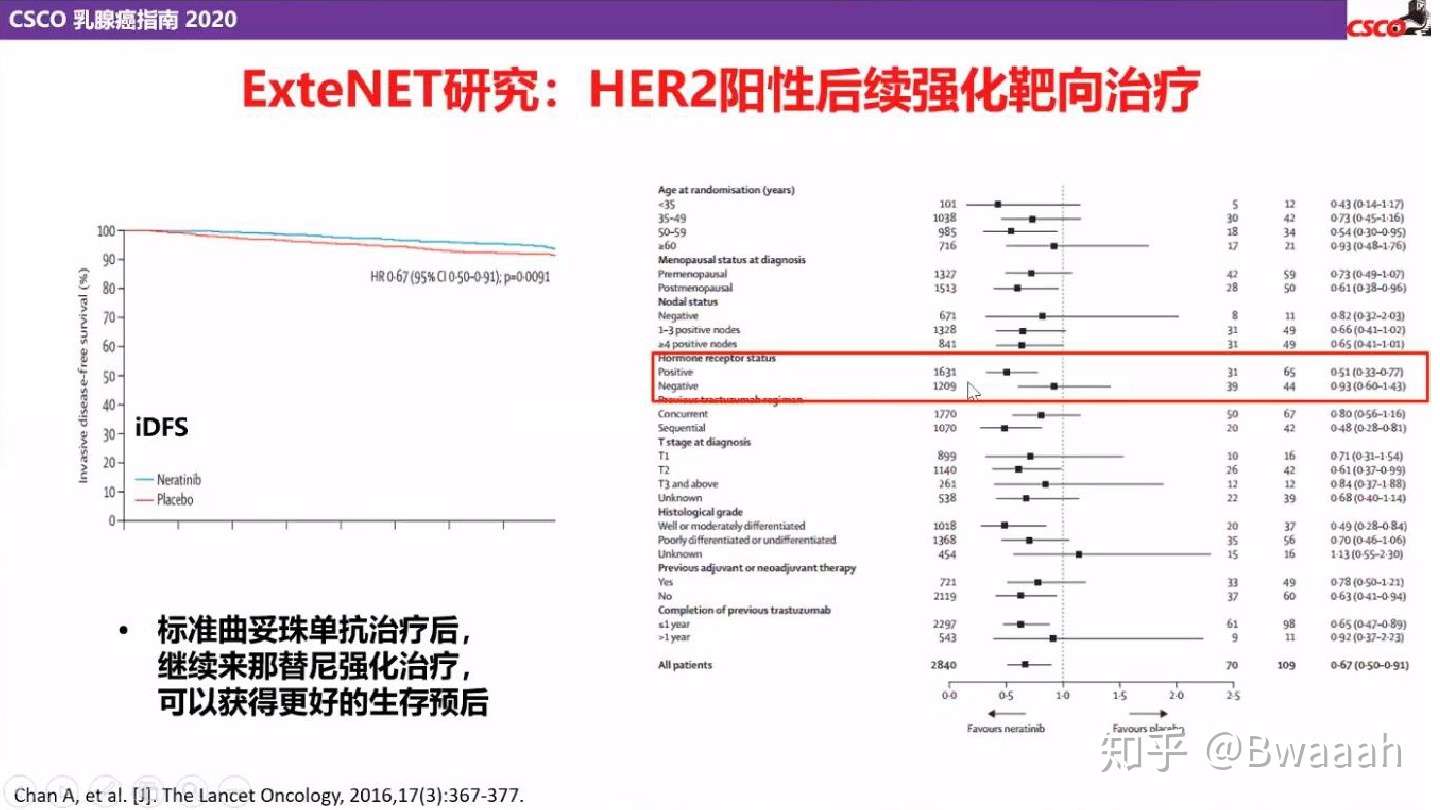
吡咯替尼:吡咯替尼是我国自主研发,作用于EGFR、HER2和HER4的口服TKI药物。吡咯替尼+卡陪他滨组相较拉帕替尼+卡陪他滨组,和单用卡陪他滨组,疗效明显更佳,与卡陪他滨联合治疗复发或转移乳腺癌。
拉帕替尼:拉帕替尼也是小分子TKI口服药物,目前联合卡陪他滨治疗复发或转移性乳腺癌。
DS8201:此药跟T-DM1类似,目前研究显示疗效很牛批,未来可期。
ONT-380:小分子TKI药物,目前研究表明此药对脑转移疗效较好。
靶向治疗就写到这里,写着写着发现篇幅过长了。之后尽量精简吧。
关于放疗
放疗是通过放射线杀死可能存在的癌细胞,是一种局部治疗手段,可以降低局部复发的风险。放疗时间的选择,未化疗患者应该在术后8周内开始,接受化疗的患者应该在末次化疗后2-4周内开始,需内分泌治疗的患者,放疗与内分泌治疗可同时进行。保乳患者原则上必须放疗。全切患者,淋巴结1-3枚阳性者,但有肿块较大、淋巴管癌栓等因素,也推荐放疗,但此种情况下,如果有BRCA胚系突变的患者,谨慎选择全乳放疗。淋巴结大于3枚患者原则上必须放疗。
放疗每周5次,大概需要25次左右,费用是报销前5万上下,大分割放疗的时间和费用较少。根据目前的实验数据,大分割方案与常规方案疗效相似,副作用稍轻。放疗对皮肤的损失大概像晒伤,可以涂抹三乙醇胺乳膏(比亚芬)。其他没什么可说的,技术活,交给医生就行了。
今天闲来无事来更新了,把最近有些群友遇到的问题在这里写一下:
1、有一部分患者的原发灶和转移至免疫组化不一样,所有转移灶都应尽可能的做穿刺活检明确肿瘤的ER、PR以及HER2状态,指导治疗手段。如果转移灶免疫组化改变,而没有被检测出来,这种影响可能是致命的。
2、HER2的免疫组化检测存在假阴性和假阳性,有时候需要结合病情和不同分型的病理特点判断。如肿瘤非常大、生长迅速的情况下,考虑对HER2阴性患者重新检测。
3、有研究发现,CYP2D6与他莫昔芬耐药有关,弱代谢型复发时间显著缩短。然而,又有研究证明,CYP2D6基因型与临床结果无关。基于目前证据的矛盾性,NCCN指南与ASCO指南均不推荐进行CYP2D6检测,以判断使用他莫昔芬还是托瑞米芬。使用他莫昔芬时,避免服用帕罗西汀、氟西汀等药物。目前,国内邵志敏教授牵头,正在做CYP2D6弱代谢型中他莫昔芬和托瑞米芬的疗效对比的临床试验,期待结果。如实在纠结,CYP2D6弱代谢型患者可选择托瑞米芬。
4、HER2的过表达和扩增是不一样的概念,HER2基因的扩增会导致HER2蛋白的过表达,但是过表达不一定都是扩增导致,还有可能是其他原因,比如17号染色体多倍体(可能是2+或3+,FISH检测无扩增的原因),类似的概念还有HER2的突变。三阴患者雄激素受体型HER2突变率高,使用吡咯替尼+卡陪他滨有很好的疗效。
5、推荐所有晚期患者进行致病性基因检测。
6、帕博西利(爱博新)目前没有进入医保,价格较贵,可考虑孟加拉版本。此药需与餐同服,暴露量最高,药效最好,避免和质子泵抑制剂一起使用。
7、HR+晚期可能用到的常见药物有 mTOR抑制剂:依维莫司;CDK4/6抑制剂:帕博西利、阿贝西利;HDAC抑制剂:西达本胺;PI3K抑制剂:阿培利司;VEGF抑制剂:贝伐珠单抗、阿帕替尼;以及未来可期的AKT抑制剂、PARP抑制剂、FGFR抑制剂、AR抑制剂等。HR+晚期乳腺癌一般生存期较长,已逐渐成为慢性疾病。
8、针对HER2低表达患者,即1+和2+ FISH-患者,DS8201显示出良好的疗效。
9、非晚期HR+乳腺癌患者普遍预后较好,能不能进一步提升治愈率呢?对于2阳1阴,淋巴结转移4枚以上的高危患者,标准内分泌治疗联合阿贝西利可进一步降低复发率。
10、三阴性乳腺癌患者,可在标准化疗后,使用卡陪他滨节拍化疗一年,进一步降低复发率。
好久没更新了,今天闲来无事,聊聊最近被问到的几个药:
11、关于GP2乳腺癌疫苗。GP2是一种免疫治疗,2期结果是在12月份在圣安东尼奥乳腺癌大会上发布的,实验组入组46例HER2阳性患者,经过标准化疗和曲妥珠单抗治疗后,使用GP2+GM-CSF,五年无一例复发,而对照组入组50名患者,在手术后经过化疗和曲妥珠单抗治疗后,仅接受GM-CSF治疗,五年复发率为89.4%。2期试验是不可能大量入组的,但是现在说GP2治愈HER2阳性乳腺癌,我觉得目前这个情况差的还是有点远。而且此药是在标准治疗的基础上,再进行免疫治疗,所以该做的手术、化疗、靶向治疗一个都少不了。目前试验2期才刚刚结束,咱国家十年内能用上药就不错了,未来肯定是免疫治疗的天下,希望此药能有更让人信服的数据出来,早日应用于临床,造福广大患者,也希望更多针对HR阳性和三阴性的免疫治疗能有所突破。
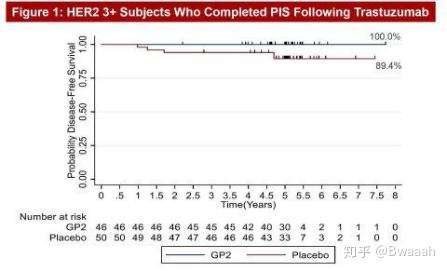
12、三阴性乳腺癌的第一款ADC靶向药物Sacituzumab govitecan 上市了,名字太长了,商品名叫Trodelvy,也有人称为IMMU-132,这个其实是试验的名字。这个药跟T-DM1是同类药,就是找到癌细胞的精准靶点,打靶的同时再释放化疗药,这个靶点是TROP-2。这药目前适应症是晚期三阴,国内也买不到,有条件的可以找找资源。
13、内分泌药的服用,建议每天固定时间,以维持稳定的血药浓度。
最近一段时间比较忙,今天抽空更新一下文章,注点新鲜血液。
14、最近有很多人很纠结自己是Luminal A型还是B型,其实,分子分型是基于55基因表达的检测方法,只不过这种方法难以在临床推广,就用了免疫组化的ER PR KI67 和HER2替代方法,这种替代方法与分子分型的本质还是存在一定的差异,大概也只有70%多的准确率。回到Luminal A 和B的问题上,如果你ER PR 高表达,KI67低表达,那也只是倾向于Luminal A型,更有可能是Luminal A型,如果你ER PR 低表达,KI67高表达,也只是倾向于Luminal B型,同样的,如果你的免疫组化是三阴性,那你也只是有80%的可能是真正的Basal-like型,如果你免疫组化是HER2阳性,也不排除有小概率是其他的基因表型。
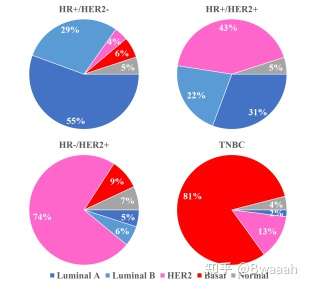
在Luminal 型中,Luminal A型占了绝大多数,B型是比较少的,我建议大家不妨都把自己当成A型来看待,增强自己的信心,因为A型的预后要明显好于B型。有的患者KI67 15%,根据网上N年前的分型版本(KI67<14),严格的把自己划为了Luminal B型......其实这都是些无谓的做法,徒增烦恼而已。
15、昨天群里谈到内分泌吃5年还是10年的问题。我查询了一下最新的NCCN指南和CSCO指南,大致意见是,除非极低危,比如肿瘤高分化、微浸润等,一般建议都是10年。这是基于大量实验数据,10年内分泌治疗较5年能显著降低复发率和死亡率。如果做过化疗,有化疗指征的,一般都不是极低危,都要做够10年。
16、市面上多种预测复发风险的基因检测,只有21基因检测,即Oncotype Dx,通过了临床验证,适应于临床复发风险较低的2阳1阴,淋巴结阴性的患者,以确定是否需要化疗。这个基因检测仅适用于预测辅助化疗收益,而且只能是2阳1阴的低危患者才能做。若临床高危,T+G>=4,即肿瘤大小+组织学分级>=4,推荐进行辅助化疗。
17、有很多人分不清基因突变中的体系和胚系。我们乳腺癌的致病性基因检测分为体细胞检测和外周血检测(胚系)。人是从受精卵发育而来的,如果受精卵的基因出问题,那么长大后体内的每一个细胞都会有问题,受精卵出问题的就是遗传性的致病突变,你爸妈遗传给你的,当然了,受精卵也有可能自己突变,只不过概率非常小,绝大多数胚系突变都是遗传的。我们查体细胞基因突变就是查肿瘤病灶,看看这个肿瘤是什么基因突变引起的。所以,如果要查胚系突变,就直接抽血,如果要做致病性基因检测,那就直接拿切下来的癌灶进行检测,这两者的目的是不同的。胚系突变更多的意义是在于进行预防性的干预,比如切除卵巢,和手术指导,比如选择全切手术,而体细胞的突变更多是对用药进行指导,一般在晚期的时候考虑。早期如果要查遗传性的话,直接进行外周血检测就可以了。
18、辅助化疗在术后肯定是越早做越好,原则上不超过1个月。1个月以内都是OK的,超过1个月对治愈率有点影响,超过3个月有重大影响。
19、化疗期间会引起肿瘤标志物的升高,只要不超过正常指标好几倍都问题不大。如果肿瘤标志物超过的很多,或者持续升高,CA153,CEA,CA125这些,可能需要做PETCT。
有段时间没来更新。今天闲下来写点最近遇到的:
20、初始治疗选择甾体类AI(依西美坦)和非甾体类AI(来曲唑和阿那曲唑)都可以,副作用不一样。如果在治疗过程中复发后一般不再选择AI类药物,因为甾体和非甾体存在比较多的交叉耐药。
21、最近看到一篇文章说早期2阳1阴可在内分泌治疗的基础上,口服S-1化疗,能显著降低复发风险。这些文章都是标题党。这个研究是日本做的,POTENT研究。S-1是一种口服的氟尿嘧啶衍生物,对于增殖期,尤其是S期细胞作用更好,而内分泌治疗则是抑制癌细胞的生长。POTENT研究对临床的指导意义不大,后续期待更多的此类临床研究和数据,而目前,几乎所有的指南和专家组都不推荐内分泌联合S-1口服化疗药。
22、有些患者对化疗脱发很在意,目前化疗药方案里面,脂质体阿霉素,也就是多柔比星脂质体,和吡柔比星的脱发率比较低。
23、最近有不少人问到中医治疗。中医的定位一定要是术后辅助作用,如果单纯靠中医治疗癌症,那无异于自杀。中医治疗应在放化疗及靶向治疗结束后,治疗期间,尤其是化疗期间,服用中药会加重肝脏负担,造成肝功能异常和损伤。一定要去正规三甲医院,最好是肿瘤医院的中医科,带上病理和目前的治疗方案,找中医进行把脉,一人一方。凡是带有“祖传”、“秘方”、“专利”等字眼的一概绕行。
24、虽然常规复查项目中一般都有肿瘤标志物,但是不推荐早期乳腺癌患者使用任何肿瘤标志物检测疾病复发。
25、生育问题,规范的治疗后进行生育不会增加复发率或死亡率,孕育出的后代也不会有出生缺陷或者其他疾病,但是可能会影响生育能力。所以在治疗前可以进行冰冻胚胎或者卵细胞,或者在化疗期间打卵巢抑制针保护卵巢。要注意的是,打针也是提高妊娠的概率,对生育能力的保护不是绝对性的。
26、复发转移的患者,首次复发时应尽量穿刺活检明确ER、PR以及HER2的状态。大量的报告显示出这种不一致性,ER阴性变阳性的不一致率范围在3.4%到60%之间,ER阳性变阴性的不一致率范围在7.2%到31%之间,HER2的不一致率在0.7%至11%。这种变化的原因可能是肿瘤的异质性、生物学特性的变化、检测的准确性有关。
27、乳腺分叶状肿瘤属于肉瘤,以手术为主要手段,切缘应大于1cm,较少转移淋巴结,通常多见肺转移,化疗对其无明显作用。
28、炎性乳腺癌是一种临床三期的乳腺癌类型,诊断要求乳房三分之一以上的皮肤出现橘皮症,其原因是肿瘤栓堵塞了真皮淋巴管。该类型乳腺癌常为2阴1阳,预后较差。
29、有些朋友是微乳头状癌,在看了我的文章后很恐慌,因为我写了微乳头状癌预后较差。微乳头状癌预后差是因为容易淋巴结转移,发现的时候一般都转移淋巴结较多,分期偏晚。如果你能较早发现,那预后还是较好的,这个病理类型差是差在你发现的时候一般就不是早期了。
30、导管内癌,导管原位癌理论上不会发生转移,完整切除后可以100%治愈。但是有些原位癌可能存在浸润部分,只是因为取材、切片有限而误诊为原位癌。小叶原位癌要注意多发和对侧乳腺发生的问题,据统计,有60%以上的小叶原位癌有这些问题。
31、最近被问到最多的就是饮食问题,乳腺癌患者其实忌口问题很简单,主要是烟酒、腌制、发霉、高糖高油脂、保健品这些食物,这些食物正常人也应该少吃。激素受体阳性的乳腺癌应该忌口蜂王浆、紫河车、雪蛤这些东西。其他没什么忌口的,像牛奶豆浆,牛肉鸡肉,鱼虾蟹这些都可以吃,而且提倡吃。乳腺癌病人提倡的是营养要均衡,你不能每顿饭都吃鸡肉吧,也不能每顿饭都吃青菜吧,除了上述一些确实有害的,其他种类的都可以吃喝,包括辣椒、包括大蒜、包括咖啡、包括茶。油炸的是不是一定就不能吃了呢?不是的,这些是少吃,而不是需要完全忌口,一个月吃一条炸鸡腿,吃一顿火锅解解馋还是不错的。平时饮食要多样化,搭配均衡,维生素、脂肪、膳食纤维、碳水化合物这些人体七大营养素一个都不能少,补充好蛋白质,每天两颗鸡蛋。不要吃蛋白粉这些东西,某子粉,某斛什么的,如果别人送了你,你就转送给其他人,还能落个人情,送不出去那就自己喝了也行吧,反正也没什么用,可千万不要自己花钱交智商税。乳腺癌病人手术放化疗后就进入正常生活,正常饮食,莫把自己当病人,非要补点什么。
32、最近ESMO上DS8201大放异彩,大幅度秒杀了t-dm1,降低疾病复发死亡风险70%+,HER2阳性的晚期患者真是有福了。这个药真是里程碑式的,以后晚期二线治疗要首选DS8201了,不仅晚期二线,甚至可能是晚期一线、甚至是早期辅助治疗。期待一下DS8201在早期辅助治疗与曲帕双靶的头对头研究比较,如果同样秒杀了曲帕(预期是阳性结果),那HER2阳性的治愈率很可能高于luminal型患者,成为预后最好的乳腺癌类型,那以后HER2阳性可是一种幸福了。美中不足的是这个药目前国内不可及,从国外买一个月的治疗费用差不多也要7万左右,希望早日在国内上市并纳入医保,造福广大病友。同时,一些HER2阳性的患者可以留意一下此药的实验组。
术后生活状态很重要,最近发现有些病友治疗结束后躺床上刷抖音到半夜的,坐一整天打麻将的,抽烟喝酒的,这种复发了也怪不得别人。网上确实有很多复发的案例,那些人真正过好生活的又有几个?我简单打个比方,100个人做完所有治疗以后,体内有残留癌细胞的还有40个人。那另外60个确确实实没有癌细胞的,再怎么作践自己也不会复发,顶多再新得一次癌。而这有癌的40个人,你一天不运动、不均衡饮食、不按时按量服用内分泌药,复发转移几乎是必然结果,你要愿意赌这概率你就去赌。心态+饮食+运动+睡眠,这四样做好了,再复发那确实是命不好,你都做不好这些,有什么资格埋怨自己的命运。有些病友一有风吹草动,甚至脸上长个痘痘都要给我拍照片看看是不是肿瘤复发的,这种心态确实影响治愈率。
33、关于脉管癌栓的问题,有些朋友在网上查了很多资料,说是脉管癌栓就意味着肿瘤进入了血管,会造成转移。这句话有没有道理,也有一定的道理,但多少有点儿危言耸听。目前的共识是浸润癌在1-2mm的时候就会进入血管,不管有没有癌栓或者血管侵犯,肿瘤可以自己生成血管。也就是说你只要是浸润性乳腺癌,那基本上血管里多少已经会有肿瘤细胞进入过了。我们为什么术后要做化疗,内分泌治疗,靶向治疗,不就是要杀死这些循环肿瘤细胞和微转移灶吗?如果脉管有癌栓或者脉管有侵犯就等于癌细胞进入血液,没有侵犯就等于没有进入血液,那化不化疗,做不做内分泌治疗不就看看有没有癌栓就行了?进入血液的癌细胞也是只有极少部分会存活下来,存活下来也不一定就一定会导致转移,癌症转移是一件非常困难的事情,它不是你开着车上了高速公路就直达目的地那么简单。所以有癌栓的不用怕,它是危险因素,但是不代表就一定会转移,没有癌栓的也别掉以轻心,该做全身治疗的还是得做,该坚持吃内分泌药还是要坚持。我三番五次重复,内分泌药一定要按时按量吃5-10年,病情严重的甚至要吃终身,这个非常非常重要。
34、有朋友问到化生癌为何预后差,这里简单介绍一下。乳腺化生性癌属于一组异质性比较强的疾病,有低级别腺鳞癌、鳞状细胞癌、梭形细胞癌、混合化生性癌等等很多种类,不能笼统的说化生癌预后差,比如低级别腺鳞癌,大家从低级别这三个字就可以看出它的预后较好。但是大部分的化生性癌预后较差,如癌肉瘤、低分化鳞状细胞癌这些。化生性癌在临床上常表现为:肿瘤较大、组织学分级较高(分化较差)、HR与HER2表达率低(三阴)、淋巴结转移率低、化疗反应差等。故大部分化生性癌具有高度恶性的生物学行为,治疗方案及治疗敏感性、治疗靶点等均为有限,较其他类型的浸润性乳腺癌虽然淋巴结转移率低,但更容易远处转移,所以预后相对来说较差。
35、对于激素受体阴性患者而言,如果存在复发时间间隔比较长(>5年),复发后肿瘤进展缓慢等情况,应尝试使用内分泌治疗。
36、血常规对晚期乳腺癌预后有一定的指导意义:
ALC>1.5*10^9/L的患者比起ALC较低的患者,总生存期更长;
NLR<3的患者比起NLR较高的患者,总生存期更长;
PLR较低的患者,疾病进展较慢;
LMR较高的患者,总生存期更长。
其中,ALC为淋巴细胞绝对数;NLR为中性粒细胞/淋巴细胞比值;PLR为血小板/淋巴细胞比值;LMR为淋巴细胞/单核细胞比值。
37、有研究显示,染发剂累积剂量与乳腺癌发病相关,尤其是与HR阴性乳腺癌相关,染发剂中含有有毒芳香类化学物质更会对身体健康造成伤害,不推荐乳腺癌患者烫发、染发。
收藏
回复(21)参与评论
评论列表
 精明的可乐
精明的可乐 魁梧的香菇2963
魁梧的香菇2963 自觉的饭卡
自觉的饭卡 搞怪的跑步鞋9085
搞怪的跑步鞋9085 景色怡人1
景色怡人1 自觉的风衣5457
自觉的风衣5457