招募!PD-L1单抗联合靶向药物治疗晚期肝癌患者
BLU-554是一款强效高选择性的口服FGFR4抑制剂,由基石药业的合作伙伴Blueprint Medicines 开发。可以以极高的特异性抑制FGFR4,从而避免了对FGFR1,FGFR2和FGFR3的作用。
CS1001是基石药业自主研发的PD-L1单抗, 是一种最接近人体的天然G型免疫球蛋白4(IgG4)单抗药物。与同类药物(PD-L1单抗)相比,CS1001在患者体内产生免疫原性及相关毒性的风险更低。
联合化疗,指在一个化疗疗程中同时或者先后出使用数种化疗药物。联合使用不同作用机制的化疗药物,能在杀灭肿瘤细胞方面产生增效作用,从而提高疗效,还可以去除耐药因素,从而减少了癌细胞产生耐药的可能性。。通过使用数种药物,避免了单独使用一种药物剂量过大、时间过长所导致的该药物毒副作用明显增加的情况。
此次试验为临床Ⅰb/Ⅱ期试验,将会评估BLU-554(靶向药物)联合CS1001(PD-L1)治疗肝细胞癌患者的安全性和有效性。
一、试验主题
一项BLU-554联合CS1001在肝细胞癌患者中的单臂、非随机化、开放、国内研究。
二、适应症
晚期或转移性肝癌患者
三、试验目的
研究BLU-554联合CS1001治疗肝细胞癌患者的安全性和有效性。
四、试验设计
试验分类 | 安全性和有效性 |
试验分期 | Ⅰb/Ⅱ期 |
设计类型 | 单臂试验 |
随机化 | 非随机化 |
盲法 | 开放 |
试验范围 | 国内试验 |
招募人数 | 25人 |
五、入选标准
1.自愿参加临床研究;完全了解、知情本研究并签署知情同意书。
2.受试者在签署ICF当天年龄≥18岁。
3.经病理组织学或细胞学证实的,不可切除的局部晚期或转移性肝细胞癌。
4.巴塞罗那临床肝癌分期系统[BCLC]分级为B或C,如果是B级,受试者必须是不适合手术和/或局部治疗,或手术和/或局部治疗后出现了疾病进展,或受试者拒绝手术和/或局部治疗。
5.Ib期,受试者接受目前针对HCC的标准系统治疗失败或不适合标准治疗。II期,受试者从未接受过系统治疗。
6.根据RECIST v1.1,受试者至少具有存在一个可测量病灶。
7.受试者的美国东部肿瘤协作组(ECOG)体能状态(PS)评分为0-1。
8.肝功能Child-Pugh评分为A级。
9.预期生存期≥3个月。
六、排除标准
1.影像学显示门静脉主干癌栓(VP4)、下腔静脉或心脏受累。
2. 既往肝性脑病病史。
3. 首次给药前4周内,曾接受过肝脏手术和/或针对HCC的局部治疗(介入、消融治疗、无水酒精注射等)或放疗等。
4. 活动性或6个月内有记录的消化道出血(如食管或胃静脉曲张、溃疡出血)。
5. 筛选期存在体格检查中可检测到的腹水,或由腹水引起的临床症状,或需要特殊处理,如反复引流、腹腔内药物灌注等。
您是否能够成功参加本研究,还需要满足其他条件,这将由研究团队与您共同讨论。
试验详情见觅健APP首页“免费用药“栏目,参加流程如下:
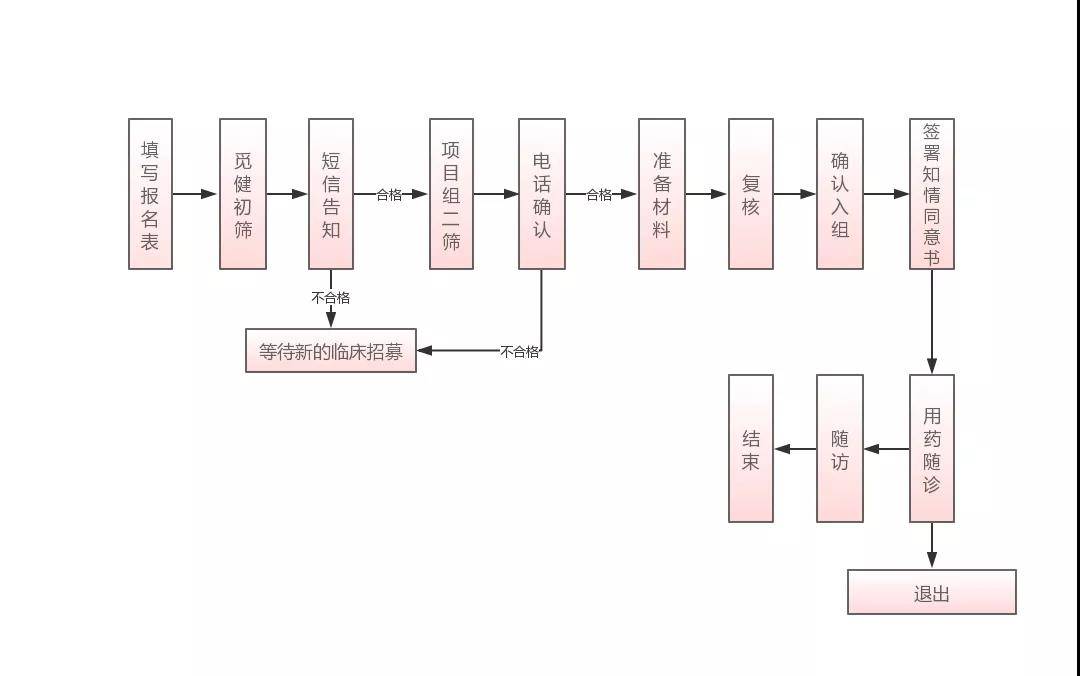
参加流程
1、报名方式(两种报名方式)
点击文末下方的“申请报名”,再点击“申请入组”填写相关信息即可申请。
2、初选
觅健工作人员对患者进行初筛,并上报项目组。
3、二次筛选
项目组二次筛查通过后可以参加临床试验项目,进行药物试验。
注意事项:报名期间,请保持电话畅通、微信可添加、陌生电话不要拒接或屏蔽,工作人员将会以此方式联系您。
互助君温馨提示:
如果有什么问题,可以在帖子下方留言,互助君会尽力给与答复
收藏
回复(0)参与评论
评论列表
























