首个三阴性乳腺癌ADC药物重磅获批!
疾病控制率高达74.1%!首个三阴性乳腺癌ADC药物重磅获批!

前沿资讯
2020年4月22日,Immunomedics公司宣布FDA加速批准其抗体偶联药物Trodelvy(sacituzumab govitecan-hziy)上市,用于治疗既往接受过至少2种疗法的转移性三阴乳腺癌成人患者。
Trodelvy(sacituzumab govitecan-hziy)是第一个获批的靶向Trop-2(人滋养层细胞表面抗原2)的抗体偶联药,曾获得FDA授予的突破性疗法和快速通稿资格。
Trop-2在乳腺癌、宫颈癌、结直肠癌、肾癌、肝癌、肺癌、胰腺癌、前列腺癌等多种肿瘤细胞表面大量表达,三阴乳腺癌患者的Trop-2表达率高达90%,但是Trop-2在正常组织中表达有限。
因此,Trodelvy可以通过特异性靶向Trop-2单抗Sacituzumab将临床常用化疗药物伊立替康的活性代谢产物 govitecan(SN-38) 靶向运送到实体瘤病灶,发挥化学毒性杀伤作用。
说到抗体药物偶联物(ADC),我们最熟悉的莫过于恩美曲妥珠单抗(TDM-1),作为全球首个获批的单药治疗实体瘤的ADC药物,目前也已在中国上市。
ADC 是将单克隆抗体药物的高特异性和小分子细胞毒药物的高活性相结合,用以提高肿瘤药物的靶向性、减少毒副作用。
和传统的完全或部分人源化抗体或抗体片段相比,ADC因为能在肿瘤组织内释放高活性的细胞毒素,理论上疗效更高。和融合蛋白相比,ADC具有更高的耐受性或较低的副作用。
ADC药物对靶点的准确识别性及非癌细胞不受影响性,极大地提高了药效并减少了毒副作用,因而备受关注。
该批准是基于一项III期验证性研究ASCENT,旨在验证II期研究Trodelvy在治疗既往至少接受过2种标准化疗进展复发的晚期三阴乳癌患者中观察到的安全性和疗效。
本研究以1:1的比例随机分配到Trodelvy组 或 其他标准化疗组(艾日布林/吉西他滨/卡培他滨/长春瑞滨)。
ASCENT研究的主要终点是无进展生存期(PFS),次要终点包括总生存期(OS)和客观缓解率(ORR)等。
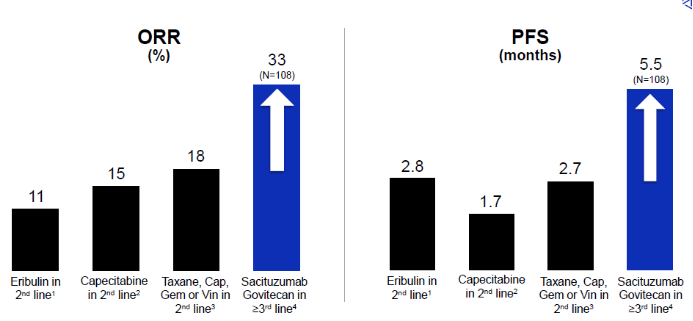
研究结果显示,在 108例入组患者中,接受Trodelvy治疗的患者组客观缓解率高达33.3%,其中包含2.8%的完全缓解率和30.6%的部分缓解率。远高于传统的化疗组疗效。
疾病控制率高达74.1%,其中37%的患者疾病稳定。到数据截至时,有6例患者临床疗效持续了12个月以上,最长的达到了30.7个月。
中位PFS是5.5个月,中位OS为13个月。
对于难治性三阴乳腺癌患者来说,这样的疗效堪称惊艳。
Trodelvy药物标签中附有一则黑框警告,提示严重的中性粒细胞减少和严重的腹泻。
发生在 25%或以上 患者中的最常见不良反应,包括恶心、中性粒细胞减少、腹泻、疲劳、贫血、呕吐、脱发、便秘、食欲减退、皮疹和腹痛。
发生在 超过5% 患者中的最常见3级或4级不良事件是中性粒细胞减少、白细胞减少、贫血、低磷血症、腹泻、疲劳、恶心和呕吐。
2% 的患者因不良事件而停止治疗。
没有与治疗相关的死亡病例,也没有神经病变或间质性肺病的严重病例。

收藏
回复(13)参与评论
评论列表
 绣球 1512
绣球 1512























