胃癌腹膜转移防治中国专家共识
胃癌是严重威胁人类健康的一种恶性疾病,全球胃癌每年新增95万例,死亡72万例,其中70%来自亚洲,而中国患者就占了将近一半。腹膜转移复发是晚期胃癌患者死亡的首要原因之一;所谓腹膜转移,是指胃癌原发灶癌细胞经血行、淋巴或腹膜直接种植生长所致的癌症转移形式。将近20%的胃癌患者在术前或术中诊断有腹膜转移,超过50%的T3、T4期患者在根治性切除术后发生腹膜转移,腹膜转移程度越高,生存期越短。
目前,我国胃癌腹膜转移诊疗现状严峻,发病率高、早期诊断困难、患者预后差。为了规范胃癌腹膜转移的诊断和治疗,加强对高危患者的筛查,及早发现腹膜转移,制定合理有效的多学科综合治疗方案,从而延长胃癌腹膜转移患者生存时间并改善生活质量。中国抗癌协会胃癌专业委员会组织国内胃癌领域权威专家制定《胃癌腹膜转移防治中国专家共识》(以下简称为共识)。
本共识适用于具有腹膜转移风险因素或确诊腹膜转移的胃癌患者。
注1.中国抗癌协会胃癌专业委员会组建共识制定专家组。首先由工作小组检索Medline、Embase、Cochrane和万方中文期刊数据库,制订共识意见的草案,随后由专家组采用国际通用的德尔菲法(Delphi method)进行讨论和修订,直至达成共识。
注2.证据等级:Ⅰ级:进一步研究几乎不可能改变对临床疗效评估结果的可信度,为高级别证据;Ⅱ级:进一步研究有可能对疗效评估结果的可信度有重要影响,且有可能改变评估结果,为中级别证据;Ⅲ级:进一步研究很有可能对疗效评估结果的可信度有重要影响,且极有可能改变评估结果,为低级别证据;Ⅳ级:任何疗效评估结果都不确定,为极低级别证据。
注3.推荐级别:Grade A:基于可得证据,非常确定获益大于风险和负担,则做出强推荐;Grade B:基于可得的证据,认为获益、风险和负担相当平衡,或获益、风险的程度存在明显的不确定,则做出弱推荐。
一、胃癌腹膜转移的发生机制
胃癌腹膜转移的发生机制尚不完全明确,"种子土壤"学说是目前认可度较高的发生机制理论。腹膜转移的发生取决于癌细胞(种子)和腹膜(土壤)的微环境。癌细胞分泌的转化生长因子β1(transforming growth factor beta 1,TGF-β1)参与细胞外基质(extracellular matrix,ECM)的生成与成熟,而ECM可为β1-整联蛋白和CD44H提供配合基,最终促使游离癌细胞的浸润及黏附;腹膜自身特异性结构(淋巴孔和乳斑区)也使得癌细胞易于"播种" 。
腹膜乳斑是一种特殊的免疫结构,由巨噬细胞围绕血管网构成,因为缺乏连续的间皮细胞层,容易造成游离癌细胞的定植。此外,游离癌细胞聚集于连接乳斑区和腹膜下淋巴管的淋巴孔处,因淋巴孔特异性分布于横膈膜、肠系膜、网膜和盆腔腹膜的浆膜表面,故而这些部位在腹膜转移的早期就易受到累及。"种子土壤"学说发生机制的描述见图1。
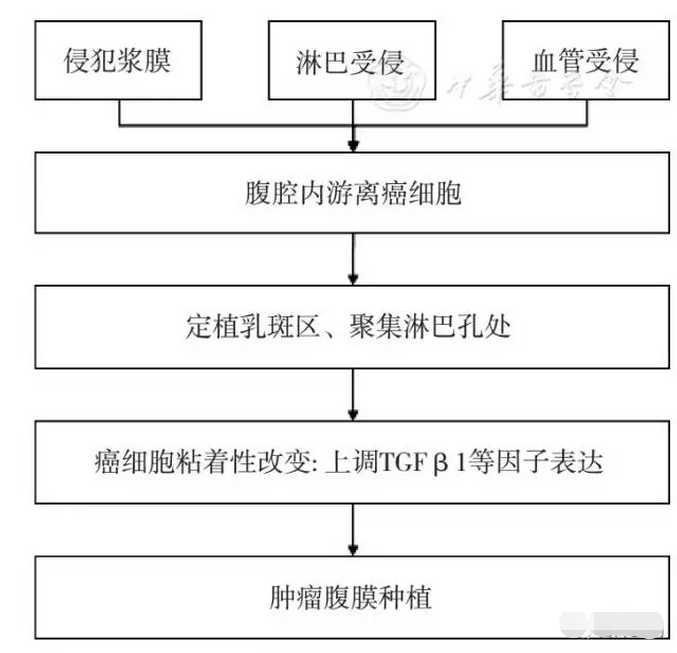
图1 胃癌腹膜转移的发生机制
二、胃癌腹膜转移的诊断与分期
1.影像诊断: 影像学诊断胃癌腹膜转移难度较大,通过典型征象确诊者多已属晚期,即便通过正电子发射型计算机断层显像(PET-CT)也难以在腹膜转移的早期阶段确诊,因而导致较高的假阴性率。推荐X线计算机断层摄影(CT)作为胃癌腹膜转移的主要影像学检查手段。CT诊断胃癌腹膜转移的敏感度为33%~51%,特异度为95%~99%,优于超声(US)和PET检查。 胃癌腹膜转移的典型CT征象包括:腹膜不均匀增厚、高强化或伴结节;网膜饼或大网膜多发索条、结节;肠系膜结节状增厚;腹盆腔大量积液。注意腹膜转移粘连侵犯导致的肾盂输尿管扩张、肝内外胆管扩张及肠梗阻等间接征象。注意少量腹水(尤其肝脾周围)对早期腹膜转移的提示意义,文献报道,胃癌患者影像学检出腹水超过50 ml,腹膜转移阳性率达75%~100%。 PACS工作站宽窗观察(脂肪间隙均质细颗粒状背景噪声清晰显示为准),避免遗漏小的转移灶;联合轴位、冠状位和矢状位三平面观察,提高对特殊部位转移灶的检出和定位能力;全面观察横结肠系膜、后腹膜、镰状韧带等胃周各韧带及系膜走行区域。 MRI可作为增强CT检查禁忌患者的备选手段,在低张和呼吸训练控制运动干扰的前提下可显示腹膜结构,并可应用扩散加权功能成像(DWI)辅助小转移灶的检出。 2.血清标志物检测: 癌胚抗原(CEA)、癌抗原125(CA125)、癌抗原19-9(CA19-9)、癌抗原724(CA724)是胃癌常用的肿瘤标志物。尽管这些血清学指标的升高与腹膜转移成正相关,但用于胃癌腹膜转移的诊断时,其敏感性及阳性预测值均较差。 因腹膜间皮细胞在受到肿瘤侵犯时可以释放CA125入血,所以,理论上CA125是检测腹膜转移的潜在指标;尽管CA125的阳性预测值显著高于其他标志物,但其敏感性也无法满足临床需求。因此,血清标志物检测仅可作为辅助诊断,不作为腹膜转移诊断的依据。 3.诊断性腹腔镜检查: 诊断性腹腔镜检查是有创检查,可以对腹腔内的转移情况进行评估,了解腹膜转移的分布和大小,并获得明确的组织学及细胞学证据,用于指导制定临床治疗策略,进而评估治疗疗效及监测疾病进展。 目前,腹腔镜检查主要适用于进展期胃癌(cT2~4及任何N和M)的治疗前诊断、术前治疗后的疗效评价。既往腹盆腔手术史明确、可疑严重腹腔粘连等无法接受腹腔镜手术、或心肺功能不能耐受麻醉及CO2气腹的患者,不能进行诊断性腹腔镜检查。 腹腔镜检查的手术操作规范: (1)患者体位:平卧或平卧分腿位; (2)建立气腹:气腹针穿刺或开放法,维持腹内压在10~15 mmHg; (3)放置套管:在脐下1 cm处作为观察孔,放置10或12 mm套管,右侧操作孔通常选择右侧腋前线与右肋弓交点下方2 cm处,放置5或10 mm套管;左侧操作孔通常选择左侧腋前线与左肋弓交点下方2 cm处,放置5或10 mm套管;可酌情增加右侧第二操作孔,通常选择右侧腋前线平脐水平,放置10 mm套管。套管间应保持5 cm以上的距离; (4)腹腔游离癌细胞检查:建立操作孔并充分止血后立即收集腹水或行腹腔灌洗(具体操作见二、(一)、4.); (5)腹腔探查:从右上腹开始,按顺时针方向进行,依次探查右侧膈肌和肝右叶、肝圆韧带、左侧膈肌和肝左叶、左侧壁腹膜及降结肠、盆腔和道格拉斯窝(女性注意探查双侧卵巢)、右侧壁腹膜及升结肠、大网膜、横结肠、结肠系膜、前腹壁、小肠及系膜。 最后探查原发病灶及胃周淋巴结情况,记录肿瘤位置、大小、是否浸润浆膜、有无周围脏器浸润。对于胃体后壁肿瘤,需要切开胃结肠韧带,探查网膜囊,包括横结肠系膜和胰腺被膜。对腹腔内可疑病灶均应行快速冰冻病理检查,同时记录病灶位置、大小、是否融合及腹膜肿瘤指数(peritoneal cancer index,PCI)等;探查过程中可根据需要调整患者体位,推荐留取图片或录像作为记录; (6)关闭切口:10 mm以上切口需直视下缝合。 4.腹腔游离癌细胞检查: 腹水或腹腔灌洗液细胞学检查是目前诊断腹腔内游离癌细胞的金标准。虽然其敏感性较低,但有助于发现肉眼无法识别的微转移。现有文献认为,腹腔内游离的癌细胞是形成腹膜转移的先决条件,是胃癌的独立预后不良因素。腹腔游离癌细胞阳性可作为Ⅳ期胃癌的独立诊断指标。诊断性腹腔镜检查应同时进行腹腔游离癌细胞检查。 腹腔游离癌细胞检查的操作规范如下: (1)腹水的收集:如有足够量(≥ 200 ml)腹水则直接取腹水进行细胞学检查,如无腹水或腹水< 200 ml者,则用> 250 ml温生理盐水依次冲洗双侧膈顶、肝下区、大网膜、双侧结肠旁沟和道格拉斯窝,避免直接冲洗原发病灶;于双侧膈下区、肝下区和道格拉斯窝收集>100 ml灌洗液,行细胞学检查。 (2)标本的制作:腹水或腹腔冲洗液2 000转离心10 min;离心后小心吸出上清液,取细胞沉淀直接涂片2张,95%乙醇固定至少5 min,采用苏木精-伊红或巴氏染色法染色。 (3)结果的记录:腹腔细胞学检测结果阴性者记录为CY0,阳性记录为CY1。 综上,上述各项检查手段各有优劣,影像学和血清学检查欠缺敏感性,腹腔镜和病理学检查虽可确诊,但亦有一定局限性,因此临床中需要综合患者的临床表现、病理分型、原发灶及转移淋巴结的分期、血清肿瘤标志物、影像学或功能影像等综合判定,必要时需要腹腔镜等有创检查手段进行明确。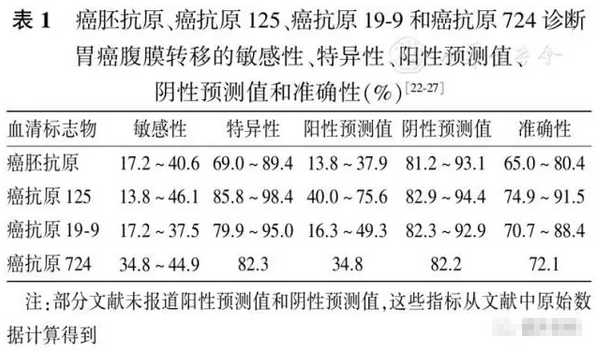
1.腹膜转移(P)(TNM分期为M1): PX:有无腹膜转移不明者;P0:无腹膜转移;P1:有腹膜转移。 注4.结合我国目前临床现状,推荐采用日本胃癌学会制定的《胃癌分期规约2010年3月第14版》中腹膜转移的分期标准,也可参考2017年第15版的分期标准。PX:有无腹膜转移不明者;P0:无腹膜转移;P1:有腹膜转移;P1a:局限性转移(至仅局限在胃、大网膜、小网膜、横结肠膜前叶、胰腺膜、脾脏等附近的腹膜);P1b:转移至上腹部(横结肠到脏侧的腹膜)P1c:转移至中下腹部;P1x:确定腹膜转移,但无法判断具体分布。 注5.休格贝克腹膜癌指数(PCI)是将腹膜瘤结节的分布和大小进行评分,而反应腹膜转移状况的一种分级方法。有研究显示,PCI指数与胃癌腹膜转移患者预后有一定的相关性。但考虑到操作难度较大,且目前尚无基于此分级的治疗推荐,因此未在共识中引用。 2.腹腔游离癌细胞(CY): CYX:未行腹腔灌洗液细胞学检查;CY0:腹腔灌洗液细胞学检查无癌细胞;CY1:腹腔灌洗液细胞学检查有癌细胞。 三、胃癌腹膜转移的预防 1.TNM分期T3、T4和N : T3、T4和N 患者腹膜转移发生率为25%,而T1、T2和N0患者仅为4%;另外,N 患者发生腹膜转移风险比N0患者高出3.84倍。 2.淋巴结外浸润: 与没有淋巴结外浸润的患者相比,有淋巴结外浸润患者的腹膜转移风险上升近18倍。 3.Borrmann分型Ⅲ、Ⅳ: 与BorrmannⅠ、Ⅱ型患者相比,BorrmannⅢ、Ⅳ型患者的腹膜转移风险高出2.06倍,是独立风险因素。 4.Lauren分型弥漫型: 弥漫型患者中腹膜转移发生率高达80%以上。 1.外科预防-无瘤技术: 可切除患者进行手术过程中应当严格按照无瘤规范进行操作,尽量避免因手术操作而导致癌细胞脱落种植于腹腔内,防止医源性扩散。无瘤操作规范的建议如下: (1)切口的保护:推荐常规使用切口保护套,特别注意切口上下端的保护; (2)手术时避免直接接触、挤压肿瘤,若肿瘤浸出浆膜层应用医用胶、纱布或手术薄膜覆盖; (3)术中及时更换污染的手套及器械:探查、分离肿瘤时,医生的手若触及破溃的肿瘤应及时更换手套,术中分离肿瘤的器械不可反复使用; (4)拭血纱布要及时更换,不可反复使用; (5)术毕用温热蒸馏水或生理盐水彻底冲洗术野及腹腔,冲洗液量应至少> 3 000 ml。 (6)关腹前充分冲洗切口。 2.术后辅助化疗: 术后通过系统性给药进行辅助化疗,可以杀灭手术无法清除的微小病灶,是降低术后复发和转移的有效手段。目前,临床常用口服氟尿嘧啶类药物[替吉奥(S-1)、卡培他滨(CAP)]单药或联合奥沙利铂(OXA)作为术后辅助化疗方案。 为预防术后腹膜转移,辅助化疗方案的选择应考虑药物的特点。传统氟尿嘧啶(5-FU)类药物分子量小容易穿透血腹屏障,适合用于术后辅助化疗,但因其迅速被二氢嘧啶脱氢(DPD)分解代谢而失去抗肿瘤活性。新型口服5-FU类药物S-1不仅可以穿透血腹屏障,而且含有吉美嘧啶(CDHP)能有效阻止5-FU分解,所以可维持有效的药物浓度。 推荐方案:S-1,80~120 mg/d,口服4周,停药2周,6周为一疗程;持续1年(Ⅱ级,Grade A)。紫杉醇(PTX)序贯S-1(Ⅲ级,Grade B)。S-1/顺铂(CDDP)序贯S-1,S-1/多西他赛(DOC)序贯S-1,DOC/CAP/CDDP(Ⅳ级,Grade B)。 循证证据 (1)Sasako等在三期随机对照研究ACTS-GC中纳入了1 059例Ⅱ~Ⅲ期胃癌患者,比较单纯手术和S-1术后辅助化疗持续1年的疗效。结果显示,S-1辅助化疗优于单纯手术(5年生存率分别为61.1%和71.7%,HR= 0.669,95%CI:0.540~0.828),S-1辅助化疗组较单纯手术组的术后腹膜转移风险显著降低了31%。 (2)Kanda等回顾性纳入了70对(140例)配对的Ⅱ~ Ⅲ期胃癌患者使用倾向性匹配分析(propensity score matching analysis),发现S-1辅助化疗组较单纯手术预后更佳(3年无复发率71%比53%,P= 0.035),且腹膜转移率明显降低(5.7%比18.6%,P= 0.017)。 (3)Tsuburaya等在三期随机对照研究SAMIT中纳入了1 495例T4a和T4b期的胃癌患者,比较PTX序贯复方替加氟(UFT)或S-1和单药UFT或S-1的疗效。PTX序贯S-1组(355例)较S-1组(364例)(S-1 80 mg·m2·d-1,d1~14,每3周1周期,持续48周)有生存获益的趋势(但差异无统计学意义)及较小的腹膜转移风险(17%比22%,P值不详)。因此,PTX序贯S-1辅助化疗不劣于单药S-1。 (4)Takahari等在一项二期研究中,对纳入的63例Ⅲ期胃癌患者使用S-1/CDDP序贯S-1辅助化疗(SP方案)共3周期:S-1 80 mg·m-2·d-1,d1~21,CDDP 60 mg/m2,d8,每5周1周期;序贯S-1 80 mg·m-2·d-1,d1~28,每6周1周期,至术后1年),3年无复发生存率为74.1%(95% CI:60.8~ 83.5),3年生存率为84.5%(95%CI:72.3~91.6),腹膜转移率为12.7%(8/63)。 (5)Fujitani等在一项二期研究中,对纳入的53例Ⅲ期胃癌患者使用S-1/DOC序贯S-1辅助化疗(S-1 80 mg·m-2·d-1,d1~14,DOC 40 mg/m2,d1,每3周1周期,共4周期;S-1 80 mg·m-2·d-1,d1~28,每6周1周期,至术后1年),3年无复发生存率为66.2%(95% CI:54.4~80.7),3年生存率为78.4%(95%CI:67.9~90.6),腹膜转移率为7.5%(4/53)。 (6)Yoon等在一项二期研究中,对纳入的43例ⅢB~Ⅳ期(AJCC6,pT3N2,pT4N1-2M0,pTanyN3M0)胃癌患者使用6周期的DOC/CAP/CDDP(DOC 60 mg/m2,d1,CAP 1 875 mg·m-2·d-1,d1~14,CDDP 60 mg/m2,d1,每3周1周期),平均随访56.1月,3年和5年无复发生存率为48%和39%,3年和5年生存率为59%和41%,腹膜转移率为27.9%(12/43)。 3.预防性腹腔热灌注化疗: 腹腔内热灌注化疗(hyperthermic intraperitoneal chemotherapy,HIPEC)的优势是药物直接作用于癌细胞,影响腹膜微环境,抑制癌细胞种植。另一优点是不良反应小,对机体的免疫力影响小。但是,目前HIPEC作为预防性手段的临床证据不足,仍需进一步探索。本共识认为,具有风险因素的患者,可以考虑术中预防性应用HIPEC[参见四、(一)](Ⅲ级,Grade B)。 循证证据 (1)一项荟萃分析显示,术中HIPEC单独(HR= 0.60;95%CI:0.43~0.83;P= 0.002)或合并早期术后腹腔化疗(HR= 0.45;95%CI:0.29~0.68;P= 0.0002)显著改善胃癌患者生存。术中腹腔常温灌注化疗有改善生存的趋势(P= 0.06),但是单独早期术后腹腔化疗或延迟术后腹腔化疗均无显著效果[47]。 (2)Fujimoto等在一项术中HIPEC的随机对照研究中纳入了141例有浆膜浸润的胃癌手术患者,结果显示,HIPEC组[含丝裂霉素(MMC)10 g/ml的灌注液3 000~4 000 ml循环120 min]的患者较对照组腹膜复发率显著降低(P= 0.000 084 7),其2、4和8年生存率分别达到88%、76%和62%,而对照组则分别为77%、58%和49%(P= 0.0362)。 (3)朱正纲等的一项非随机对照研究显示,无腹膜转移的T3、T4期患者给予术中HIPEC(42例,CDDP 50 mg/L和MMC 5 mg/L,总灌注药量5 000~6 000 ml)优于单纯手术患者(54例),术后1、2、4年生存率HIPEC组分别为85.7%、81.0%和63.9%,单纯手术组分别为77.3%、61.0%和50.8%;HIPEC组的术后腹膜复发率10.3%,低于单纯手术组的34.7%。 四、胃癌腹膜转移的治疗 1.全身系统化疗: 全身系统化疗是晚期胃癌的一种有效治疗方式,优于最佳支持治疗。目前,临床常用的5-FU类联合铂类的两药方案,其疗效优于单药方案,毒性小于三药方案。腹膜转移是胃癌全身性疾病的局部表现,全身系统化疗是胃癌腹膜转移的标准治疗,也可根据患者一般状况、合并症、有无腹水、毒性反应等结合腹腔化疗等局部治疗手段。 推荐方案:S-1/CDDP(Ⅱ级,Grade A)、S-1/奥沙利铂(OXA)(Ⅱ级,Grade A)、PTX(Ⅲ级,Grade A)、S-1单药(Ⅲ级,Grade A)、5-FU持续静滴(Ⅲ级,Grade A) 循证证据 (1)Koizumiet等在三期随机对照研究SPIRITS中,共纳入305例晚期胃癌患者,比较SP方案(S-1/CDDP)和S-1单药方案一线治疗晚期胃癌患者的疗效和安全性。结果显示,SP组中位总生存时间(overall survival,OS)比单药组显著延长(13.0月比11.0月,P= 0.04);亚组分析显示,SP方案对腹膜转移患者的疗效更佳(HR= 0.52,95%CI:0.33~0.82,P= 0.02)。 (2)Yamada等在三期随机对照临床研究G-SOX中,共纳入685例晚期胃癌患者,比较SOX方案与SP方案一线治疗晚期胃癌患者的疗效和安全性。结果显示,SOX组的中位无进展生存时间(progression free survival,PFS)非劣于SP组(5.5月比5.4月,HR= 1.004,95%CI:0.840~1.199,P= 0.004 4),且SOX组毒性更低。亚组分析显示:SOX方案对腹膜转移患者的疗效更佳(HR= 0.646,95%CI:0.433~ 0.946,P= 0.032)。 (3)Shirao等在三期随机对照临床研究JCOG0106中,共纳入237例胃癌腹膜转移的患者,比较了5-FU单药静脉连续注射与5-FU联合甲氨蝶呤(MTX)的疗效和安全性。结果显示,联合方案并未延长患者生存期(中位OS:10.6月比9.4月,P= 0.31),反而增加了血液学毒性。 (4)Boku等在三期随机对照临床研究JCOG9912中,共纳入704例晚期胃癌患者,比较5-FU单药静脉连续注射、S-1单药方案以及伊立替康(CPT-11)/CDDP方案的疗效和安全性。结果显示,三组的中位OS分别为10.8月、11.4月。亚组分析显示:对于腹膜转移的胃癌患者,与单药5-FU相比,S-1(P= 0.83)或CPT-11/CDDP(P= 0.07)并无明确的生存获益;且CPT-11/CDDP方案出现的3/4级血液学毒性更加明显。 (5)目前大型的三期临床研究中,涉及到腹膜转移亚组分析的临床研究还有REGARD(二线雷莫卢单抗对比安慰剂)、RAINBOW(二线雷莫卢单抗/PTX对比雷莫卢单抗)、WJOG 4007(二线PTX对比CPT-11)和GC0301/TOP-002(一线S-1/CPT-11对比S-1),但上述研究中并没有发现某种治疗方案优于对照组。 (6)Nishina等在一项二期多中心随机对照临床试验(JCOG0407)中,纳入110例经一线5-FU方案(5-FU持续静滴或5-FU联合MTX)治疗失败的腹膜转移患者,随机分至二线PTX组(PTX 80 mg/m2,d1、d8和d15,每4周)或另一种5-FU方案组(即一线使用5-FU持续静滴者二线使用5-FU联合MTX,反之亦然)。PTX组和最佳5-FU的中位OS和中位PFS分别是7.7月比7.7月和3.7月比2.4月(HR= 0.58,95%CI:0.38~0.88)。 (7)Moehler等在一项二期多中心随机对照临床试验中,纳入了114例晚期胃癌患者,比较CPT-11/醛氢叶酸/5-FU(ILF方案)与足叶乙甙/醛氢叶酸/5-FU(ELF方案)一线治疗晚期胃癌患者的疗效和安全性。结果显示,ILF组和ELF组的PFS和OS分别为4.5月比2.3月(HR= 1.10,95% CI:0.75~1.62,P= 0.6116)和10.8月比8.3月(HR= 1.25,95% CI:0.83~1.86,P= 0.2818)。亚组分析显示,对于腹膜转移患者,ELF组比ILF组的死亡风险更高(HR= 2.41,95% CI:0.99~5.82)。 综合已有研究证据,专家组推荐,对于一般情况良好患者,予以SP或SOX方案(对于腹水较多的患者,因CDDP所需的水化可能会导致腹水的增多,故此类患者首选SOX方案);对于一般状况较差的患者,可考虑单药化疗(PTX、S-1、5-FU持续静滴)。 2.腹腔灌注化疗: 腹腔灌注化疗(IP)可以提高局部药物浓度,降低全身不良反应。由于腹膜转移是全身系统性疾病的局部反应,因此,全身系统化疗仍为核心治疗方案,腹腔灌注化疗为补充。目前,尚无大型临床研究确证腹腔灌注化疗的疗效,在PHOENIX-GC研究中观察到腹腔灌注PTX对中量腹水患者的临床疗效。因此,应结合腹水分级考虑在系统化疗的基础上添加腹腔灌注化疗。 国内有一些观察性研究和二期研究显示,5-FU/CDDP/PTX/DOX腹腔灌注化疗联合CF/5-FU/OXA对于晚期胃癌合并恶性腹水患者有一定疗效。 推荐方案:PTX(IP)联合S-1/PTX(Ⅲ级,Grade B);5-FU/CDDP(IP)联合5-FU/CAP/OXA(Ⅲ级,Grade B) 循证证据 (1)Ishigami等在三期随机对照临床研究PHOENIX-GC中,将183例胃癌腹膜转移患者以2︰1的比例随机分配至IP组(PTX腹腔灌注联合S-1/PTX全身化疗方案:PTX灌注20 mg/m2,d1和d8,静滴50 mg/m2,S-1 80 mg·m2·d-1,d1~14,每3周1周期)或SP组(CDDP 60 mg/m2,d8静滴,S-1 80 mg·m2·d-1,d1~21,每5周1周期)。结果显示,IP组和SP组的中位OS分别为17.7月和15.2月(HR= 0.72,95%CI:0.49~1.04,P= 0.08)。腹水量是影响预后的重要因素。将基线腹水因素进行校正后显示,IP组的生存获益显著(17.7月比14.3月,HR= 0.64,95%CI:0.43~0.94,P= 0.023),特别是在中量腹水(腹水位于盆腔以上)的患者中,两组的差异明显(13.0月比6.8月,HR= 0.38)。 (2)李燕等的一项观察性研究,纳入81例胃肠道恶性肿瘤并发腹腔积液患者,观察腹腔持续引流后直接腹腔化疗联合全身化疗治疗的疗效及患者不良反应。腹腔灌注药物5-FU类药物和(或)CDDP,之后1周行以5-FU或CAP为基础联合表柔比星(EPI)、CDDP(或OXA),进行2~4个周期的全身化疗。结果显示,81例患者中腹腔积液完全缓解(CR)16例(19.8%),部分缓解(PR)18例(22.2%),稳定(SD)27例(33.3%),进展(PD)20例(24.7%),总有效(CR PB)率42%;总获益(CR PR SD)率75.3%,中位进展时间(mTTP)4个月,中位生存期(mOS)5.3个月,1年生存率16.0%。 (3)黄万中等在一项二期临床研究中,纳入43例Ⅲb~Ⅳ期胃癌患者(其中14例合并腹膜转移)旨在评价多西紫杉醇腹腔灌注化疗联合CF/5-FU/OXA的临床疗效和安全性。结果显示,多西紫杉醇腹腔灌注化疗联合全身化疗总有效(CR PR)率为58.1%,1年生存率为67.4%,且不良反应可以耐受。 (4)李翔在一项观察性研究中,纳入23例晚期胃癌合并癌性腹水患者给予PTX 60 mg/m2腹腔灌注,d1、d5和d8;亚叶酸钙(LV)200 mg/m2静脉滴注2 h,d1~4;5-FU 750 mg/m2持续静滴24 h,每天1次,d1~4;OXA 130 mg/m2静滴2 h,d1。每21天为1个周期,每2个周期评价疗效。结果显示,有效率为69.6%,疾病控制率为86.9%,中位肿瘤进展时间为6.6月,1年生存率为71%。 3.手术: 对于确诊腹膜转移的初治患者,现有证据显示,手术联合化疗较单纯化疗没有显示生存优势,不推荐手术治疗;但如果存在外科急症如肠梗阻、出血、顽固性腹水等,多学科协作(multidisciplinary team,MDT)讨论后,可以考虑通过姑息性手术缓解相关症状。 对于化疗后出现明确的腹膜转移缓解(CY0P0)的患者,如一般状况较好,经过MDT讨论后,可以考虑手术治疗。但目前手术治疗胃癌腹膜转移仍缺乏前瞻性高级别证据,无论是减瘤手术还是姑息性手术,术后的获益人群仍然需要进一步明确。 五、胃癌腹膜转移相关并发症的处理 当胃癌腹膜转移患者出现癌性腹水和肠梗阻等并发症时,患者的生活质量和预后较差。针对并发症,目前分为对症治疗和抗肿瘤治疗两部分:对症治疗是以缓解症状为主的治疗,如腹水引流、利尿剂、低钠饮食、改善肠梗阻、维持营养状况等;抗肿瘤治疗是根据患者并发症的程度,经MDT讨论后,个体化地选择系统化疗、局部灌注治疗或最佳支持治疗。 1.癌性腹水的控制: 大约10%的胃癌患者存在腹水,而对于检出腹水> 50 ml的胃癌患者,腹膜转移的发生率高达75%以上。腹水患者常伴腹痛、厌食、腹胀、恶心等症状,以及黄疸和肠梗阻等并发症,临床处理难度极大。针对癌性腹水,尚无基于循证证据的治疗指南。目前,腹水引流仍然是临床控制腹水的主要手段,每日引流量应根据患者症状、血电解质、白蛋白水平综合考虑。 反复穿刺放腹水有引起有效循环血量下降、低钠血证、肾功能障碍、低白蛋白血症以及感染等并发症的危险。腹腔置管引流术适用于腹腔穿刺放液并发严重电解质紊乱或需反复腹腔穿刺放液的患者。该方法极少引起电解质紊乱,少有凝血机制障碍的危险,且引流管不易阻塞。 2.恶性肠梗阻的改善: 恶性肠梗阻是胃癌腹膜转移发生后的主要临床表现之一,此类患者占恶性肠梗阻患者总数的30%~40%。目前因认识不足,缺乏有效的治疗手段,临床主要的处理原则是对症治疗。 药物治疗需要联合应用抗分泌药物、止痛、止吐药物以及激素类药物来达到缓解恶性肠梗阻症状的目的。生长抑素类似物可起到良好的止吐效果;皮质类固醇激素不仅可以起到止吐作用,还可以减轻肿瘤周围及肠道的炎性病变和水肿,从而使肠道梗阻得到缓解;抗胆碱类药物可减少消化道平滑肌运动。 此类患者通常不适宜手术治疗,或因术后的高死亡率及高并发症发生率而无法获益。但对于肿瘤引起的单一部位梗阻或非癌性因素所导致的机械性梗阻,手术可作为治疗选择。 自扩张金属支架置入适用于胃幽门、十二指肠及结直肠梗阻的姑息治疗,被认为是腹腔转移癌所致结直肠梗阻的首选治疗。但对于多部位梗阻及腹腔广泛转移的患者,支架治疗属于禁忌。 全胃肠外营养(total parenteral nutrition,TPN)可改善患者的一般状况,纠正营养不良,TPN适用于Karnofsky评分>50、预计生存时间>2~3月、瘤生长缓慢、可能接受进一步化疗、肿瘤尚未引起其他重要脏器功能损害的患者。 腹水是影响患者生存预后的核心因素之一。临床实际中,不同腹水量患者的生存预后具有较大的差异。经CT检查评估腹水量将患者分级为:无腹水、少量腹水(腹水在盆腔以下)、中量腹水(腹水在盆腔以上)和大量腹水(腹水蔓延至整个腹腔并伴有症状),分别考虑予以不同治疗策略。 1.无/少量腹水患者: 全身系统化疗为核心治疗[参见五、(一)、1]。 2.中量腹水患者: 全身系统化疗的基础上,可以考虑联合腹腔灌注化疗,可以有效地控制腹水,改善生活质量、延缓恶液质[参见四、2]。 3.大量腹水患者: 由于预期生存较差,大量腹水的患者往往被排除在临床研究之外。因反复引流以及多种临床症状,该类患者往往很难实施抗肿瘤治疗。为此,针对该类患者,引流缓解症状配合最佳支持治疗仍然是主要的治疗手段。对于腹水控制良好、且体能较好的患者,可以经MDT讨论后给予抗肿瘤治疗。 六、结语 本共识以循证证据和临床现实为基础、以规范中国胃癌腹膜转移患者诊疗现状为出发点、以综合国内胃癌领域专家认知为原则而撰写。力求简单实用、科学严谨,具有普遍适用性。部分尚未在国内上市的药物(如卡妥索单抗),以及尚在研究阶段的治疗方案(如减瘤手术、术前新辅助腹腔灌注化疗、腹腔灌注贝伐珠单抗等),未列入其中。 希望通过本共识的制定,能为广大临床医师提供工作参考。胃癌腹膜转移的诊疗流程见图2。初诊伴有腹膜转移者治疗流程图见图3。随着更多高级别的临床研究公布,专家委员会将及时对共识的内容进行更新和补充,以期不断提高我国胃癌的诊治水平。 图2 胃癌腹膜转移的诊疗流程图(图中治疗推荐仅针对P1或CY1为唯一非治愈因子的情况,如果出现多脏器转移,应以全身系统治疗为主) 图3 初诊伴有腹膜转移者治疗流程图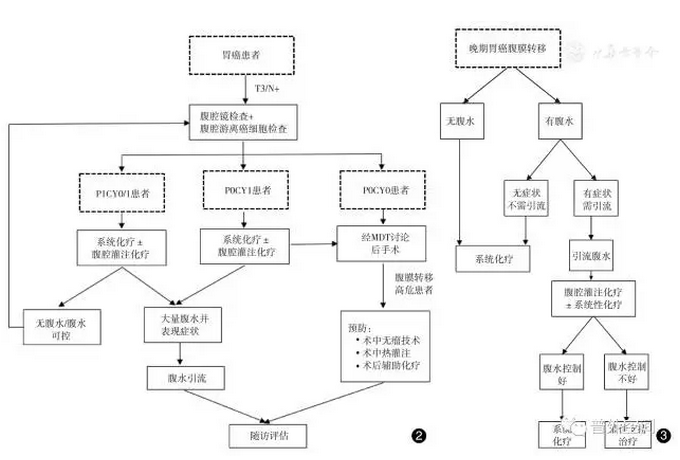
作者:中国抗癌协会胃癌专业委员会
文章来源:中华胃肠外科杂志,2017,20(5)
收藏
回复(2)参与评论
评论列表
























