中国肿瘤患者膳食营养白皮书9(胃癌、结直肠癌的营养支持治疗)
不同部位肿瘤患者的营养支持治疗
一、胃癌的营养支持治疗
(一) 概述
胃癌(Gastric Carcinoma) 是指原发于胃的上皮源性恶性肿瘤。全球每年新发胃癌病例约120万,中国约占其中的40%。在我国胃癌发病率仅次于肺癌居第二位,死亡率排第三位。我国早期胃癌占比很低,仅约 20%,大多数发现时已是进展期,总体5年生存率不足50%。近年来随着胃镜检查的普及,早期胃癌比例逐年增高。
所有的肿瘤都会在不同程度上影响营养素的摄入和/或利用,从而造成营养不良。不同肿瘤营养不良的发生率不同,大体上说消化系统肿瘤高于非消化系统肿瘤,上消化道肿瘤高于下消化道肿瘤。
1>胃癌患者营养不良的原因主要有:
①疾病本身导致的厌食、抑郁相关性厌食使食物摄入减少。在所有肿瘤中,胃癌引起的厌食、早饱感发生率最高;
②机械性因素造成的摄入困难;
③化疗药物毒性引起的吸收和消化障碍;
④ 合并有分解代谢增加的因素,比如感染或手术治疗。同期放化疗具有吸烟饮酒嗜好的胃癌患者,在粒细胞下降时容易发生局部感染;
⑤胃手术特有的影响:在所有胃肠道手术中,以胃手术的并发症最多、对营养与代谢的影响最大、持续时间最长。临床上,营养不良是胃癌患者的常见问题。15%的患者在诊断初期即有体重减轻。
2>胃癌病人发生营养不良的原因及机制复杂,
与肿瘤本身的特点及抗肿瘤治疗对机体的影响有关。恶性肿瘤导致进食调节中枢功能障碍,手术、放化疗等抗肿瘤治疗导致的疼痛、恶心呕吐、焦虑抑郁等,引起厌食和早饱,影响营养物质的摄入。同时,肿瘤病人的营养物质代谢特点不同于非肿瘤病人,碳水化合物代谢异常、蛋白质转化率增加、脂肪分解增加、脂肪储存减少、肌肉及内脏蛋白消耗、瘦体重减少、水电解 质平衡紊乱、能量消耗改变等,均会诱发和加重营养不良。

3>胃癌相关性营养不良带来的负面影响也体现在机体及功能两个层面。
它削弱了放化疗的疗效,增加了药物不良反应风险、术后并发症和院内感染的机会以及各种并发症的发生率和病死率,降低了骨骼肌质量和功能以及患者的生活质量,延长了住院时间,增加了医疗费用。营养不良还限制了胃癌患者治疗方案的选择,使得他们不得不选择一些非最优或者不恰当的治疗方案。总之,营养不良与预后不良密切相关。对于接受肿瘤手术切除的胃癌患者和接受姑息治疗的胃癌患者来说, 充足的营养支持是必不可少的。营养不良的胃癌患者面临着更大的风险,包括更高的并发症发生率和更低的生存率。因此,营养不良在胃癌的治疗中显得尤为重要。
(二) 营养代谢特点
1>能量代谢异常
一些调查报道显示癌症病人能量代谢需要比正常代谢高 10%。但亦有报道认为未见有明显差别。然而癌症病人的体重下降较明显,除摄入减少的原因外,消耗的增加亦是不能忽视的一个方面。
2>碳水化合物代谢异常
有氧糖酵解增强,葡萄糖摄取和消耗增加,主要表现为葡萄糖的氧化和利用降低,葡萄糖转化增加,胰岛素抵抗和胰岛素分泌相对不足。
3>脂肪代谢异常
癌症病人有大量蛋白质的丧失,应激和肿瘤本身释放脂溶因素可使脂肪分解作用增加,合成降低,血清脂蛋白脂酶活性降低,出现高脂血症,主要表现为血浆脂蛋白、 甘油三酯和胆固醇升高,外源性脂肪利用下降,脂肪动员增加。
4>蛋白质代谢异常
癌症病人体内蛋白质的转换率增加。肝脏蛋白质合成增加,肌肉中的蛋白质合成降低。主要表现为骨骼肌不断降解,体重下降,内脏蛋白消耗和低蛋白血症,血浆支链氨基酸含量下降。
5>维生素代谢异常
病人血浆中可见到抗氧化营养素下降,如β-胡萝卜素,维生素C、E等。此外其他维生素如维生素B12在胃癌病人血浆中含量降低,叶酸亦有降低。
6>微量元素代谢异常
癌症病人大多都有血硒含量的降低和锌含量的降低,同时可见到抗氧化能力降低和细胞免疫功能的下降。胃癌病人还可见到血钴和血锰含量的下降。
(三) 营养评估
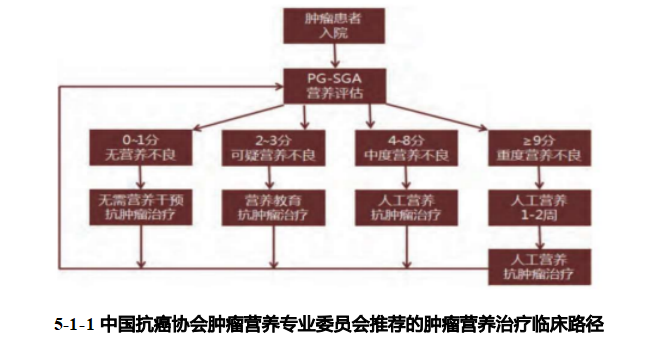
正确评定每个肿瘤患者的营养状况,筛选出具备营养治疗适应证的患者,及时给予治疗。为了客观评价营养治疗的疗效,需要在治疗过程中不断进行再评价,以便及时调整治疗方案。目前临床上常用的营养筛查与评估工具包括:营养风险筛查2002(Nutritional Risk Screening 2002,NRS 2002)、主观整体评估(Subjective Globe Assessment,SGA)、患者主观整体评估(Patient-Generated Subjective Global Assessment,PG-SGA)、微型营养评估(Mini Nutritional Assessment,MNA)、营养不良通用筛查工具(Malnutrition Universal Screening Tools,MUST) 等。
现阶段应用最广泛的恶性肿瘤营养风险筛查工具为营养风险筛查量表(NRS2002)及患者营养状况主观评估表(PG-SGA)。NRS评分<3分者虽然没有营养风险,但应在其住院期间每周筛查1次。NRS评分≥3分者具有营养风险,需要根据患者的临床情况,制订基于个体化的营养计划,给予营养干预。
(四) 营养支持治疗
胃癌病人的营养治疗是综合治疗的重要组成部分,应从疾病确诊开始,在多学科综合治疗协作组(multiple disciplinary team,MDT)讨论时参与治疗方案的制定和调整,贯穿抗肿瘤治疗的全过程。胃癌综合治疗方案的制定和优化依赖多学科协作,除手术、放化疗、靶向治疗等抗肿瘤治疗手段之外,营养治疗也是胃癌综合治疗的重要组成部分,是一线治疗。营养不良会严重影响病人对治疗的耐受性和疗效,增加不良反应和治疗并发症,影响抗肿瘤治疗方案的顺利实施。通过营养治疗,包括饮食指导、 改善摄食、经口营养补充和人工营养支持,为机体提供充足的营养底物,防止营养状况的进一步恶化,帮助病人更加安全地接受抗肿瘤治疗。
1>能量和蛋白质需求
若条件允许,推荐采用间接测热法对病人静息能量消耗进行测定。若无法测定病人的能量消耗值,也可采用体重公式进行估算,按照25~30kcal/(kg·d)来计算能量的目标需要量,但需要根据病人的年龄、活动量、应激水平、肝肾功能等情况进行校正和调整,理想的实际补充量应达到目标需要量的80%左右。对于长期营养不良的病人,营养治疗应循序渐进,监测电解质及血糖水平,警惕再喂养综合征的发生。病人术后早期受手术创伤、炎症等刺激,处于应激状态,允许相对低热量供能[15~25 kcal/(kg·d)],利于降低感染相关并发症的发生率。
充足的蛋白质供应对胃癌患者十分重要,充足的能量和蛋白质摄入可明显降低危重病人的死亡风险。ESPEN 推荐对恶性肿瘤病人按照1.0~2.0g/(kg·d)补充蛋白质。胃癌手术病人围手术期推荐按照1.2~1.5g/(kg·d)计算蛋白质需要量。接受大型手术的病人或处于重度应激反应的病人对蛋白质的需求量更高,围手术期按照1.5~2.0g/(kg·d)补充蛋白质,并根据病人实际情况适当调整。
非荷瘤状态下三大营养素的供能比例与健康人相同,为碳水化合物50%~55%、 脂肪25%~30%、蛋白质15%;荷瘤患者应该减少碳水化合物在总能量中的供能比例,提高蛋白质、脂肪的供能比例。按照需要量100%补充矿物质及维生素,根据实际情况可调整其中部分微量营养素的用量。
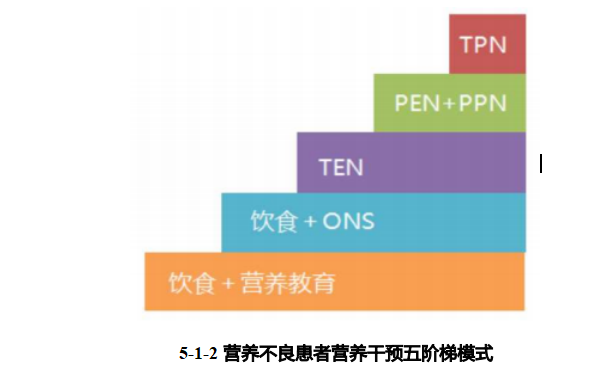
2>营养不良的五阶梯治疗模式
营养不良的规范治疗应该遵循五阶梯治疗原则:首先选择营养教育,然后依次向上晋级选择口服营养补充(oral nutritional supplements,ONS)、全肠内营养(total enteral nutrition,TEN)、部分肠外营养(partial parenteral nutrition,PPN)、全肠外营养(total parenteralnutrition,TPN)。参照ESPEN指南建议,当下一阶梯不能满足 60% 目标能量需求 3~5天时,应该选择上一阶梯。
3>营养治疗途径
胃癌患者营养治疗的途径同样包括肠内营养(口服、管饲)及肠外营养(静脉)。口服是生理的途径,是第一选择。胃癌患者围手术期、围放疗期、围化疗期等治疗期间乃至家居期间营养治疗首选口服营养补充(ONS),必要时辅以静脉途径补充口服(日常饮食)摄入的不足部分,如部分肠外营养(PPN)或补充性肠外营养(SPN)。
任何情况下,只要肠内途径可用,应优先使用肠内营养。手术后应尽早(24小时内) 开始肠内营养。术后患者推荐首选肠内营养;鼓励患者尽早恢复经口进食,对于能经口进食的患者推荐口服营养支持;对不能早期进行口服营养支持的患者,应用管饲喂养,胃癌患者推荐使用鼻空肠管行肠内营养。
补充性肠外营养(SPN)给予时机:NRS-2002≤3分或NUTRIC Score≤5分的低营养风险患者,如果EN未能达到60%目标能量及蛋白质需要量超过7天时,启动SPN支持治疗;NRS-2002≥5分或NUTRIC Score≥6分的高营养风险患者,如果EN在48~72小时内无法达到60%目标能量及蛋白质需要量时,推荐早期实施SPN。当肠内营养的供给量达到目标需要量60%时,停止SPN。
4>营养治疗评价:
营养干预的疗效评价指标分为三类 :
①快速变化指标:为实验室参数,如血常规、电解质、肝功能、肾功能、炎症参数(IL- 1、IL-6、TNF、CRP)、营养套餐(白蛋白、前白蛋白、转铁蛋白、视黄醇结合蛋白、游离脂肪酸)、血乳酸等,每周检测 1~2 次。
②中速变化指标:人体测量参数、人体成分分析、生活质量评估、体能评估、肿瘤病灶评估(双径法)、PET-CT代谢活性。每4~12周评估一次。
③慢速变化指标: 生存时间,每年评估一次。
(孙 洁; 姚 颖, 华中科技大学附属同济医院主任医师)
二、结直肠癌的营养支持治疗
2018 年中国国家癌症中心发布的全国癌症统计数据显示,我国结直肠癌(colorectalcancer,CRC) 每年发病约 37 万例,占恶性肿瘤发病率的第 3 位。就世界范围来看,其分布在不同国家有明显差异:欧美等发达国家发病率较高,而非洲、中 南亚地区发病率较低。中国许多地区,尤其是经济发达的城市,由于生活水平提高,生活和饮食习惯西化,结直肠癌发病率有明显上升趋势。目前,已有结直肠癌术前营养状况调查发现,有 50%的患者术前即出现体重丢失,约20%患者术前已存在营养不良。而体重明显丢失(>3 kg)患者病死率较体重丢失不明显组上升 2 倍。良好的营 养干预和治疗不仅可以提高患者对手术的耐受度、降低手术并发症发生率、节约住院花费、缩短住院时间。

(一) 发病风险
目前普遍认为结直肠癌的发生是饮食、环境、生活方式和遗传因素共同作用的结 果。大量研究证实,超重/肥胖、膳食结构不合理(缺乏水果蔬菜、经常食用红肉和加 工肉)、过量饮酒、缺少体育锻炼、久坐生活方式、吸烟以及遗传因素等是结直肠癌发 病的高风险因素。其中饮食因素是至关重要的危险因素,通过改变饮食和生活习惯,能有效降低结直肠癌的发生风险,如美国结直肠癌的发病率已从 1976 年的 60.5 人/10 万人下降到 2005 年的 46.4 人/10 万。
(二) 营养问题
1>腹痛或排便习惯改变
超过 90%的腹腔手术患者都会发生一定程度的腹腔粘连,主要表现为腹痛或腹部不适,便秘或腹泻等排便习惯的改变。化疗或腹部放疗的胃肠道毒副作用也可导致患者出现痉挛性腹痛、腹泻等,严重影响营养素的摄入、消化及吸收。部分患者会出现 慢性放射性肠炎,甚至发生慢性肠梗阻或肠瘘等并发症,而这一系列并发症又促进和加重了营养不良的发生和发展。
2>恶心、呕吐
临床上治疗结直肠癌主要采用以手术为主的综合治疗,胃肠手术后恶心、呕吐的发生率高达 70%~80%。化疗常见的不良反应为胃肠道的毒性,可导致黏膜炎、口腔干 燥、恶心呕吐等。腹部放疗可通过直接和间接的方式损伤肠道黏膜屏障功能,导致恶心、呕吐等症状。
3>营养不良
结直肠癌患者易出现营养不良。大多患者早期症状不明显,发现时已属中晚期,因此营养不良的发生率较高,增加了术后的并发症和病死率。有研究报道,50%结直 肠癌患者可出现体重丢失,20%结直肠癌患者出现营养不良。2015 年美国外科医师协 会与国家外科质量改善项目(ACS-NSQIP) 报道,结直肠癌患者术后病死率与术前低 白蛋白血症、低体重指数(BMI)小于18.5显著相关。

(三) 营养原则
结直肠癌高风险人群应改善生活和饮食习惯,控制总能量摄入,维持标准体重,避免超重或肥胖。研究表明,膳食纤维可被人体肠道菌群分解,产生短链脂肪酸,从而降低肠道 pH 值,还可增加粪便量,从而改善肠道内环境,减少结直肠癌发病风险。因此,应提倡科学的饮食结构,适当增加富含膳食纤维和维生素的蔬菜和水果的摄入。 同时,高风险人群应减少高脂食物的摄入,适当增加饮水量,避免吸烟、过量饮酒、久坐等不良生活习惯。对于手术和放化疗患者应注意以下营养原则:
1>能量
对于进食情况、营养状况良好的超重或肥胖结直肠癌患者,应注意控制体重和减肥,减少能量摄入。对于进食情况较差、具有营养风险或者营养不良患者,则应尽早开始肠内营养或肠外营养治疗。
2>脂肪
脂肪摄入量应控制在总能量的 30%以下,其中不饱和脂肪酸和饱和脂肪酸的比例为 2:1,尤其注意补充深海鱼等富含 ω-3 多不饱和脂肪酸的食物。
3>蛋白质
没有营养性贫血的患者以禽、鱼虾、蛋、乳和豆类为蛋白质主要来源,减少红肉摄入,尤其是加工红肉,例如热狗、腊肠、香肠、熏肉、火腿及午餐肉等。
4>膳食纤维
术后早期患者可选用富含可溶性膳食纤维的食物或医用食品。膳食恢复正常后,可适当增加膳食纤维摄入量,少选用精制食物。一般来说,每 100 克的食物里膳食纤 维含量高于 2 克的都是高纤维食物,植物性食物是纤维素的主要来源,在蔬菜、水果、 豆类、粗粮、菌藻、坚果类的食物中含量较多。
5>维生素
大量临床研究、动物研究及分子生物水平研究均证实,维生素 D 是结直肠癌的保护因素,可抑制结直肠癌的发生发展,因此,结直肠癌患者应多晒太阳,并有意识补充富含维生素 D 的食物,如肝脏、乳制品等。充足的维生素摄入是保障肠道健康的重要因素,维生素缺乏的结直肠癌患者应注意适当补充。
6>益生菌和益生元
肠道菌群失调导致局部环境内稳态失衡,从而引起肠道对于有毒化学物吸收增加 被认为是结直肠癌的重要发病机制。双歧杆菌、乳酸杆菌等肠道有益菌能够与肠道黏 膜结合形成生物学屏障,保护肠道不受生物、化学因素的侵袭,同时还可以调节机体免疫因子,从而达到防癌作用。益生元作为益生菌的消化底物,可以在体内促进肠道有益菌的生长和繁殖,改善肠道微生态,进而提高免疫力。
7>水
足量饮水可以减少肠道疾病。一项病例对照研究发现水的摄入量与结直肠癌发病之间有着较强的负剂量-反应关系,即水摄入量越多,结直肠癌的发病风险越小。
(四) 营养治疗
对于营养状况良好的结直肠癌患者,可在营养师的指导下选择科学合理的治疗膳食。如 NRS 2002 营养风险评分≥3 分或营养不良患者,应立即启动肠内或肠外营养。

1>治疗膳食
对于结直肠癌保肛术后营养状况良好的稳定期患者, 应减少富含饱和脂肪酸和胆固醇的食物摄入,适当增加膳食纤维摄入,防止体重超重和肥胖。食物多样化,适当增加大豆制品、新鲜的深色蔬菜、新鲜水果、酸奶等健康食物。足量饮水,可以选择白开水或淡茶等。避免食用肥腻、辛辣、刺激性食物、腌制、烟熏和油炸食物。对于 肠造口患者应尽量减少易产气食物的摄入,如黄豆、牛奶、白萝卜、洋葱、韭菜、大蒜等。
对于中重度营养不良同时伴有便血的结直肠癌患者,应注意给予少渣、高蛋白半流质饮食,每天能量目标需要量可高达40~50kcal/kg供给,蛋白质为1.5~2.0g/kg,以增加营养,提高机体的免疫功能。
2>肠内营养(enteral nutrition,EN)
当治疗膳食不能达到营养目标量 60%持续 3~5 天时,有消化道功能的结直肠癌患 者可以结合临床实际情况选择口服营养补充剂(oral nutritionalsupplements,ONS) 和 /或管饲(enteral tube feeding,ETF)。根据《结直肠癌围手术期营养治疗中国专家共识 (2019 版)》,结直肠癌患者总能量按照 25~30 kcal/(kg·d)提供,蛋白质目标需要量为 1.0~1.5 g/(kg ·d)。对于中重度营养不良的结直肠癌患者,可适当提高营养治疗配方中 脂肪供能的比例, 增加膳食能量密度。补充生理需要量的维生素及微量元素。
3>肠外营养(parenteral nutrition,PN)
根据《中国肿瘤营养治疗指南(2015 版)》营养不良的五阶梯治疗原则,如果肠内营养不能满足营养目标量60% 持续3~5天时,则建议加用补充性肠外营养(supplemental parenteralnutrition, SPN)。如患者出现完全性肠梗阻、严重吻合口漏、 肠功能衰竭等 EN 绝对禁忌症,则由临床医生、营养师和护士共同组成的营养支持小 组根据患者的具体病情和病程,制定个体化全肠外营养方案,启动全肠外营养(total parenteral nutrition,TPN) 治疗。
(郑璇, 上海长海医院主任医师)
收藏
回复(5)参与评论
评论列表
























