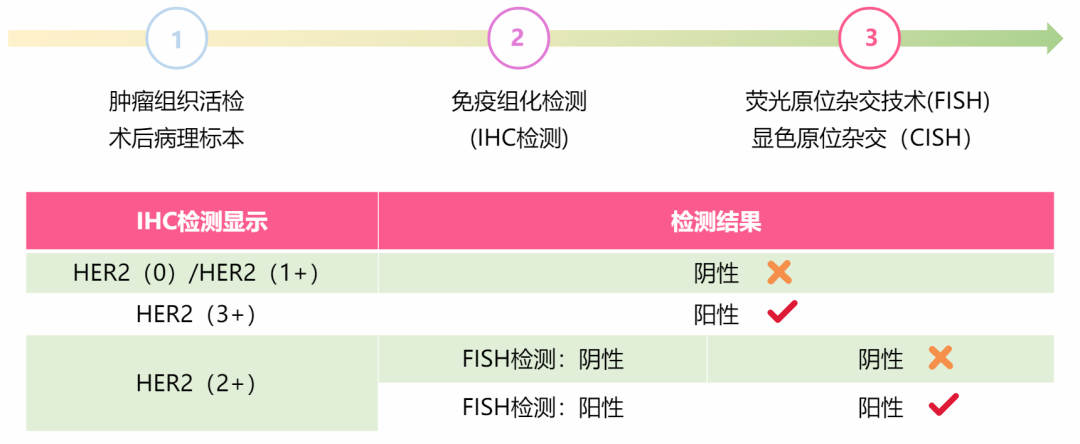
2022年12月18日,在隆重召开的京城肿瘤冬季论坛暨2022 SABCS会议,中国乃至世界首部《人表皮生长因子受体2低表达乳腺癌临床诊疗共识(2022版)》(以下简称《HER2低表达乳腺癌临床诊疗共识》)发布会正式启动。在过去谈论乳腺癌的HER2分型时,往往非阴即阳,经常看到“HER2 ”或“HER2-”的表述。研究者们通过IHC和ISH两项检测判断是否为HER2阳性乳腺癌。
这个判定结果决定了患者能否接受抗HER2靶向治疗。然而在科学不断发展的进程中,研究者发现虽然抗HER2药物对HER2表达1-2个“ ”且原位杂交(ISH)阴性的乳腺癌疗效不佳。于是,近年来,有人提出将这种病理类型的乳腺癌称为“HER2低表达”乳腺癌。2021 CSCO乳腺癌指南中将HER2低表达定义:IHC2 且ISH阴性或IHC1 。既往的三阴性乳腺癌和HR阳性乳腺癌中都含有HER2低表达的患者。一项纳入5235例 I-III期 HER2阴性患者的研究显示,HR 中HER2低表达占58%,TNBC中占39%[1]。既往三阴性乳腺癌以及激素受体阳性乳腺癌中的HER2低表达患者多以传统的化疗或是内分泌治疗为主,治疗效果差强人意。因此,针对HER2低表达乳腺癌,目前仍缺乏特异性的治疗方法。新一代HER2靶向药的问世,为HER2低表达患者的治疗提供新的选择。上世纪80年代,美国学者重拾Paul Ehrlich教授的“魔法子弹”理念,提出了“抗癌精准导弹”理论。最终研制出来的就是抗体偶联药物(ADC)。ADC药物通过将单抗部与肿瘤细胞表面的靶蛋白结合,通过内吞作用进入肿瘤细胞,随后释放小分子细胞毒药物杀伤肿瘤细胞,在肿瘤细胞被杀死后,剩余的细胞毒药物开始杀伤周围的肿瘤细胞,即“旁观者效应”。HER2——这个最早成功的靶向治疗靶点之一,再次成就了ADC这类如今备受关注药物。HER2低表达的患者,癌细胞表面也有HER2分子,只是数量较少,仅靠普通的抗HER2靶向药抑制HER2功能不足以杀死这些癌细胞。但如果在单抗上偶联上化疗药物,通过癌细胞表面少量的HER2分子,精准地把化疗药运送到癌细胞处,或许就能有效杀死HER2低表达的癌细胞了。DESTINY-Breast04是首个针对HER2低表达转移性乳腺癌患者的HER2靶向治疗的III期临床试验,与标准治疗相比,该试验在无进展生存期和总生存期方面显示出具有统计学意义和临床意义的益处。正如同当年HER2抗体问世,极大改善HER2阳性乳腺癌患者的生存预后一样,现如今如雨后春笋般问世的HER2 ADC,也必将为HER2低表达这一类患者群体带来突破暗影的利剑。随着DS-8201对HER2低表达乳腺癌患者疗效的确立, HER2低表达或成为乳腺癌新的靶向治疗亚型。为了更好地规范HER2 低表达乳腺癌临床合理诊疗,本共识专家委员会参考国内外最新的临床研究以及近年来发表的重要参考文献,结合我国病理科医生和肿瘤科医生的临床经验, 经专家组讨论后形成本共识。
专家意见1:目前HER-2低表达定义为HER-2 IHC1 或IHC2 /ISH-。专家意见2:对于既往判断为HER-2 IHC0的患者,如患者有潜在治疗可能,可考虑重新判读、检测或活检,以明确HER-2状态。专家意见3:HER-2低表达已成为晚期乳腺癌中可预测临床疗效的药物选择指标,用于指导临床药物选择。专家意见4:依据DS-8201在HER-2低表达晚期乳腺癌中的确切疗效,其可作为HER-2低表达患者的推荐治疗之一。HER-2低表达患者的初始治疗仍应基于分子分型进行治疗方案的选择。专家意见5:对于HER-2低表达HR 不伴内脏危象的晚期乳腺癌患者,一线CDK4/6抑制剂联合内分泌治疗进展后,应基于患者的既往治疗、肿瘤负荷和生物标志物等选择后线治疗方案。专家意见6:对于HER-2低表达HR 的内分泌难治性(经内分泌治疗失败或不适合内分泌治疗)且至少接受过1种化疗后的晚期乳腺癌患者,优选T-DXd治疗。专家意见7:HER-2低表达HR-晚期乳腺癌的治疗目前参照TNBC治疗,包括化疗、免疫治疗、靶向治疗及SG治疗等。 对于一线治疗失败的患者,DS-8201可作为新的推荐方案之一。我国《HER2低表达乳腺癌临床诊疗共识》是世界范围内首个针对HER2低表达领域的临床共识,将为HER2低表达晚期乳腺癌患者的诊疗规范性提供重要指导和建议。
封面图片来源:稿定设计
责任编辑:乳腺癌互助君
参考来源:
[1]Li Y et al. Front Oncol. 2022 Jan 17;11:774577.
[2]Fehrenbacher L, Cecchini RS, Geyer CE Jr, et al. NSABP B-47/NRG Oncology Phase III Randomized Trial Comparing Adjuvant Chemotherapy With or Without Trastuzumab in High-Risk Invasive Breast Cancer Negative for HER2 by FISH and With IHC 1 or 2. J Clin Oncol. 2020 Feb 10;38(5):444-453.
[3] Gianni L, Lladó A, Bianchi G, et al. Open-label, phase II, multicenter, randomized study of the efficacy and safety of two dose levels of Pertuzumab, a human epidermal growth factor receptor 2 dimerization inhibitor, in patients with human epidermal growth factor receptor 2-negative metastatic breast cancer. J Clin Oncol. 2010 Mar 1;28(7):1131-7.
[4]Press MF, Finn RS, Cameron D, et al. HER-2 gene amplification, HER-2 and epidermal growth factor receptor mRNA and protein expression, and lapatinib efficacy in women with metastatic breast cancer. Clin Cancer Res. 2008;14(23):7861-7870.
[5] Burris HA 3rd, Rugo HS, Vukelja SJ, et al. Phase II study of the antibody drug conjugate trastuzumab-DM1 for the treatment of human epidermal growth factor receptor 2 (HER2)-positive breast cancer after prior HER2-directed therapy. J Clin Oncol. 2011 Feb 1;29(4):398-405.
[6]Krop IE, LoRusso P, Miller KD, et al. A phase II study of trastuzumab emtansine in patients with human epidermal growth factor receptor 2-positive metastatic breast cancer who were previously treated with trastuzumab, lapatinib, an anthracycline, a taxane, and capecitabine. J Clin Oncol. 2012 Sep 10;30(26):3234-41.