DS8201(Enhertu)乳腺癌her2阳性中国正式提交上市申请
长期以来,HER2低表达的乳腺癌患者没有靶向治疗的机会,不能从HER2靶向治疗里获益。这部分乳腺癌患者会根据激素受体表达、PD-L1表达来选择其他治疗措施。现在,DS-8201的出现将改变这部分乳腺癌患者的治疗格局。DS-8201还可以与免疫药物、内分泌治疗药物、化疗药物进行组合,这无疑增加了治疗的选择机会,相信会有更多患者受益。
一、DS-8201治疗HER2阳性乳腺癌III期临床研
8月15日,阿斯利康/第一三共联合宣布,Trastuzumabderuxtecan(DS-8201,T-DXd,Enhertu)的III期DESTINY-Breast02临床成功,达到主要研究终点:在既往接受过T-DM1治疗的HER2阳性不可切除和/或转移性乳腺癌患者中,与标准疗法相比,T-DXd组的无进展生存期(PFS)具有统计学意义和临床意义改善。此外,该研究还达到了改善总生存期(OS)的关键次要终点。
DESTINY-Breast02是一项随机、多中心、开放标签的III期试验,旨在评估与标准疗法(曲妥珠单抗/卡培他滨或拉帕替尼/卡培他滨)相比,T-DXd(5.4mg/kg)在既往接受过T-DM1治疗的HER2阳性不可切除和/或转移性乳腺癌患者中的有效性和安全性。
该研究主要终点是基于盲法独立中心评估(BICR)的PFS。关键次要终点是OS,其他次要终点包括基于BICR和研究者评估的客观缓解率(ORR)和缓解持续时间(DoR)等。
研究结果显示,T-DXd显著延缓了HER2阳性转移性乳腺癌患者的疾病进展。T-DXd在DESTINY-Breast02研究中的安全性与之前的试验一致,未发现新的安全性问题。间质性肺病(ILD)的发生率和严重程度与在其他转移性乳腺癌试验中观察到的一致,经独立评审委员会确认的5级ILD事件发生率较低。
二、首个肺癌HER2靶向药物
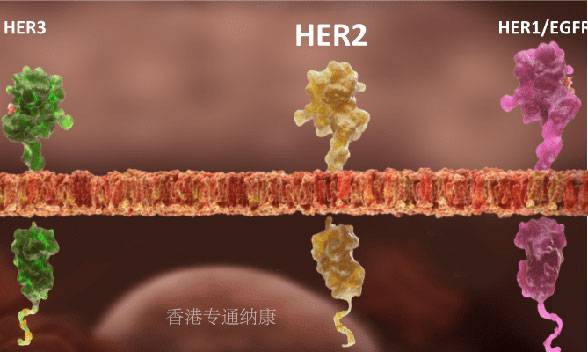
HER2也是非小细胞肺癌中较为常见的一个突变,发生率在2%~4%左右。与乳腺癌中不同,肺癌的HER2突变以20外显子的插入突变HER2YVMA为主,这也使得现有的HER2靶向疗法在肺癌中疗效不佳,无一获批。
 而DS-8201改变了这一切。在DESTINY-Lung01研究中,接受DS-8201治疗的91位HER2阳性非小细胞肺癌患者,1人完全缓解,49人部分缓解,共有84人的肿瘤缩小,客观缓解率和疾病控制率分别达到了55%和92%。
而DS-8201改变了这一切。在DESTINY-Lung01研究中,接受DS-8201治疗的91位HER2阳性非小细胞肺癌患者,1人完全缓解,49人部分缓解,共有84人的肿瘤缩小,客观缓解率和疾病控制率分别达到了55%和92%。
随后的DESTINY-Lung02研究中,DS-8201又在目前的52名HER2阳性肺癌患者中,取得了58%的客观缓解率和8.7个月的中位疗效持续时间。
FDA也因此加速批准了DS-8201用于接受过全身治疗的HER2阳性不可切除或转移性非小细胞肺癌,让它成为了首个用于肺癌的HER2靶向疗法。
三、DS8201(Enhertu)正是提交国内上市申请
值得注意的是,Enhertu已于今年3月正式递交国内上市申请,并于5月被正式纳入优先审评目录,首个适应症为:治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
乳腺癌在全球和中国高发癌种中分别排名第二位和第五位,相关治疗药物拥有巨大的市场空间,ADC药物尽管靶点众多,乳腺癌一定是必争之地。作为一个刚刚启动的增量市场,ADC药物市场空间广阔,目前谈论过度竞争言之尚早。
收藏
回复(7)参与评论
评论列表
























