同行分享|CLDN18.2 靶点介绍
CLDN18属于Claudins蛋白家族成员,Claudin蛋白由ShoichiroTsukita及其同事在1998年发现。在人体内由CLDN18基因编码,该蛋白表达在上皮上。上皮细胞是位于皮肤或腔道表层的细胞,主要功能是作为物理和化学屏障,上皮细胞间连接最主要的连接是紧密连接。Claudin是构成细胞紧密连接的重要分子,紧密连接决定了上皮细胞的渗透性,也起到阻挡细胞膜表面蛋白和脂质扩散的作用1。
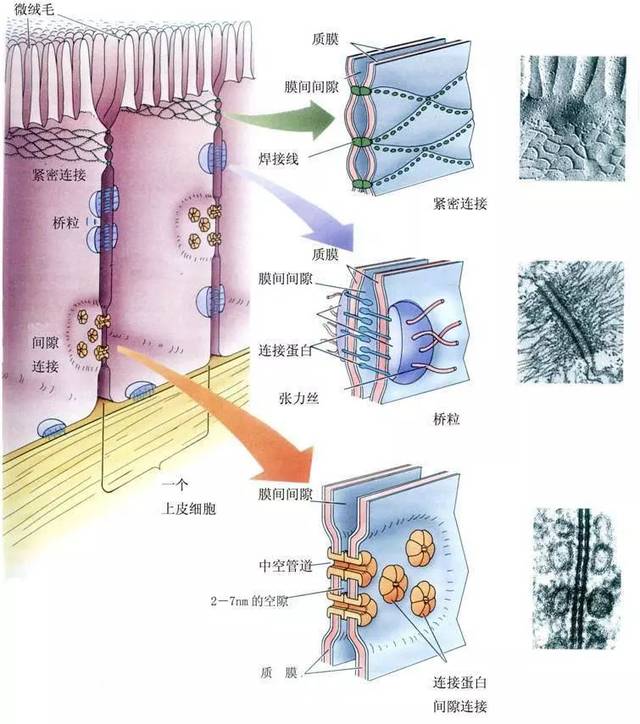
图1 小肠上皮细胞的三种连接方式:紧密连接、桥粒和间隙连接2
通过形态学研究,预测Claudin蛋白存在于所有的脊椎动物中和背囊动物中。对于大部分物种仅有几种Claudin蛋白,哺乳动物中有27中Claudin基因,并不是这些基因存在于一种物种中,例如,人有26个Claudin基因,唯独缺少CLDN-13基因。
CLDN18基因及蛋白结构特征:
人的CLDN18基因具有两个不同的1号外显子,转录后经过可变剪接最终生成仅在N端具有不同序列的两个蛋白亚型CLDN18.1和CLDN18.2,如图2所示。
CLDN18.1和CLDN18.2均由261个氨基酸组成,均具有四个跨膜结构域,NH2端和COOH端位于胞内,具有两个胞外环(ExtracellularLoops:ECL1,ECL2)。CLDN18.1和CLDN18.2胞外区1中仅存在8个氨基酸差别,如图2所示。
鉴于CLDN18的膜蛋白特性,CLDN18.1和CLDN18.2的高度同源性及ECL1存在高级结构,筛选针对CLDN18.2的高质量抗体具有较大的难度。
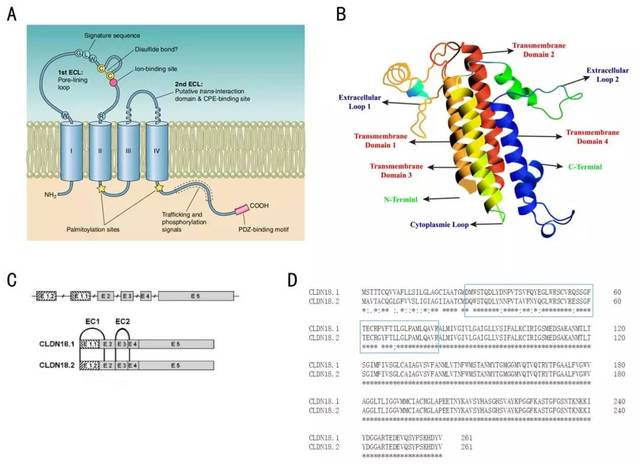
图2 A.Claudin蛋白模型;B.CLDN18蛋白模型1,3;C.CLDN18基因位点的结构及对应变体中外显子组成,方框分别表示CLDN18.1(E 1.1)和CLDN18.2 (E 1.2)特异的第一外显子4;D.CLDN18.1和CLDN18.2氨基酸序列比对,蓝色框表示第一个胞外环(ECL1)序列
CLDN18组织特异性表达:
不同的Claudin蛋白表达在不同的组织上,在人体中CLDN18.1和CLDN18.2的表达具有组织特异性,CLDN18.1主要表达在肺组织中,CLDN18.2作为一个高度特异性的细胞表面分子,在正常的组织中仅表达在分化的胃粘膜上表皮细胞上,不表达在胃干细胞上4。
CLDN18.2在肿瘤细胞激活表达:
在原发性胃癌及其转移后癌症类型中大部分都表达CLDN18.2分子,另外在胰腺癌,食管癌,卵巢癌,肺癌中也常常观察到CLDN18.2被激活表达。CLDN18.2的激活表达依赖于转录因子环腺苷酸应答元件结合蛋白结合到其基因未甲基化的蛋白结合位点上。由于CLDN18.2在正常组织表达的高度特异性及在多种癌症中被激活表达,因此针对上皮性肿瘤,CLDN18.2成为极具潜力的靶点4。
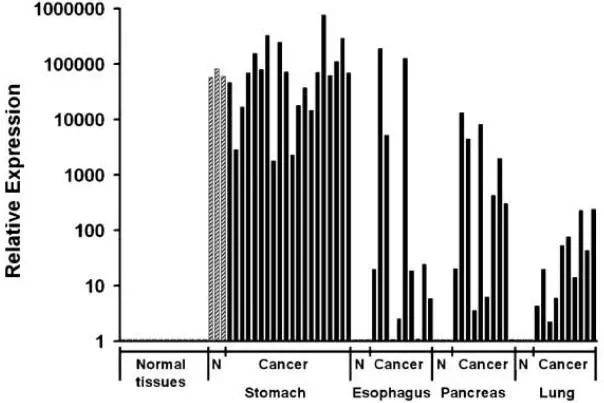
图2 CLDN18.2在多种肿瘤组织中表达,N:Normalhuman tissues4
CLDN18.2抗体临床研究:
Claudin蛋白作为组织特异性蛋白,其作用与各自组织肿瘤发生具有相关性。CLDN-1在结肠癌上,CLDN-10在肝细胞癌上,CLDN-18在胃癌上具有相应的临床价值。CLDN18.2作为细胞膜表面蛋白,暴露的胞外结构允许抗体的结合,这些特点表明CLDN18.2是一个理想的治疗性单克隆抗体开发的靶点。
2016年10月29日,日本制药企业安斯泰来宣布以14亿美元收购德国GanymedPharmaceuticalsAG。Ganymed,小型制药公司,核心资产是胃癌重磅新药——IMAB362。该抗体主要是通过ADCC及CDC作用杀伤癌细胞3,IMAB362在胃癌二期试验中比标准化疗显著延长生存期(13.2对8.4个月),在Claudin18.2高表达患者优势更明显(16.7对9个月)。
科济生物公布了其在研CAR-Claudin18.2T细胞治疗胃癌/胰腺癌的临床数据。接受治疗的12名患者中,8名患者经历了不同程度肿瘤消退。特别是在一个经过改良的治疗亚组中,6名患者有5名达到客观缓解(其中1名待确认客观缓解),另外1名达到完全缓解。
收藏
回复(2)参与评论
评论列表

























