肺Ca抗血管生成药物治疗策略
1、本帖只是个人对于资料和经验的整理,不具备绝对客观性,也难免有缺漏之处,希望一起交流讨论;
2、卡博至今已服用将近一年,虽未有耐药迹象,但心里确实也担心,毕竟难以确定当时卡博的起效机制,是met起效?还是v靶点起效?甚或是其他靶点?老人高龄,再次穿刺取组织做基因检测实甚折腾,因此需做好试药准备,到时可节省时间,不至于手忙脚乱;
3、本帖的靶向耐药联合抗血管生成药物的讨论尤其针对egfr相关突变类型,因为我家开始是这个突变;
一、什么是抗血管生成药物?
抗血管生成,即是抑制肿瘤血管生成,切断其营养来源,主要包含三种作用机制:
a. 使细胞外的游离Vegf蛋白失活;
b. 堵住细胞表面的Vegfr、Pdgfr、Fgfr受体,使其不能与相关游离蛋白结合;
c. 直接抑制血管内皮生成;
抗血管生成药物不仅可以导致肿瘤现有的血管系统退化以及抑制新的血管生成,同时也可正常化蜷曲的血管,使更多的药物分子进入肿瘤内部,间接提升疗效,因此即便原治疗方案耐药,联合抗血管生成药物仍有较高概率有效。
第一种作用机制代表药物是贝伐,第二种作用机制则对应于多种小分子TKI,如安罗替尼、卡博替尼、阿西替尼、乐伐替尼等等,第三种作用机制对应于恩度。
一般而言,贝伐和恩度副作用相对较小,在联合用药(联合化疗、靶向、免疫)方面应用相对广泛一些,且与小分子TKI不同,这两个的作用位点单一,因而疗效也可能相对更好。
两者区别在于,恩度可以替代贝伐应用于鳞癌或明确的中心型肿瘤等出血风险较高的肿瘤类型,因为贝伐引发出血的概率比恩度更高。

二、各小分子TKI抗血管生成药物之间的选择和轮换
这里想要讨论的小分子TKI抗血管生成药物包括安罗替尼、卡博替尼、乐伐替尼、阿西替尼、尼达尼布五种,其他如凡德他尼、索拉非尼、瑞格菲尼等等暂且按下不表。
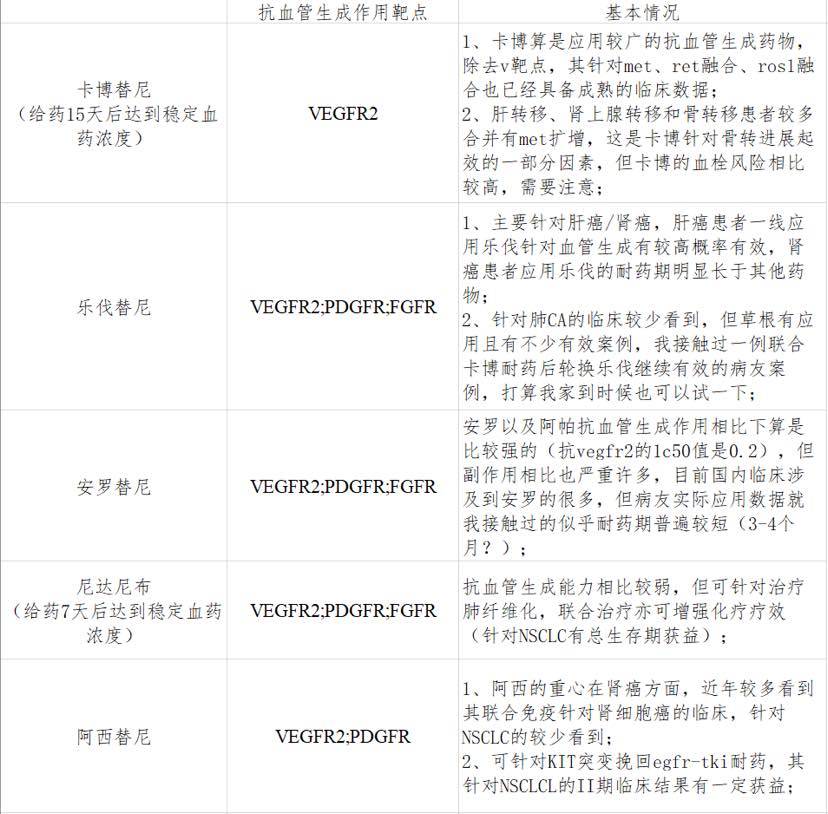
五种药物各自的基本情况如上,与贝伐不同的是,小分子TKI抗血管生成药物相对更容易耐药,因其针对的是肿瘤细胞表面的较单一受体通道,后者容易发生新的变异,或者出现新的受体通道接收信号,进而出现耐药。
各抗血管生成药物之间不存在交叉耐药现象,换言之其中一种药物耐药后换用另一种仍有较高概率有效(代入我家情况的话,卡博出现耐药后个人会先尝试met,再尝试v靶点,如果换联克唑无效,那么下一步即尝试乐伐或者轮换乐伐),且其中一种药物有无效果不与其他药物疗效直接相关。
一般而言:
1、在化疗、靶向还未完全耐药时,或者在两者以及免疫应用初期,为尽量延缓耐药时间,提升总生存期,以及提升疗效,可以联合贝伐,剂量5mg-7.5mg/kg;
2、当原化疗或靶向出现耐药时,仍可联合同等剂量贝伐,仍有较高概率有效;
3、当原靶向(需要考虑抗血管生成药物联合一般是三代92耐药的情况)出现耐药时,最好还是做下基因检测,e靶点92耐药盲试首选建议是联合met和v靶点双靶点卡博(40mg剂量),或者met活性相对更高的卡帕(150mg-250mg*2剂量)
4、在卡博有效的前提下,若是抗血管生成起效考虑,可以尝试主动轮换,因为抗血管生成药物有效的窗口期较短(肿瘤血管会恢复正常,这个正常化过程较短且可逆),因此如何有效利用这段时期可能很关键,但具体轮换方式个体性很强,我家会率先尝试与乐伐轮换;
5、安罗、卡博的抗血管生成作用相对较强,且两者同时也是广谱靶点药物,因此可以留在末线单药使用,亦有概率控制肿瘤;
三、抗血管生成药物的副作用处理
所有抗血管生成药物都有出现血压升高、血栓和出血的副作用风险,因此在使用之前需要评估血压和血栓病史,以及出血风险(上面已有提及)。
针对血压升高可以伴随服用缅沙坦控制,若效果不理想,可进一步再联合拜新同,以及及时调整用药剂量;
服用期间注意筛查凝血功能和D-二聚体,若出现纤维蛋白升高或D-二聚体升高,考虑出现高凝状态,可使用拜瑞妥或低分子肝素降低肺栓塞发生率,亦可伴随服用阿司匹林等抗凝药物提升通透度;
出血分为两种,一种需要提前预判是否能够应用抗血管生成药物,一旦出现会很危险,另一种则是黏膜出血,如牙龈、鼻腔出血,前者一般可自愈并消失,后者可用红霉素软膏涂抹鼻腔。
收藏
回复(110)参与评论
评论列表