中国卵巢上皮性癌维持治疗指南(2021年版)
中国卵巢上皮性癌维持治疗指南(2021年版)
中国抗癌协会妇科肿瘤专业委员会
卵巢恶性肿瘤是女性生殖系统常见的恶性肿瘤之一,中国人群卵巢癌新发病例为52 100 例/年,死亡达22 500例/年[1]。由于缺乏有效的早期筛查手段,患者就诊时多为晚期,中国卵巢癌患者5年生存率约为40%[2]。近年来,随着抗血管生成药物、聚腺苷二磷酸核糖聚合酶(poly ADPribose polymerase,PARP)抑制剂等靶向治疗药物的出现及相关维持治疗研究结果的公布,有效地延长了晚期患者的生存期,改变了卵巢癌的治疗策略。
为指导和规范卵巢上皮性癌的维持治疗,中国抗癌协会妇科肿瘤专业委员会(CGCS)于2020年3月发布了《中国卵巢上皮性癌维持治疗专家共识(2020)》[3]。基于多项维
持治疗临床研究数据的公布与更新,国内外维持治疗新适应证的获批,以及《卵巢上皮性癌PARP抑制剂相关生物标志物检测的中国专家共识》[4]的发布,本文将上述维持治疗
专家共识更新为指南。针对低级别浆液性及低级别子宫内膜样卵巢癌的内分泌维持治疗不在本指南探讨范围之中。
本指南采用以下推荐级别,见表1。相关推荐同样适用于输卵管癌及原发性腹膜癌。

1 卵巢癌维持治疗的定义
维持治疗是指卵巢癌完成既定的手术或化疗后达到最大限度临床缓解(完全或部分缓解)后,继续应用化疗药物或靶向药物进行的治疗,治疗的目的是延缓复发,延长
无进展生存期(progression-free survival,PFS)和总生存期(overall survival,OS)。维持治疗分为一线维持(初始治疗后)和二线及以上维持(铂敏感复发治疗后)。
2 卵巢癌维持治疗的药物概述
目前,基于临床研究证据,国内外指南曾推荐用于卵巢癌维持治疗的药物治疗方案主要包括化疗药物(紫杉醇)、抗血管生成药物、PARP抑制剂以及抗血管生成药物
与PARP抑制剂的药物组合方案。
2.1 化疗药物近20年来,拓扑替康、表柔比星、紫杉醇等化疗药物均被探索用于晚期卵巢癌一线治疗后的维持治疗,仅有紫杉醇曾短暂获得国际指南的推荐。
紫杉醇可使微管蛋白和组成微管的微管蛋白二聚体失去动态平衡,诱导与促进微管蛋白聚合、微管装配、防止解聚,从而使微管稳定并抑制癌细胞的有丝分裂和防止诱
导细胞凋亡,进而有效阻止癌细胞的增殖,起到抗癌作用。
2.2 抗血管生成药物血管内皮生长因子(vascular endothelialgrowth factor,VEGF)通过与血管内皮细胞生长因子受体(vascular endothelial growth factor receptor,VEGFR)结合,激活一系列信号传导通路,调控血管内皮细胞活化、增殖、迁移,促进肿瘤生长、侵袭和转移[5]。基于阻断肿瘤血管生成机制研发出的靶向VEGF、VEGFR和其他相关分子的药物,统称为抗血管生成药物,可分为4大类:大分子单抗类药物、竞争性受体类药物、受体酪氨酸激酶小分子抑制剂及非受体酪氨酸激酶抑制剂类小分子药物。
贝伐珠单抗是首个抗血管生成靶向药物,是一种靶向VEGF的人源化IgG1型单抗,通过结合VEGF阻止其与内皮细胞表面受体结合,抑制肿瘤新生血管的形成;此外,还可使肿瘤组织血管结构正常化,使化疗药物能够有效到达肿瘤组织,发挥协同作用[6]。培唑帕尼、索拉非尼、厄洛替尼都属于受体酪氨酸激酶小分子抑制剂,通过抑制VEGFR的酪氨酸激酶的活性来抑制肿瘤的血管形成。此外,这类药物往往还会同时作用于VEGFR之外的其他靶点[如血小板衍生生长因子受体(platelet-derived growth factor receptor,PDGFR)、成纤维细胞生长因子受体(fibroblast growth factor receptor,
FGFR)等],产生相应的生物学效应。
贝伐珠单抗、培唑帕尼、索拉非尼、厄洛替尼均被探索用于晚期卵巢癌一线治疗后的维持治疗。目前,贝伐珠单抗是唯一可用做卵巢癌一线或复发维持治疗的抗血管生
成药物。除贝伐珠单抗外,培唑帕尼也曾被推荐用于晚期卵巢癌患者的一线维持治疗。
2.3 PARP抑制剂BRCA1/2 是抑癌基因,在DNA损伤修复、细胞正常生长等方面均具有重要作用。BRCA1/2 和其他同源重组修复(homologous recombination repair,HRR)通路相关的基因突变或表观遗传学改变可抑制DNA损伤后正常修复能力,引起同源重组修复缺陷(homologous recombinationdeficiency,HRD),使DNA双链断裂不能通过HRR途径进行高保真地修复。正常情况下,细胞出现DNA单链断裂时,可依赖PARP酶通过碱基切除修复(BER)途径进行修复。当PARP抑制剂作用于肿瘤细胞时,PARP酶无法发挥作用,抑制BER导致复制叉停滞,进而形成DNA双链断裂。如果肿瘤细胞存在HRD,PARP抑制剂作用下不断形成的DNA双链断裂无法通过HRR途径得到有效修复,
两者的“合成致死”效应最终导致肿瘤细胞死亡[7-8]。
目前,国内外获批可用于卵巢癌维持治疗的PARP抑制剂包括奥拉帕利、尼拉帕利、Rucaparib,而国内仅有奥拉帕利、尼拉帕利获批维持治疗的适应证。此外,氟唑帕利以及帕米帕利在卵巢癌维持治疗中的研究正在进行。
2.4 药物组合基于有效的单药维持治疗,上述药物的组合方案也被探索用于晚期卵巢癌的维持治疗,如抗血管生成药物联合PARP抑制剂。2020年5月,美国食品药品监督管理局(Food and Drug Administration,FDA)批准贝伐珠单抗联合奥拉帕利用于存在HRD且一线含铂化疗过程中联合使用贝伐珠单抗晚期卵巢癌患者的维持治疗。
除上述涉及的维持治疗药物,目前仍有多种药物及药物组合方案正被积极探索用于卵巢癌的维持治疗,如CA125单克隆抗体、贝伐珠单抗/免疫检查点抑制剂/PARP抑制剂三联药物组合方案等。
3 基因检测在卵巢癌维持治疗中的应用
在新诊断晚期卵巢癌中,BRCA1/2 和HRD检测被推荐用于指导卵巢癌一线维持治疗的方案选择[9-10]。与HRD阴性相比,存在BRCA1/2 突变或HRD阳性的卵巢癌患者可更加获益于PARP抑制剂单药以及与贝伐珠单抗联合的双药维持治疗,约50%的高级别浆液性卵巢癌存在HRD。而对于铂敏感复发的卵巢癌患者,BRCA1/2 突变及HRD状态并不作为含铂化疗后PARP抑制剂维持治疗的选择标准,但对于患者疗效预测及预后判断具有一定参考价值。目前,尚无明确的疗效预测生物标志物可以指导贝伐珠单抗的临床应用。
鉴于生物标志物在卵巢癌维持治疗临床实践中的关键指导作用,《卵巢上皮性癌PARP抑制剂相关生物标志物检测的中国专家共识》对相关生物标志物检测进行如下推荐[4]:(1)推荐所有非黏液性卵巢癌患者在初次病理确诊时,明确肿瘤BRCA1/2 的突变(包括胚系和体细胞突变)状态,对于Ⅰ期患者仅需明确胚系BRCA1/2 突变状态(1类)。
(2)对于新诊断的晚期卵巢癌患者(目前主要证据在高级别浆液性卵巢癌和高级别子宫内膜样癌),HRD状态(包括BRCA1/2 和HRD score)有助于医生选择不同维持治疗方案以期达到最佳治疗效果:①建议进行HRD 检测(包括BRCA1/2 和HRD score)(2A类);如患者存在抗血管生成药物治疗的禁忌证,或不考虑抗血管生成药物治疗时,HRD状态对于维持治疗的疗效预测及预后判断仍有参考价值(2B类);②如既往接受过肿瘤BRCA1/2 检测,且结果为阳性,不需要再补充进行HRD检测(1类);③如既往接受过肿瘤BRCA1/2 检测,且结果为阴性,建议对肿瘤样本进行HRD检测以明确是否为HRD阳性(2A类)。(3)PARP抑制剂对于铂类敏感复发的卵巢癌患者,BRCA1/2 突变状态及HRD状态并不作为含铂化疗后PARP抑制剂维持治疗的选择标准,但对于患者疗效预测及预后判断具有一定参考价值。
4 卵巢癌维持治疗的策略
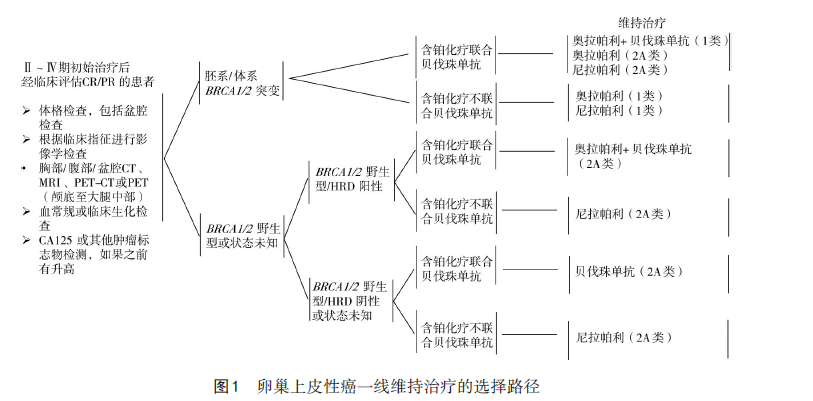
4.1 一线维持治疗卵巢癌一线维持治疗是指对完成初始化疗达到临床完全缓解(CR)或部分缓解(PR)的患者给予后续治疗,旨在推迟复发,改善生存预后。基于循证医学证据,目前用于一线维持治疗的药物主要包括抗血管生成药物和PARP抑制剂。针对考虑接受一线维持治疗的晚期卵巢上皮性癌患者,具体维持治疗的选择可参考图1。
4.1.1 化疗药物既往2 项Ⅲ期临床研究(SWOG-GOG178和After-6 Protocol)探索了铂类联合紫杉醇一线化疗结束后继续使用紫杉醇单药维持治疗能否使患者获益。SWOG-GOG 178研究提示,在Ⅲ~Ⅳ期卵巢癌患者结束了铂类联合紫杉醇一线化疗后,12个周期紫杉醇单药维持治疗的PFS显著优于3个周期紫杉醇单药维持(mPFS 28个月vs. 21个月,P=0.0035),但OS差异无统计学意义[11]。然而,另一项After-6 Protocol研究中ⅡB~Ⅳ期卵巢癌患者在6个周期紫杉醇+铂一线化疗后,继续进行6个周期紫杉醇单药维持并未延长CR 患者的PFS 或OS[12]。基于SWOGGOG178研究最初PFS获益的证据,NCCN曾推荐紫杉醇单药用作晚期卵巢上皮性癌的维持治疗。但随着更多抗血管生成药物以及PARP抑制剂的出现,以及该研究更长时间的随访显示仅有PFS获益而无OS改善,且该方案与周围神经病变及更差的生活质量相关后,目前不再被推荐用于卵巢癌的维持治疗[13]。而拓扑替康等其他药物的换药维持治疗研究,均未显示出PFS获益。
4.1.2 抗血管生成药物贝伐珠单抗、培唑帕尼、索拉非尼、厄洛替尼等均探索用于晚期卵巢癌一线治疗后的维持治疗,目前仅贝伐珠单抗在FDA和欧洲药品管理局(European Medicines Agency,EMA)获批可用作卵巢癌的维持治疗。
4.1.2.1 贝伐珠单抗两项随机对照临床试验旨在研究卵巢癌初始化疗联合贝伐珠单抗治疗并在化疗结束后序贯贝伐珠单抗维持治疗的有效性和安全性。ICON7 研究2011年公布最初研究结果显示,与单化疗组相比,化疗联合贝伐珠单抗+贝伐珠单抗维持治疗组患者进展或死亡风险降低13%(mPFS 19.8个月vs. 17.4个月;HR 0.87,95%CI0.77~0.99);高风险亚组(包括Ⅳ期和未行手术及手术未达无肉眼可见残余癌灶即R0的Ⅲ期)患者进展或死亡风险降低27%(mPFS 16个月vs. 10.5个月;HR 0.73,95%CI 0.60~0.93)[14]。2015年ICON7研究公布最终结果,总人群中位OS 差异无统计学意义(mOS 58.0 个月vs. 58.6 个月;HR0.99,95%CI 0.85~1.14),但其中高风险亚组患者死亡风险可降低22%(mOS 39.7 个月vs. 30.2 个月,HR 0.78,95%CI 0.63~0.97)[15]。值得注意的是,在ICON7研究中观察到非等比例风险效应(即药物治疗效应会随时间发生变化),采用限制性平均生存时间进行分析,得出的结论趋势仍然是一致的。
GOG218研究纳入Ⅳ期和未手术或未达R0的Ⅲ期高危卵巢癌患者,2011年最初结果显示与对照组(单纯化疗组)相比,化疗联合贝伐珠单抗+贝伐珠单抗维持治疗组患者疾病进展或死亡风险降低28.3%(mPFS 14.1个月vs. 10.3个月;HR 0.717,95%CI 0.625~0.824)[16]。2019 年公布了GOG218研究最终结果,两组患者中位OS比较差异无统计学意义(mOS 43.4个月vs. 41.1个月;HR 0.96;95%CI 0.85~1.09)[17]。
4.1.2.2 培唑帕尼AGO-OVAR16是一项Ⅲ期随机试验,探索培唑帕尼用于一线治疗后疾病未进展的Ⅱ~Ⅳ期卵巢上皮性癌,输卵管癌或原发性腹膜癌患者的维持治疗。结果显示,与安慰剂相比,培唑帕尼组患者疾病进展或死亡风险降低23%(mPFS 17.9 个月vs. 12.3 个月;HR 0.77,95%CI 0.64~0.91),但总生存率没有改善,培唑帕尼组的不良反应发生增加,如3/4级高血压[18]。而针对东亚人群的亚组分析表明,相比安慰剂治疗,接受培唑帕尼治疗的东亚人群PFS更短[19]。
索拉非尼、厄洛替尼被探索用于新诊断卵巢上皮性癌、输卵管癌或原发性腹膜癌患者化疗后的维持治疗,均未带来PFS的显著改善。
4.1.3 PARP抑制剂
4.1.3.1 奥拉帕利在SOLO1研究中,携带胚系或体细胞BRCA1/2 突变的晚期卵巢上皮性癌患者在一线含铂化疗缓解(CR/PR)后接受奥拉帕利或安慰剂维持治疗2年,中位随访40.7个月,奥拉帕利组患者复发或死亡风险下降70%(mPFS 未达到vs. 13.8 个月;HR 0.30,95%CI 0.23~0.41)[20]。2020 年欧洲肿瘤内科学会(European Society forMedical Oncology,ESMO)更新了SOLO1长期随访数据,随访至最后1例患者随机后5年,奥拉帕利组中位PFS 达到56.0个月,而中位治疗时间仅24.6个月[21]。中国亦参与了此项研究,中国队列的疗效和安全性数据与全球数据基本一致。
4.1.3.2 尼拉帕利PRIMA研究是一项在晚期卵巢上皮性癌一线含铂化疗缓解后对比尼拉帕利与安慰剂维持治疗的Ⅲ期随机对照研究。该研究与SOLO1研究主要的不同点在于纳入的是具有高复发风险的患者,无论BRCA 突变状态如何均可入组,HRD状态为随机分层因素,并且维持治疗期限从SOLO1的2年增加到3年。在HRD阳性患者中,尼拉帕利组较安慰剂组降低57%的疾病进展或死亡风险(mPFS 21.9 个月vs. 10.4 个月;HR 0.43,95%CI 0.31~0.59)。在总体人群中,尼拉帕利组较安慰剂组降低38%的疾病进展或死亡风险(mPFS 13.8 个月vs. 8.2 个月;HR0.62,95%CI 0.50~0.76)。同时,在生物标志物不同的亚组分析中,均可看到尼拉帕利组有不同程度获益,HRD阴性患者仍有获益(mPFS 8.1个月vs. 5.4个月;HR 0.68,95%CI0.49~0.94)。该研究支持尼拉帕利用于所有卵巢上皮性癌的一线维持治疗,即使是没有BRCA 突变或HRD阴性的患者,但其获益程度不如生物标志物阳性的患者[22]。
4.1.4 抗血管生成药物+PARP抑制剂如何进一步提高PARP抑制剂的疗效并扩大PARP抑制剂获益人群是目前的研究热点。研究者正在探索不同的联合方案,如联合抗血管生成药物、免疫检查点抑制剂和DNA损伤修复通路抑制剂等。
4.1.4.1 贝伐珠单抗+奥拉帕利PAOLA-1研究是一项在新诊断的晚期卵巢癌患者中开展的Ⅲ期随机对照临床试验,旨在对比奥拉帕利(2年)联合贝伐珠单抗(15个月)维持治疗对比贝伐珠单抗单药维持治疗的疗效与安全性[23]。
与贝伐珠单抗单药相比,奥拉帕利联合贝伐珠单抗治疗使BRCA 突变患者复发或死亡风险降低69%(mPFS 37.2个月vs. 21.7 个月;HR 0.31,95%CI 0.20~0.47);BRCA 野生型/HRD阳性患者复发或死亡风险降低57%(mPFS 28.1个月vs. 16.6 个月;HR 0.43,95%CI 0.28~0.66);BRCA 野生型/HRD阴性/未知患者复发或死亡风险在两组间无显著差异(mPFS 16.9 个月vs. 16.0 个月;HR 0.92,95%CI 0.72 ~1.17)。联合用药组与贝伐珠单抗治疗组≥3级不良事件发生率分别为57%与51%,其中联合用药组血液学不良反应以及乏力、虚弱与恶心的发生率高于贝伐珠单抗单药组,而高血压的发生率低于单药组。研究表明,奥拉帕利联合贝伐珠单抗维持治疗可使BRCA 突变或HRD阳性患者获益。
4.1.4.2 贝伐珠单抗+尼拉帕利OVARIO 研究是一项针对晚期卵巢癌一线含铂化疗联合贝伐珠单抗后,尼拉帕利联合贝伐珠单抗维持治疗的Ⅱ期单臂临床研究。共入组105例患者,63%的患者接受新辅助化疗,28%的患者携带BRCA 突变,47%的患者为HRD阳性,采用个体化起始剂量给药,78%患者的起始剂量为200 mg。6个月时PFS率为89.5%,12个月时PFS率为75%,18个月时PFS率为62%。77% 患者出现≥3 级治疗期间出现的不良事件(treatmentemergent adverse event,TEAE),73%患者因为TEAE需要进一步减量,27%患者因为TEAE退出治疗[24]。
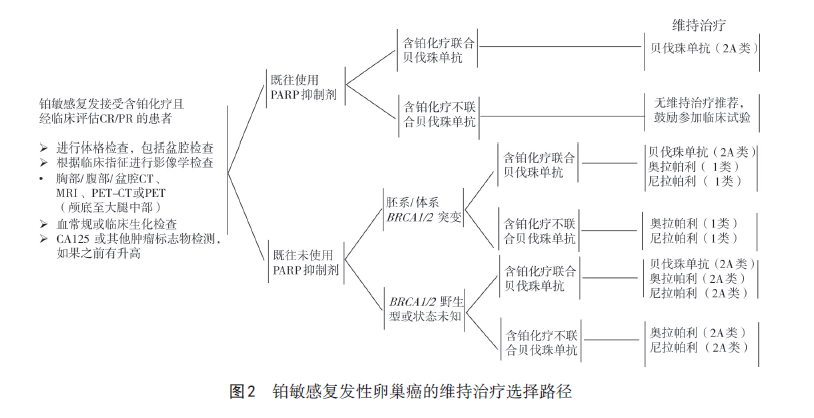
4.2 铂敏感复发维持治疗卵巢癌复发分为铂敏感复发和铂耐药复发,前者指化疗结束后6个月及以上的复发,后者指化疗结束后6个月内的复发。铂敏感复发患者的系统性治疗原则是首选以铂类为基础的联合化疗或联合贝伐珠单抗,再予以PARP抑制剂或贝伐珠单抗维持治疗,以推迟再次复发时间或降低复发风险。目前,不推荐既往使用过PARP抑制剂的患者再次使用PARP抑制剂。对于考虑接受维持治疗的铂敏感复发患者,具体的维持治疗选择推荐可参考图2。
4.2.1 抗血管生成药物2 项Ⅲ期随机对照临床试验OCEANS研究(吉西他滨+卡铂±贝伐珠单抗)和GOG213研究(紫杉醇+卡铂±贝伐珠单抗)均证实化疗联合贝伐珠单抗相比单纯含铂化疗,能够显著延长铂敏感复发卵巢癌的无进展生存期。OCEANS研究中,贝伐珠单抗联合治疗方案能够降低患者51.6%疾病进展或死亡风险(mPFS 12.4个月vs. 8.4个月;HR 0.484,95%CI 0.388~0.605),而中位OS无显著改善(mOS 33.6个月vs. 32.9个月;HR 0.952,95%CI0.771~1.176)[25]。同样,GOG213研究中,贝伐珠单抗联合方案能够降低37.2%的疾病进展或死亡风险(mPFS 13.8个月vs. 10.4 个月;HR 0.628,95%CI 0.534~0.739),而中位OS亦无显著统计学差异(mOS 42.2个月vs. 37.3个月;HR0.829,95%CI 0.683~1.005)[26]。上述两项研究表明贝伐珠单抗与含铂化疗联用并序贯维持能够显著延长铂敏感复发性卵巢癌的PFS,但OS无显著获益。
对于一线使用贝伐珠单抗进展后是否依然可以使用贝伐珠单抗的问题在MITO16b研究中得到解答。该研究纳入一线使用贝伐珠单抗的铂敏感复发卵巢癌患者,分为单纯化疗对照组及贝伐珠单抗联合化疗+贝伐珠单抗序贯治疗组。结果显示与单纯化疗对照组相比,贝伐珠单抗联合化疗+贝伐珠单抗序贯治疗组可降低患者49%疾病进展或死亡风险(mPFS 11.8 个月vs. 8.8 个月;HR 0.51,95%CI0.41~0.65)。该研究表明既往一线使用过贝伐珠单抗的铂敏感复发卵巢癌患者在传统化疗的基础上继续使用贝伐珠单抗,可延长患者的无进展生存期[27]。
4.2.2 PARP抑制剂
4.2.2.1 奥拉帕利Study 19是一项Ⅱ期随机安慰剂对照研究,入选了经铂类再治获得缓解的铂敏感复发卵巢癌患者,而对患者的BRCA1/2 突变状态未做要求[28]。该研究证实相比安慰剂,奥拉帕利维持治疗能够降低全人群65%的疾病进展或死亡风险(研究者评估,mPFS 8.4个月vs. 4.8个月;HR 0.35,95%CI 0.25~0.49),其中BRCA 突变患者的获益更为显著,与对照组相比,奥拉帕利维持治疗可降低BRCA 突变患者82%的疾病进展或死亡风险(研究者评估,mPFS 11.2个月vs. 4.3个月;HR 0.18,95%CI 0.10~0.31)。SOLO2研究是一项Ⅲ期随机对照临床研究,入选了携带有BRCA 突变的铂敏感复发卵巢癌患者,在含铂化疗缓解后随机接受PARP抑制剂维持治疗或安慰剂治疗[29-30]。
该研究显示,与安慰组相比,奥拉帕利维持治疗能够降低70%的疾病进展或死亡风险(研究者评估,mPFS 19.1个月vs. 5.5 个月;HR 0.30,95%CI 0.22~0.41)。2020 ASCO 报道了SOLO2 最终OS分析结果,证实即使安慰剂组38%的患者出现了交叉治疗,奥拉帕利维持治疗仍可延长中位OS 12.9个月,降低死亡风险26%(mOS 51.7个月vs. 38.8个月;HR 0.74,95%CI 0.54~1.00);剔除安慰剂组交叉部分患者数据后,奥拉帕利组中位OS获益提升到16.3个月。
OPINION 研究是一项针对既往接受过二线及以上含铂化疗的non-gBRCA 突变铂敏感复发患者采用奥拉帕利单药维持治疗的单臂、ⅢB期研究[31]。截至2019年11月15日有152个PFS事件,数据成熟度54%,结果(研究者评估)显示奥拉帕利单药维持治疗组患者中位PFS 为9.2 个月(95%CI 7.6~10.9)。亚组分析提示不论HRD状态均能获益,其中HRD阳性包含sBRCA 突变组中位PFS为10.9个月(95%CI 9.1~14.5),HRD阳性排除sBRCA 突变组中位PFS为9.7个月(95%CI 8.1~11.1),HRD阴性组中位PFS为7.3个月(95%CI 5.5~9.1)。该研究进一步证实了奥拉帕利为胚系BRCA 突变阴性患者也能带来显著临床获益。
4.2.2.2 尼拉帕利NOVA研究为针对铂敏感复发患者的Ⅲ期随机对照研究,结果显示与对照组相比,尼拉帕利维持治疗可降低gBRCA 胚系突变患者73%的疾病进展或死亡风险(独立盲法评估,mPFS 21个月vs. 5.5个月;HR 0.27,95%CI 0.17~0.41);对于gBRCA 野生型患者,尼拉帕利维持治疗可降低55% 的疾病进展或死亡风险(独立盲法评估,mPFS 9.3 个月vs. 3.9 个月;HR 0.45,95%CI 0.34~0.61);对于gBRCA 野生型/HRD阳性患者,尼拉帕利维持治疗可降低62% 的疾病进展或死亡风险(独立盲法评估,mPFS 12.9 个月vs. 3.8 个月;HR 0.38,95%CI 0.24~0.59)[32]。NORA研究[33]是目前报道的首个在中国铂敏感复发患者中采用尼拉帕利个体化起始剂量的Ⅲ期研究。结果显示在总人群中,与对照组相比,尼拉帕利维持治疗可降低68%的疾病进展或死亡风险(独立盲法评估,mPFS 18.3个月vs. 5.4 个月;HR 0.32,95%CI 0.23~0.45)。其中对于gBRCA 突变患者,尼拉帕利维持治疗可降低78%的疾病进展或死亡风险(独立盲法评估,mPFS 未达到vs. 5.5个月;HR 0.22,95%CI 0.12~0.39);对于gBRCA 野生型患者,尼拉帕利维持治疗可降低60%的疾病进展或死亡风险(独立盲法评估,mPFS 11.1 个月vs. 3.9 个月;HR 0.40,95%CI0.26~0.61)。
4.2.2.3 Rucaparib ARIEL3研究显示对于铂敏感复发患者,与对照组相比,Rucaparib维持治疗可降低64%的疾病进展或死亡风险(研究者评估,mPFS 10.8个月vs. 5.4个月;HR 0.36,95%CI 0.30~0.45)[34]。亚组分析显示对于BRCA突变患者,Rucaparib维持治疗可降低77%的疾病进展或死亡风险(研究者评估,mPFS 16.6个月vs. 5.4个月,HR 0.23,95%CI 0.16~0.34);对于BRCA 野生型HRD阳性患者,Rucaparib维持治疗可降低56%的进展或死亡风险(研究者评估,mPFS 9.7个月vs. 5.4个月;HR 0.44,95%CI 0.29~0.66)。
4.2.2.4 氟唑帕利FZOCUS-2研究是在中国铂敏感复发
患者中开展的一项Ⅲ期随机对照研究。2021年SGO会议上报道的中期分析结果显示,与对照组相比,氟唑帕利维持治疗能够降低75%的疾病进展或死亡风险(独立盲法评估,mPFS 12.9 个月vs. 5.5 个月;HR 0.25,95%CI 0.17~0.36)[35]。其中对于gBRCA 突变患者,氟唑帕利维持治疗可降低86% 的疾病进展或死亡风险(HR 0.14,95%CI 0.07~0.28);对于gBRCA 野生型患者,氟唑帕利维持治疗可降低54%的疾病进展或死亡风险(HR 0.46,95%CI 0.29~0.74)。
4.2.2.5 PARP 抑制剂再使用(PARPi after PARPi) 对于既往使用过PARP抑制剂的患者,在疾病进展后是否可以继续使用PARP 抑制剂是目前临床热点问题。一项小样本、回顾性研究显示22例既往接受过PARP抑制剂治疗/维持治疗的卵巢癌复发患者再次使用PARP抑制剂治疗/维持治疗,有3例患者达到部分缓解,其中,在接受PARP抑制剂治疗过程中进展的8例患者中,再次接受PARP抑制剂治疗的最佳疗效仅为SD(5/8)[36]。目前正在开展的OReO研究是一项ⅢB期、随机、对照研究,旨在评估卵巢癌患者在既往接受PARP抑制剂维持治疗进展后,再次接受含铂化疗并获得缓解后,继续使用奥拉帕利维持治疗的疗效与安全性[37]。基于目前有限的数据,不推荐PARP抑制剂再次使用。
收藏
回复(8)举报
参与评论
评论列表
按投票顺序
 πD
πD这篇指南,还有最后一部分是不良反应管理方面,鉴于我以前整理过此类内容,没再放,字太多了,我复制太费劲了 鉴于现在都维持治疗,但是每个人维持的药物不一样,选择自己需要的内容查看即可。
有需要全文的可以百度查看原文。
鉴于现在都维持治疗,但是每个人维持的药物不一样,选择自己需要的内容查看即可。
有需要全文的可以百度查看原文。
举报
2022-01-11 15:18:49 有用(1)
回复(2)
姐,我透明3A的,在术后第三次化疗的时候加用了贝伐,结疗后也继续贝伐维持治疗,现在化疗结疗一个多月,今天复查Ca125 32(上个月24),HE4 98(上个月78),是复发了吗?好担心啊

举报
2022-02-06 20:10:37 有用(0)
回复(2)
他们吹嘘的神药差点要了我老婆的命,他们眼里一无是处的药却救了我老婆的命!
举报
2022-01-14 18:15:16 有用(0)
回复(0)
 醉了3375
醉了3375复发了只能挨个方案试,不同的人适合不同的方案,只要有效对自己来说这个方案就是合适的!
举报
2022-07-21 10:59:41 有用(0)
回复(0)
相关推荐
热点推荐
2013-11-19 14:23:04
爸爸确诊病情已经有11个多月了。一共做了8次大化疗,2次小化疗,以及35次放疗,上月返医院检查“瘤子”没有了。这一路走来,有多少的艰辛与泪水。在这里与大家分享爸爸的治疗过程。起初,拿到病例报告的时候,
2013-11-19 14:31:01
妈妈患肺癌已经有三年了,这三年来一直在接受治疗到现在,下面是妈妈检查以及治疗的过程。2010年10月,妈妈体检出肺癌IV期,纵隔淋巴转移,肝部转移,去省肿瘤医院复查,做了PET-CT,结果一样,省肿瘤
2013-11-19 15:04:43
2011年11月,妈妈被诊断肺癌,我在网上浏览了很多帖子,学到了很多,看到了一批又一批共同奋斗在抗癌战线上的战友。这15个月走下来,越来越体会到抗癌之路的艰辛,今天发个帖子,记录一下妈妈的治疗经过,也
























