强强联合,提高肿瘤免疫治疗疗效丨临床招募
近年来,随着肿瘤学与免疫学的不断发展与深入,肿瘤免疫治疗已经成为抗肿瘤领域最前沿的癌症治疗手段。免疫治疗如免疫检查点抑制剂(PD-1/PD-L1)的获批为临床医生与患者带来抗癌新希望。
同样,也有越来越多的证据显示新生血管生成在多种实体肿瘤的生长、增殖和转移中发挥着关键作用。抗血管生成药物可通过靶向作用于血管内皮生长因子(VEGF)等信号因子,抑制其过度表达,促进肿瘤血管正常化。
因此,抗血管生成与免疫治疗联合应用,一方面,可以通过阻断VEGF通路实现血管正常化,并使淋巴细胞更多的传输到肿瘤部位;另一方面,还可以解除对肿瘤微环境的抑制作用,以便达到更好的疗效。
2018年,帕博利珠单抗(Keytruda,简称“K药”)在我国获批上市,首个获批的适应症是用于治疗一线治疗失败的不可切除或转移性黑色素瘤患者。
2019年,仅8个月的时间内,K药接连斩获三个晚期非小细胞肺癌(NSCLC)一线治疗适应症,堪称“适应症收割机”。
不仅如此,KEYNOTE-001的五年随访数据显示,对比化疗时代,晚期非小细胞肺癌五年生存率仅有6%,而帕博利珠单抗(Keytruda,简称“K药”)单药治疗初治的晚期非小细胞肺癌患者五年生存率达到了23.3%。免疫治疗大大延长了晚期肺癌患者的生存期。
仑伐替尼是一个多靶点的口服RTK抑制剂,它能参与抑制肿瘤增殖的其他促血管生成和致癌信号通路相关RTK,还能够选择性抑制血管内皮生长因子( VEGF)受体和成纤维生长因子(FGF )受体的激酶活性。
“可乐组合”(帕博利珠单抗 仑伐替尼),PD-1抑制剂 多靶点抗血管生成药物可谓是“强强联合”,屡屡展现出“1 1大于2”的惊艳疗效。多个会议上都给出了“可乐组合”在各个癌种的给力数据。
“可乐组合“一线治疗不可切除的肝癌患者的临床研究(KEYNOTE-524/Study116)显示:
总体客观缓解率(ORR)为42.3%(11/26),剂量扩大组(20例)中有效率ORR达到35%,控制率更是高达100%,创下满分新高!
在2019年ESMO会议上,该联合方案更新了临床数据:在可评估的67位患者中,ORR高达44.8%,总生存期(OS)达到了史无前例的20.4个月,6%的患者肿瘤完全消失(CR),创下了肝癌治疗新历史。
正式基于“可乐组合”在肝癌领域耀眼的数据,2019年9月,“帕博利珠单抗 仑伐替尼”获FDA授予一线治疗晚期肝癌的突破性疗法认定。
在2018年的ASCO会议上,研究人员更新了“可乐组合”针对肾细胞癌的临床数据。临床设计招募30名晚期肾癌,包括未经过系统治疗的12位患者,和经过1-2次系统治疗的18位患者;具体的联合方案:仑伐替尼的剂量是每天20mg或24mg,帕博利珠单抗是200mg三周一次。
在所有30位患者中,21位肿瘤明显缩小,有效率高达70%;还有8位患者肿瘤稳定不长大,疾病控制率96.7%。也就是说,30位患者中,只有一位患者的肿瘤增大,其余29位患者都得到了有效的控制!
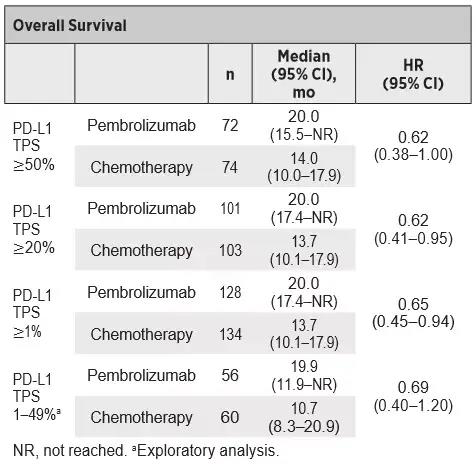
2019年,WCLC会议上帕博利珠单抗公布了单药一线治疗非小细胞肺癌(NSCLC)的中国研究数据,研究结果显示:中位随访11.3个月后,在262例无EGFR/ALK敏感突变但PD-L1 TPS≥1%的局部晚期/转移性NSCLC患者中,与基于铂的化疗相比,帕博利珠单抗均改善了晚期肺癌患者的OS。
具体数据如下:
PD-L1 TPS≥50%患者的OS分别为:20.0个月 vs 14.0个月(帕博利珠单抗单药一线治疗对比化疗);
PD-L1 TPS≥20%患者的OS分别为:20.0 个月 vs 13.7个月;
PD-L1 TPS≥1%患者的OS分别为:20.0个月 vs 13.7个月。
目前,帕博利珠单抗在肺癌领域已经先后获批联合化疗一线治疗非鳞状NSCLC、单药一线治疗PD-L1表达阳性(TPS≥1%)NSCLC、以及联合化疗一线治疗转移性鳞状NSCLC(肺鳞癌)共三个一线适应症。
而帕博利珠单抗并未止步于此,在已有免疫单药保底的情况下,帕博利珠单抗联合仑伐替尼进行了一项1b/2期研究,试验纳入了21例晚期NSCLC患者,接受仑伐替尼20mg/天 帕博利珠单抗200mg/三周治疗。
LEAP-007是一项帕博利珠单抗联合或不联合仑伐替尼治疗的3期随机双盲试验,试验受试者为肿瘤比例评分(TPS)大于或等于 1%的初治转移性非小细胞肺癌患者。
对肺癌临床研究LEAP-007有意者,可扫描图片中的二维码了解项目详情。

国内多家医院正在为这项研究招募患者,项目简介如下。
1.试验药物简介
本试验的适应症是TPS大于或等于1%的初治转移性NSCLC。
2.试验目的
评估帕博利珠单抗(MK-3475)联合仑伐替尼(MK-7902 / E7080)与帕博利珠单抗联合仑伐替尼匹配安慰剂治疗未接受针对转移性疾病的系统治疗、程序性细胞死亡配体1(PD-L1)肿瘤比例得分(TPS)大于或等于1%、且无EGFR或ALK/ROS1靶向治疗指征的初治成年转移性非小细胞肺癌(NSCLC)受试者的安全性和有效性
3.试验设计
试验分类:安全性和有效性
试验分期:III期
设计类型:平行分组
随机化:随机化
盲法:双盲
试验范围:国际多中心试验
试验人数:总体620人,中国待定人
4. 入选标准
1 组织学或细胞学确诊非小细胞肺癌(NSCLC)
2 根据美国癌症联合委员会[AJCC]第8版分期为IV期NSCLC
3确认不存在EGFR-、ALK-或ROS1-相关突变指示应以靶向治疗为主要治疗
4根据RECIST 1.1确定有可测量病灶
5能够提交组织样本至中心实验室,使用IHC 22C3 pharmDx评估,证实肿瘤组织的肿瘤细胞PD-L1表达≥1%(TPS≥1%)
6在签署知情同意书时年满18岁
7 预期寿命不少于3个月
8在首次给予研究治疗前7日内、随机分组之前,美国东部肿瘤协作组(ECOG)体能状态评分为0或1分
9 男性受试者必须在治疗期间以及最后一次仑伐替尼/安慰剂给药后至少30天同意以下内容:1)停止以异性性交作为首选日常生活方式(长期持续禁欲),并同意保持禁欲状态或 2)必须同意使用研究允许的避孕方式,除非确认为无精症(输精管切除或继发于医学原因)。仑伐替尼/安慰剂停止给药30天后,仍在接受帕博利珠单抗单药治疗的男性患者无需采取避孕措施
10女性受试者必须不处于妊娠期或哺乳期,且至少符合以下条件之一:1)不是具有生育能力的女性(WOCBP);2)是WOCBP,从治疗期间到最后一次帕博利珠单抗给药后至少120天,或最后一次仑伐替尼/安慰剂给药后至少30天,以后发生者为准,采用一种对使用者依赖性低的高效避孕方法(每年失败率<1%),或停止以异性性交作为首选日常生活方式(长期持续禁欲)
11在使用或未使用抗高血压药物的情况下血压(BP)控制充分,定义为BP≤150/90 mmHg并且在随机分组之前1周内抗高血压药物保持不变
12方案定义的充分器官功能,检测样本须在开始研究治疗前10天内采集
5.排除标准
1已知存在未经治疗的中枢神经系统转移和/或脑膜转移癌
2 在研究治疗第一次给药前2周内发生具有临床意义的咯血(至少0.5茶匙鲜血)或肿瘤出血
3大血管侵犯/浸润的影像学证据
4存在其他恶性肿瘤的已知病史,除非受试者已接受潜在根治性治疗,且治疗后至少3年无疾病复发证据(该时间要求不适用于已成功根治性切除的皮肤基底细胞癌、浅表性膀胱癌、皮肤鳞状细胞癌、原位宫颈癌或其他原位癌)
5 患有活动性自身免疫性疾病,且在过去2年中需要全身治疗。激素替代治疗(例如,甲状腺素、胰岛素或因肾上腺或垂体功能不全而使用的生理性皮质类固醇替代治疗等)不被视作全身治疗,允许使用
6已进行了异体组织/实体器官移植
7已知的人类免疫缺陷病毒(HIV)感染病史
8 需类固醇全身用药的肺炎(非感染性)病史或现患有间质性肺炎/间质性肺病
9 已知乙型肝炎病史(定义为乙型肝炎表面抗原[HBsAg]阳性或检测到乙型肝炎病毒[HBV-DNA])或已知的活动性丙型肝炎病毒(HCV,定义为检出HCV-RNA[定性]或HCV抗体阳性)感染
10研究者认为可能影响口服研究药物吸收的胃肠道病史或手术史
11研究治疗第一次给药前12个月内发生重大心血管疾病,例如纽约心脏协会II级以上的充血性心力衰竭病史、不稳定型心绞痛、心肌梗死或脑血管意外(CVA)/卒中,或与血流动力学不稳定相关的心律失常
12在开始治疗之前,尚未从任何大手术的损伤和/或并发症中充分恢复
13 已知的活动性结核病史(TB)
14 患有需全身治疗的活动性感染
15 会干扰受试者配合研究要求能力的已知精神疾病或药物滥用障碍
16 既往对mAb治疗严重过敏或已知对仑伐替尼或帕博利珠单抗的任何成分过敏或不耐受
17 首次研究干预开始前24小时内尿妊娠试验阳性的WOCBP。如果尿液检查结果为阳性或无法确认为阴性,则需要进行血清妊娠试验
18 既往已接受过针对转移性NSCLC的全身化疗或其他靶向或生物抗肿瘤治疗
19 既往接受过抗PD-1、抗-PD-L1或抗PD-L2药物治疗或作用于另一种刺激信号或协同抑制T细胞受体的药物(例如CTLA-4、OX 40、CD137)治疗,或者接受过仑伐替尼单药治疗或仑伐替尼联合抗PD-1药物治疗
20研究治疗首次给药前14天内曾接受放疗,或在研究治疗首次给药前6个月内曾接受>30 Gy的肺部放疗(受试者必须从所有放射相关毒性中恢复至1级或以下、无需接受皮质类固醇治疗并且从未发生放射性肺炎)
21诊断为免疫缺陷或研究治疗第一次给药前7天内正在接受任何形式的免疫抑制治疗
22在第一次研究治疗前7天内接受全身类固醇治疗(日剂量超过10 mg泼尼松当量)
23在第一次研究干预前30天内接种过活疫苗
24 尿试纸检测/尿液分析蛋白尿>1 的受试者将接受24小时尿液收集以定量评估蛋白尿。尿蛋白≥1g/24 h不可入组
25 QTc间期延长至>480 ms和/或多门控采集扫描(MUGA)或超声心动图(ECHO)测定的左心室射血分数(LVEF)低于机构正常范围
26 在第一次研究干预前3周内进行过大手术。注意:大型手术后必须对伤口是否充分愈合进行临床评估,与入组资格要求时间窗无关
27 既往已出现CTCAE 3级及以上胃肠道或非胃肠道瘘
28治疗研究者认为既往或当前存在可能干扰本研究结果,影响受试者在整个研究过程中的参与情况,或表明参与研究不能给受试者带来最大利益的疾病、治疗或实验室检查异常
6. 医院和研究者信息
主要研究者信息

各参加机构信息
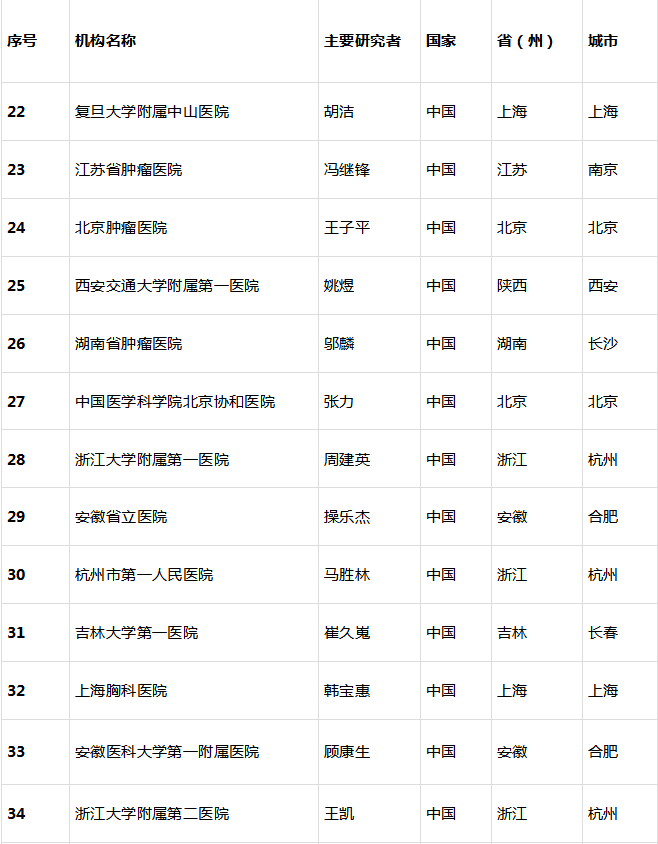
参考来源:
[1]Makker V, Rasco DW, Vogelzang NJ, et al. Lenvatinib pembrolizumab in patients with advanced endometrial cancer: updated results. J Clin Oncol. 2018;36 (suppl; abstr 5596).
[2]Makker V, Rasco D, Vogelzang NJ, et al. Lenvatinib plus pembrolizumab in patients with advanced endometrial cancer: an interim analysis of a multicentre, open-label, single-arm, phase 2 trial. Lancet Oncology. 2019;20(5):711-718. doi: 10.1016/S1470-2045(19)30020-8.
[3]747P-Aphase Ib trial of lenvatinib(LEN)plus pembrolizumab (PEMBRO) in unresectable hepatocellular carcinoma(uHCC):Updated results.
相关资讯