乳腺癌复发转移了,用DS-8201后,幸好还有这些药能用!她的癌细胞很多都被消灭了!
最近有姐妹问,如果用了DS-8201(德曲妥珠单抗)后出现耐药,还有其他治疗选择吗?今天互助君就结合最新的研究进展,来聊聊DS-8201耐药的相关问题,希望能为大家提供一些参考和帮助。

图源:乳腺癌互助圈社群
01
DS-8201是一种靶向HER2的新型抗体药物偶联物,适用于HER2阳性和低表达乳腺癌。尽管疗效显著,但仍有部分患者对其不敏感或在治疗后出现耐药,表现为肿瘤先缩小后再生长,提示药物效果逐渐减弱甚至失效。
而今年6月发表在《自然·癌症》的一项由多国科研团队合作的研究,揭示了DS-8201可能的耐药机制[1]。

图源:参考资料[1]
研究发现,部分耐药的乳腺癌细胞会表达一种“缩短版”的HER2蛋白,被称为p95HER2。
这种变异蛋白不仅会干扰DS-8201中抗体部分的识别,使其难以锁定癌细胞,还会促使肿瘤分泌PD-L1和IL-6等免疫抑制分子,导致免疫细胞功能被抑制,甚至“自杀”,从而削弱人体对肿瘤的免疫攻击。
02
1.HER2蛋白表达减少
DS-8201需识别癌细胞表面的HER2蛋白才能发挥作用。当HER2表达从IHC 3+降至IHC 0时,药物失去靶点,疗效下降。常见原因包括肿瘤异质性、治疗诱导的适应性变化、基因调控异常、信号通路改变或基因突变等。
此外,部分癌细胞虽HER2 mRNA水平高,但因转录或翻译障碍,无法生成足够的HER2蛋白,尤其在激素受体阳性乳腺癌中更常见,这同样会导致靶点减少、药效减弱。
图源:摄图网
2.HER2蛋白与其他蛋白形成复合体
如果HER2蛋白与其他受体蛋白如HER3结合,形成复合体,就会激活下游促进癌细胞生长的信号通路(如PI3K/AKT通路),从而增强肿瘤存活能力。这种异常信号传导会削弱DS-8201的抗肿瘤效果,使药物难以有效抑制癌细胞生长。
3.基因突变或扩增变化
那怎么知道自己是因为哪种情况导致的耐药?
可以通过病理检测看HER2表达是否下降,或者基因检测了解是否有其他基因突变;还可以检测PD-L1和IL-6水平,看看免疫系统是否被抑制。并结合影像检查和医生评估,来判断耐药的原因,根据结果调整后续治疗方案。
03
既然明确了DS-8201的耐药机制,就可以根据具体病因调整治疗方案,从而延缓或逆转肿瘤进展。
研究发现[1],针对耐药相关蛋白p95HER2,奈拉替尼具有降解作用,可减轻其引发的免疫抑制,恢复机体抗肿瘤免疫反应,从而重新激活DS-8201的疗效。
此外,奈拉替尼作为一种口服HER2酪氨酸激酶抑制剂(TKI),即使HER2蛋白表达下降,仍可通过作用于HER2信号通路发挥抗肿瘤作用。临床观察显示,奈拉替尼联合氟维司群和紫杉醇,在部分DS-8201耐药的转移性乳腺癌患者中表现出良好疗效[3]。
2025年发表于《Frontiers in Oncology》[3]的一例38岁HR+(激素受体阳性)、HER2阳性伴骨转移及肝转移的乳腺癌患者,在经历多种抗HER2治疗后出现耐药。基因检测显示ERBB2扩增及多种耐药突变。初始使用DS-8201实现近完全缓解,疾病进展后换用奈拉替尼联合氟维司群和紫杉醇,再次实现显著缓解,且耐受性良好。
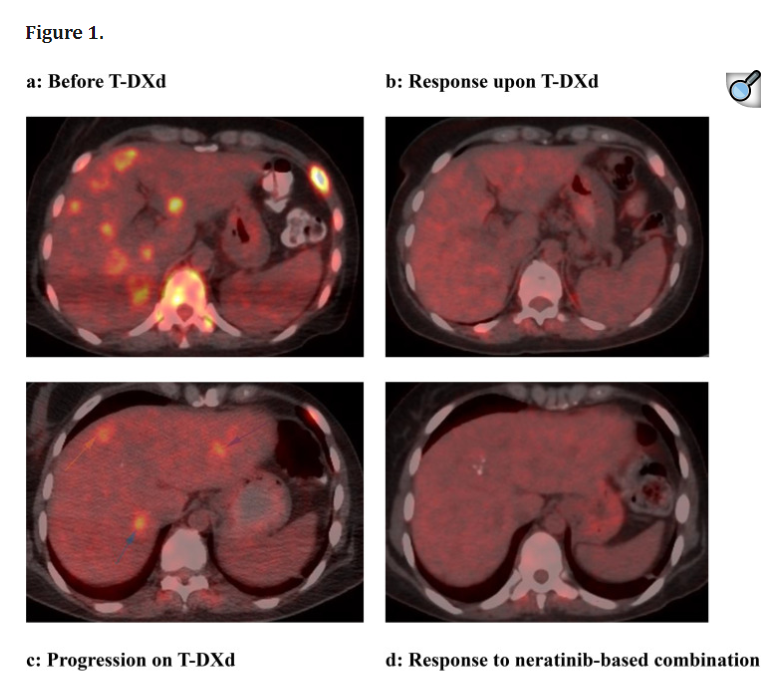
图源:参考资料[3]
除了奈拉替尼,DS-8201耐药后还可选择其他HER2靶向药物,例如指南中提到的T-DM1(恩美曲妥珠单抗)、图卡替尼、拉帕替尼、伊尼妥单抗等。这些药物与化疗(如卡培他滨)联合使用,可增强抗肿瘤效果。
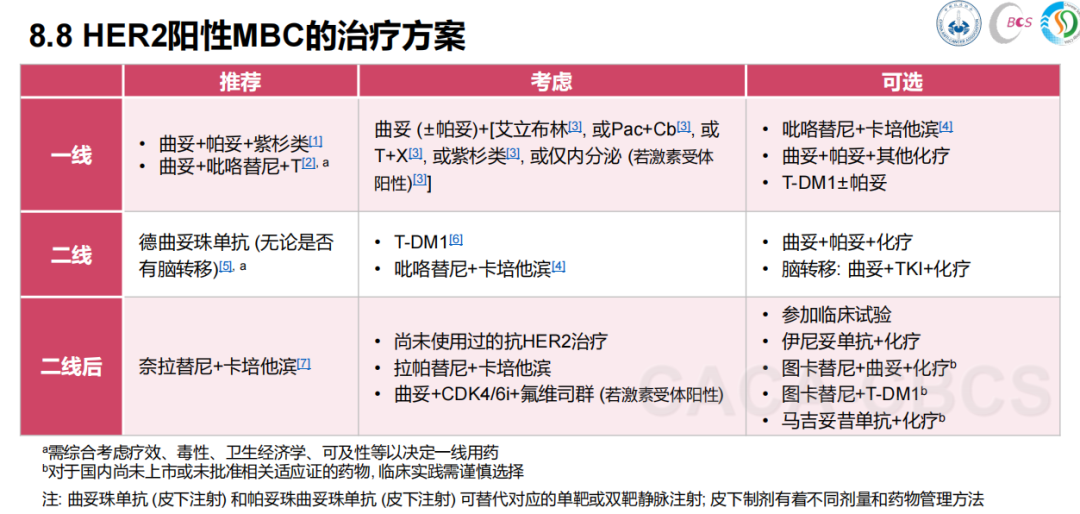
图源:CBCS&CSOBO乳腺癌诊治指南与规范精要本(2025年版)
对于激素受体阳性的患者,联合内分泌治疗(如氟维司群、CDK4/6抑制剂)也是一种重要策略。HER2信号通路与雌激素受体之间存在相互影响,联合使用HER2靶向药和内分泌治疗,有助于提升整体疗效。
此外,其他一些新型抗体药物偶联物(ADC)也相继获批应用于HER2阳性乳腺癌治疗。例如我国自主创新的维迪西妥单抗于今年5月获国家药监局批准,用于既往接受过曲妥珠单抗及其生物类似物和紫杉类药物治疗的HER2阳性且存在肝转移的晚期乳腺癌患者,并在6月提交了用于二线晚期乳腺癌HER2低表达适应证的上市申请。
有关维迪西妥单抗的文章,《刚刚!这款乳腺癌药获批了新适应证,针对乳腺癌肝转移!不是化疗药……》。
04
新药不断涌现,治愈的希望就在前方。只要积极治疗、定期复查、规律生活、保持好心态,姐妹们一定能找到适合自己的疗法,战胜癌细胞!
收藏
回复(5)参与评论
评论列表

























