EGFR靶向之路(Mark)
今天看了一篇文章,认真看了几遍,受益。
mark在这里。
一线之争:一代VS二代
既往共9个大型III期随机对照研究结果奠定了EGFR-TKI在EGFR敏感突变患者中一线治疗的地位,成为此类患者首选的治疗方案;近年,各权威指南均做出了相应的治疗推荐;但一、二代EGFR-TKI孰优孰劣,尚未见充足证据。来自中国的胸部肿瘤协作组的CTONG0901临床试验对比了厄洛替尼与吉非替尼在治疗携带EGFR 19或21突变的晚期非小细胞肺癌中的疗效以及生存差异。结果证实,无论是有效率、PFS还是OS,两者都未有明显差异。
LUX-Lung7为首个头对头比较吉非替尼与阿法替尼疗效的III期临床试验,其结果也在去年公布:与吉非替尼组相比,阿法替尼组PFS(HR 0.73,95%CI 0.57-0.95,P=0.016 5)显著得到提高,随着时间的推移,PFS改善更加显著,阿法替尼组和吉非替尼组的中位至治疗失败时间(TTF)分别为13.7 个月和11.5 个月(P=0.0073),但毒副作用上阿法替尼大过吉非替尼。OS 数据尚不成熟。
另一项LUX-Lung3和LUX-Lung6的合并分析显示:对于EGFR 19外显子缺失突变病人,阿法替尼组的总生存要显著优于化疗组。而另一个二代EGFR-TKI达克替尼(Dacomitinib)与一代TKI吉非替尼及厄洛替尼相比较,在疾病无进展生存期和总生存期有一定延长作用,但严重的不良反应有可能会限制该药物的发展;其在一线用药的III期临床研究(ARCHER 1050)也即将公布。
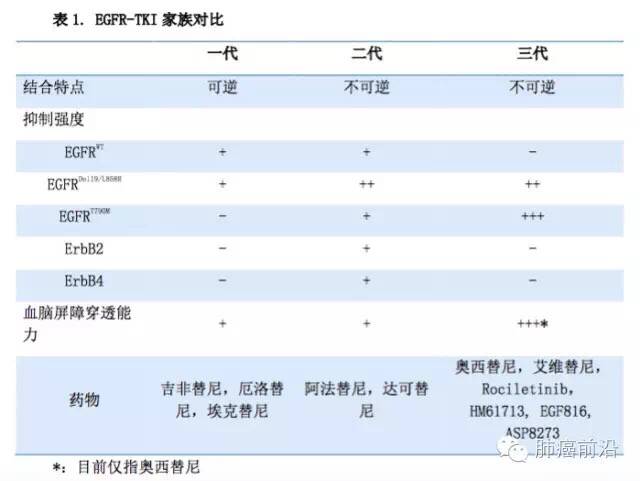
目前,在一线获得适应症的一代EGFR-TKI有吉非替尼和厄洛替尼,二代有阿法替尼。临床中选择何种EGFR-TKI需要综合考虑病人的EGFR突变亚型,毒性耐受程度以及经济成本。
EGFR突变亚型细分:19外显子缺失,L858R点突变和其他少见突变
EGFR突变在亚裔人群占22.2%到64.2%,而在高加索人群仅占10%。常见EGFR突变类型包括19外显子缺失和L858R点突变,占全部EGFR突变患者的90%左右。越来越多的数据表明:EGFR-TKI应用于不同EGFR敏感突变类型的效果不尽相同。LUX-Lung3和LUX-Lung6两个大型、开放III期临床研究的总生存数据显示:无论是单独研究分析还是探索性合并分析,与化疗相比,19外显子缺失突变患者一线接受阿法替尼治疗可明显提高OS。但21外显子点突变患者的OS,与化疗相比,均无显著性差异。该研究结论提示,19外显子缺失突变和21外显子点突变患者可能是两类不同的NSCLC人群,应在未来分开进行研究。
少见突变占EGFR突变患者的10%左右,且突变种类众多,是一类异质性较大的人群。Wu等整理了LUX-Lung2,LUX-Lung3和LUX-Lung6中共75例EGFR少见突变患者服用阿法替尼的疗效数据。其中G719X, L861G和S768I 少见突变患者服用阿法替尼的有效率分别是77.8%, 56.3%,100%,提示对于这类少见突变,阿法替尼可能是一项很好的选择。而T790M和20外显子插入突变对阿法替尼反应率差,中位无进展生存时间不到3个月,疗效差于传统的化疗。
EGFR-TKI联合治疗策略
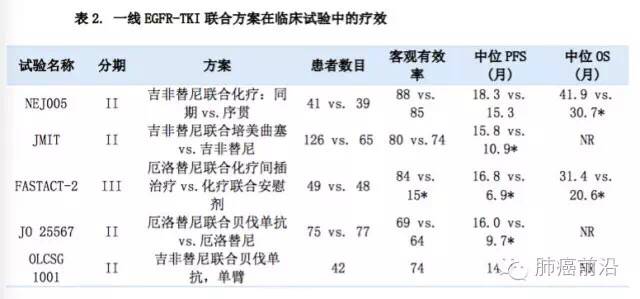
EGFR-TKI联合化疗的模式一直存在争议。有部分临床前研究显示EGFR-TKIs与化疗直接联合可能产生拮抗作用。今年JCO 报道的JMIT研究以 EGFR高频突变的东亚人群为研究对象,对靶向药物和化疗的同步联合治疗模式进行了进一步探索,培美曲塞(不含铂)联合吉非替尼的PFS为15.8个月,相对于吉非替尼单药可带来将近5个月的PFS改善,且没有明显增加不良反应的发生率,这对EGFR敏感突变患者的一线治疗策略的选择有较大的指导意义,期待OS数据的后续报道。NEJ005研究证实对于EGFR突变的晚期NSCLC患者,同步联合治疗较序贯治疗模式更胜一筹,并开展了同步联合治疗对比单药靶向治疗的III期临床研究(NEJ009)。
在联合治疗模式中,EGFR-TKI联合抗血管生成也被认为具有协同作用,进一步促进抗肿瘤作用。JO25567研究中厄洛替尼联合贝伐珠单抗一线治疗EGFR突变患者的治疗模式的PFS为16.0个月(16.0月 vs 9.7月,P=0.0015),然而这只是一个单中心的小样本量II期研究,目前还需要更多的数据支持。
针对EGFR-TKI耐药策略目前较成熟的有T790M抑制剂(第三代EGFR-TKI)和MET抑制剂。针对T790M突变患者,奥希替尼能够带来61%的缓解率和9.6个月的中位PFS获益,且皮疹等不良反应发生率较低。同时奥希替尼一线治疗EGFR突变患者也有着令人满意的效果,从2016 年ASCO公布的60例患者数据来看, ORR为73%,DCR达到97%。目前奥希替尼对比吉非替尼一线治疗EGFR突变晚期非小细胞肺癌III期临床研究(FLAURA)研究尚在进行中。Rociletinib(CO-1686)由于疗效稳定性欠佳,同时伴有较严重的毒副反应而被FDA叫停。其他第3代EGFR-TKI在T790M阳性患者中的疗效分别为:HM61713 56%, EGF816 44%, ASP8273 65%。而针对第三代EGFR-TKI耐药的病例已有陆续报道,其机制包括有EGFR新型突变C797S及T790M突变消失等。
此外,近期有两个MET抑制剂的研究公布了其最新数据,客观有效率分别为31% (capmatinib,INC280)和27%(tepotinib),其中capmatinib在MET≥ 6个拷贝的亚组及tepotinib在MET≥5个拷贝的亚组中有效率都高达50%。
克服脑转移问题
大约有25%-40%的非小细胞肺癌患者在治疗过程中会出现中枢神经系统(CNS)转移。而CNS转移在EGFR突变患者常见其可能与突变患者生存期延长,一、二代TKI在颅内浓度低相关。既往报道显示,一代EGFR-TKI及阿法替尼在CNS转移患者中均有疗效,客观有限率为58%-83%,中位PFS和OS分别为7-15 个月和13-21个月。2016年ASCO年会上报道了第三代EGFR-TKI奥西替尼和新型EGFR-TKI AZD3759在CNS转移患者中的I期研究(BLOOM研究)结果。在奥西替尼组,7例患者(33%)达到已确认的影像学好转; 9例患者(43%)达到已确认的颅内疾病稳定(SD),2例未确认的颅内SD。提示奥希替尼在CNS转移中具有显著的疗效。
AZD3759 是第一个为有效透过血脑屏障治疗脑转移而设计的EGFR抑制剂,旨在克服EGFR突变的CNS转移,ASCO中报道AZD3759治疗脑实质转移和脑膜转移NSCLC的I期研究提示AZD3759是可耐受的,可达到抑制靶病灶,颅内抗肿瘤效果可观。
近十几年来非小细胞肺癌的治疗状态:从化疗时代的30%到如今的接近80%,中位生存期也从原来的10个月增长到39个月,并且还将继续延长。
但新的问题也随之而来:1)随着时空异质性以及多重耐药问题的出现,精准治疗之下应该如何合理地选择病人2)是否应该在一出现T790M突变即改用第3代EGFR-TKI 3)液体活检的时间点该如何选择?动态、定量检测 T790M突变,其耐药的阈值该如何设定?
mark在这里。
一线之争:一代VS二代
既往共9个大型III期随机对照研究结果奠定了EGFR-TKI在EGFR敏感突变患者中一线治疗的地位,成为此类患者首选的治疗方案;近年,各权威指南均做出了相应的治疗推荐;但一、二代EGFR-TKI孰优孰劣,尚未见充足证据。来自中国的胸部肿瘤协作组的CTONG0901临床试验对比了厄洛替尼与吉非替尼在治疗携带EGFR 19或21突变的晚期非小细胞肺癌中的疗效以及生存差异。结果证实,无论是有效率、PFS还是OS,两者都未有明显差异。
LUX-Lung7为首个头对头比较吉非替尼与阿法替尼疗效的III期临床试验,其结果也在去年公布:与吉非替尼组相比,阿法替尼组PFS(HR 0.73,95%CI 0.57-0.95,P=0.016 5)显著得到提高,随着时间的推移,PFS改善更加显著,阿法替尼组和吉非替尼组的中位至治疗失败时间(TTF)分别为13.7 个月和11.5 个月(P=0.0073),但毒副作用上阿法替尼大过吉非替尼。OS 数据尚不成熟。
另一项LUX-Lung3和LUX-Lung6的合并分析显示:对于EGFR 19外显子缺失突变病人,阿法替尼组的总生存要显著优于化疗组。而另一个二代EGFR-TKI达克替尼(Dacomitinib)与一代TKI吉非替尼及厄洛替尼相比较,在疾病无进展生存期和总生存期有一定延长作用,但严重的不良反应有可能会限制该药物的发展;其在一线用药的III期临床研究(ARCHER 1050)也即将公布。
目前,在一线获得适应症的一代EGFR-TKI有吉非替尼和厄洛替尼,二代有阿法替尼。临床中选择何种EGFR-TKI需要综合考虑病人的EGFR突变亚型,毒性耐受程度以及经济成本。
EGFR突变亚型细分:19外显子缺失,L858R点突变和其他少见突变
EGFR突变在亚裔人群占22.2%到64.2%,而在高加索人群仅占10%。常见EGFR突变类型包括19外显子缺失和L858R点突变,占全部EGFR突变患者的90%左右。越来越多的数据表明:EGFR-TKI应用于不同EGFR敏感突变类型的效果不尽相同。LUX-Lung3和LUX-Lung6两个大型、开放III期临床研究的总生存数据显示:无论是单独研究分析还是探索性合并分析,与化疗相比,19外显子缺失突变患者一线接受阿法替尼治疗可明显提高OS。但21外显子点突变患者的OS,与化疗相比,均无显著性差异。该研究结论提示,19外显子缺失突变和21外显子点突变患者可能是两类不同的NSCLC人群,应在未来分开进行研究。
少见突变占EGFR突变患者的10%左右,且突变种类众多,是一类异质性较大的人群。Wu等整理了LUX-Lung2,LUX-Lung3和LUX-Lung6中共75例EGFR少见突变患者服用阿法替尼的疗效数据。其中G719X, L861G和S768I 少见突变患者服用阿法替尼的有效率分别是77.8%, 56.3%,100%,提示对于这类少见突变,阿法替尼可能是一项很好的选择。而T790M和20外显子插入突变对阿法替尼反应率差,中位无进展生存时间不到3个月,疗效差于传统的化疗。
EGFR-TKI联合治疗策略
EGFR-TKI联合化疗的模式一直存在争议。有部分临床前研究显示EGFR-TKIs与化疗直接联合可能产生拮抗作用。今年JCO 报道的JMIT研究以 EGFR高频突变的东亚人群为研究对象,对靶向药物和化疗的同步联合治疗模式进行了进一步探索,培美曲塞(不含铂)联合吉非替尼的PFS为15.8个月,相对于吉非替尼单药可带来将近5个月的PFS改善,且没有明显增加不良反应的发生率,这对EGFR敏感突变患者的一线治疗策略的选择有较大的指导意义,期待OS数据的后续报道。NEJ005研究证实对于EGFR突变的晚期NSCLC患者,同步联合治疗较序贯治疗模式更胜一筹,并开展了同步联合治疗对比单药靶向治疗的III期临床研究(NEJ009)。
在联合治疗模式中,EGFR-TKI联合抗血管生成也被认为具有协同作用,进一步促进抗肿瘤作用。JO25567研究中厄洛替尼联合贝伐珠单抗一线治疗EGFR突变患者的治疗模式的PFS为16.0个月(16.0月 vs 9.7月,P=0.0015),然而这只是一个单中心的小样本量II期研究,目前还需要更多的数据支持。
针对EGFR-TKI耐药策略目前较成熟的有T790M抑制剂(第三代EGFR-TKI)和MET抑制剂。针对T790M突变患者,奥希替尼能够带来61%的缓解率和9.6个月的中位PFS获益,且皮疹等不良反应发生率较低。同时奥希替尼一线治疗EGFR突变患者也有着令人满意的效果,从2016 年ASCO公布的60例患者数据来看, ORR为73%,DCR达到97%。目前奥希替尼对比吉非替尼一线治疗EGFR突变晚期非小细胞肺癌III期临床研究(FLAURA)研究尚在进行中。Rociletinib(CO-1686)由于疗效稳定性欠佳,同时伴有较严重的毒副反应而被FDA叫停。其他第3代EGFR-TKI在T790M阳性患者中的疗效分别为:HM61713 56%, EGF816 44%, ASP8273 65%。而针对第三代EGFR-TKI耐药的病例已有陆续报道,其机制包括有EGFR新型突变C797S及T790M突变消失等。
此外,近期有两个MET抑制剂的研究公布了其最新数据,客观有效率分别为31% (capmatinib,INC280)和27%(tepotinib),其中capmatinib在MET≥ 6个拷贝的亚组及tepotinib在MET≥5个拷贝的亚组中有效率都高达50%。
克服脑转移问题
大约有25%-40%的非小细胞肺癌患者在治疗过程中会出现中枢神经系统(CNS)转移。而CNS转移在EGFR突变患者常见其可能与突变患者生存期延长,一、二代TKI在颅内浓度低相关。既往报道显示,一代EGFR-TKI及阿法替尼在CNS转移患者中均有疗效,客观有限率为58%-83%,中位PFS和OS分别为7-15 个月和13-21个月。2016年ASCO年会上报道了第三代EGFR-TKI奥西替尼和新型EGFR-TKI AZD3759在CNS转移患者中的I期研究(BLOOM研究)结果。在奥西替尼组,7例患者(33%)达到已确认的影像学好转; 9例患者(43%)达到已确认的颅内疾病稳定(SD),2例未确认的颅内SD。提示奥希替尼在CNS转移中具有显著的疗效。
AZD3759 是第一个为有效透过血脑屏障治疗脑转移而设计的EGFR抑制剂,旨在克服EGFR突变的CNS转移,ASCO中报道AZD3759治疗脑实质转移和脑膜转移NSCLC的I期研究提示AZD3759是可耐受的,可达到抑制靶病灶,颅内抗肿瘤效果可观。
近十几年来非小细胞肺癌的治疗状态:从化疗时代的30%到如今的接近80%,中位生存期也从原来的10个月增长到39个月,并且还将继续延长。
但新的问题也随之而来:1)随着时空异质性以及多重耐药问题的出现,精准治疗之下应该如何合理地选择病人2)是否应该在一出现T790M突变即改用第3代EGFR-TKI 3)液体活检的时间点该如何选择?动态、定量检测 T790M突变,其耐药的阈值该如何设定?
收藏
回复(0)举报
参与评论
评论列表
按投票顺序
相关推荐
热点推荐
暂无数据
























