非小细胞肺鳞癌的患者,这些靶向药物也可以考虑
虽然鳞癌EGFR、ALK突变率低,但NCCN指南仍然推荐无吸烟史或小组织样本(穿刺活检)确诊鳞癌或腺鳞混合癌的患者初始进行EGFR、ALK突变检测,NCCN指南也推荐鳞癌患者初始进行ROS1突变检测,而且除了以上突变检测,还应进行更广泛的分子检测。
主要驱动突变与相应TKI如下表:
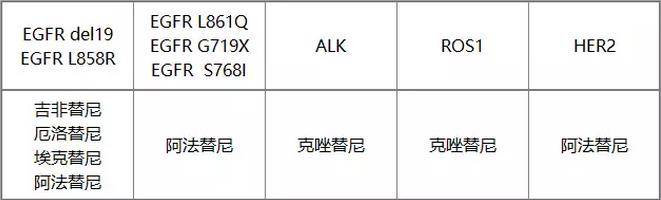
除了TKI外,一线分子靶向药物还有Necitumumab,这是一种EGFR 单抗,与吉西他滨 铂类化疗方案联合一线治疗晚期鳞癌,相比化疗延长了患者的中位无进展生存期(PFS 11.5个月VS 9.9个月),基于此FDA批准Necitumumab联合双药化疗方案应用于晚期鳞癌一线治疗,但NCCN指南未将Necitumumab纳入一线推荐治疗方案。
二线分子靶向治疗
驱动基因突变明确的鳞癌
EGFR突变晚期鳞癌患者一线TKI治疗后疾病进展,NCCN指南推荐行T790M突变检查,若T790M突变阳性则可接受Tagrisso(AZD9291 泰瑞沙)治疗。

ALK阳性晚期鳞癌患者一线TKI治疗后疾病进展,NCCN指南推荐艾乐替尼或色瑞替尼作为二线治疗。
没有驱动基因突变的鳞癌
对于没有驱动突变的晚期鳞癌患者,NCCN指南推荐的唯一分子靶向治疗方案是雷莫芦单抗联合多西他赛,此方案被推荐用于二线治疗。雷莫芦单抗也是目前唯一被FDA批准用于鳞癌的抗血管生成药,在III期临床试验REVEL中,雷莫芦单抗联合多西他赛治疗经含铂化疗方案治疗后疾病进展的NSCLC,较安慰剂 多西他赛显著延长了中位PFS(4.5个月VS 3个月),中位总生存期(OS 10.5个月VS 9.1个月),客观缓解率(ORR 22.9% VS 13.6%),腺癌、鳞癌获益相似,雷莫芦单抗联合多西他赛组有更多的出血事件(任何级别 28.9 % vs 15.2%),但≥3级出血事件则没有显著增多(2.4% vs 2.3%)。
驱动基因突变不明的鳞癌
FDA和欧盟于2016年4月基于LUX-Lung-8 III期临床试验结果批准阿法替尼用于经含铂化疗方案治疗后疾病进展的晚期鳞癌治疗。LUX-Lung 8试验是目前样本量最大的、前瞻性、头对头比较阿法替尼和厄洛替尼二线治疗晚期鳞癌的临床试验,厄洛替尼之前曾被批准用于晚期NSCLC的维持或二线治疗,结果阿法替尼在PFS(2.6个月VS 1.9个月)、OS(7.9个月VS 6.8个月)及患者报告健康状况方面均优于厄洛替尼。然而NCCN指南并未将阿法替尼纳入肺鳞癌二线推荐治疗方案。
虽然FDA早在2004年已批准厄洛替尼用于晚期NSCLC二线治疗,并于2010年扩展厄洛替尼适应症为晚期NSCLC一线化疗后的维持治疗,但在2016年10月FDA再次将厄洛替尼的适应症修改为EGFR del19或L858R突变晚期NSCLC维持或二线治疗 ,这是对肺癌驱动突变认识深化的结果。阿法替尼在鳞癌二线治疗上仅被证明优于厄洛替尼,因此将其应用于未经筛选的晚期鳞癌二线治疗的证据并不够有力。
新靶点探索
FGFR
12%的鳞癌患者具有FGFR的扩增,临床前研究显示其抑制剂Nintedanib、Dovitinib等均有疗效。Nintedanib的作用靶点是FGFR、VEGFR、PDGFR,在LUME-lung 1这个III期研究中,研究者评估了多西他赛联合Nintedanib(n=206)对比多西他赛联合安慰剂(n=199)作为NSCLC的二线治疗方案的有效性和安全性,结果显示不论组织学类型如何,联合应用延长了PFS,明显延长了腺癌患者OS。入组人群中42.1%为鳞癌患者,其疾病控制率高于腺癌患者,但OS较腺癌患者差。因此,多西他赛联合Nintedanib二线治疗鳞癌患者受益不多。
Dovitinib是FGFR、VEGFR、FLT3、c-Kit的抑制剂,一个单臂的II期临床试验评估dovitinib单药治疗经治的FGFR扩增晚期鳞癌的疗效和安全性,结果:ORR 11.5%,疾病控制率50%,PFS 2.9个月,OS 5个月,研究者认为Dovitinib治疗FGFR扩增的晚期鳞癌疗效有限。
目前的临床试验结果显示FGFR并不是一个很有效的鳞癌治疗靶点。
BRAF、KRAS
相比纯鳞癌,BRAF、KRAS突变更多出现在腺鳞混合癌中,是潜在的治疗靶点。
欧盟基于一个开放标签的II期临床试验(编号NCT01336634.)结果批准达拉菲尼(BRAF抑制剂)联合曲美替尼(MEK抑制剂)用于治疗BRAF V600E突变阳性晚期NSLCL,这个临床试验入组了57例BRAF V600E突变的晚期NSCLC患者,这些患者均至少接受过一个含铂的治疗方案治疗且不超过3个全身性治疗方案,而后疾病进展。试验结果显示达拉菲尼联合曲美替尼治疗的ORR达到63.2%,中位PFS 9.7个月,但该试验纳入的患者98%为腺癌,鳞癌患者疗效仍需更大规模临床试验评估。
BGB-283是小分子RAF二聚体和EGFR双重抑制剂,目前完成了评估其治疗BRAF或KRAS/NRAS突变的实体瘤患者(含NSCLC)的安全性和有效性的Ib期临床试验,试验结果显示两例BRAF V600E突变NSCLC患者中,1例患者未确认的PR,一例患者SD。6例KRAS突变患者中,1例PR,2例SD。试验初步肯定了BGB-283的安全性和有效性,未来会开展更大规模临床试验。
CDK和MEK位于RAS基因下游,相对RAS基因更容易靶向抑制。研究人员为评估帕博西尼(Palbociclib)联合PD-0325901治疗RAS基因突变驱动的恶性肿瘤的安全性及有效性开展了I期临床试验,其中帕博西尼是已上市的CDK4/6抑制剂,PD-0325901是处于研究阶段的MEK抑制剂。
试验入组了25例患者,其中17例是KRAS突变肺癌患者,患者每天1或2次给药,以5个不同剂量接受治疗,连续给药3周,停药一周。结果1例肿瘤部分缓解,18例最佳治疗反应为疾病稳定。7例疾病稳定超过6个月,其中5例为NSCLC。试验初步证实帕博西尼联合PD-0325901安全可耐受,对KRAS突变NSCLC有一定的疗效。
收藏
回复(4)参与评论
评论列表
























