终于等到你!乳腺癌ADC药物DS-8201首次在中国获批
2月24日,中国国家药监局(NMPA)官网最新公示,阿斯利康和第一三共联合开发的注射用德曲妥珠单抗(即DS-8201)已正式在中国获批上市,这也是该药物首次在中国获批。
本次获批适应症为:单药适用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
下面就让我们简单回顾一下DS-8201的丰功伟绩。
01 强强联合,集精准威猛于一身
DS-8201是由抗体、连接子和细胞毒药物三部分组成。
抗体是专门针对HER2靶点的曲妥珠单抗,能够精准识别HER2阳性表达的癌细胞;
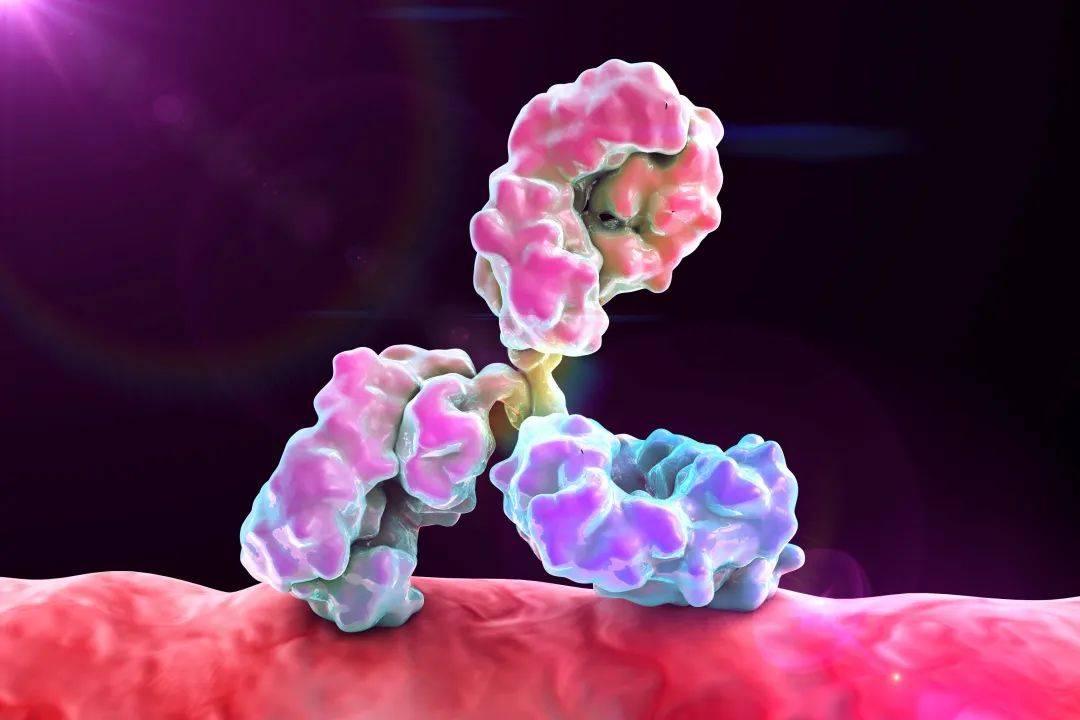
连接以上两者的连接子也是“不同凡响”,是四肽连接子,拥有1:8的药物抗体比,每个抗体可携带更多有效化疗药物,性能更高效。不仅如此,这个四肽连接子被癌细胞内的溶菌酶“锯断”,更快速的释放出Dxd,没了束缚的Dxd更能在癌细胞中“大展雄风”。
细胞毒药物则是新型拓扑异构酶抑制剂喜树碱类衍生物(Dxd),其具有更强的膜穿透性,可以穿透至邻近细胞,无论是邻近细胞是HER2阳性表达或是HER2阴性表达的癌细胞都无法逃脱它的“魔爪”;
02 DB-03:PFS超过4倍,1/5患者肿瘤消失!
本次DS-8201之所以能落地中国,主要与DESTINY-Breast03(以下简称“DB-03”)有着密切关系。
DB-03是一项Ⅲ期临床试验,研究头对头比较了T-DM1与DS-8201用于HER2阳性转移性乳腺癌患者的二线治疗的疗效与安全性。
在2021年ESMO年会发布DB03的中期分析数据中,DS-8201的疗效特别突出,显示出史无前例的PFS改善(疾病进展或死亡风险下降72%),其中主要研究终点独立盲法评估的PFS。
当时DS-8201组在中位随访16个月后尚未达到中位值(也即尚未有一半的患者出现肿瘤进展或死亡),而对照组仅6.8个月;至于关键次要研究终点OS,也由于事件数太少而差异未达到统计学显著性。
2022 SABCS大会公布了DESTINY-Breast03研究的最新数据,DS-8201的中位PFS又一次突破记录,独立盲法评估的中位PFS达到28.8个月,是对照组的4倍余(对照组为6.8个月)。
随访时间延长后,OS(总生存期)也显示出显著获益,差异达到统计学显著性,DS-8201显著降低患者死亡风险36%,两组的2年总生存率分别为77.4%和69.9%。 此外,DS-8201组有21.1%的患者达到肿瘤完全缓解,这也是前所未有的数据。 03 指南与适应症
在2022年发表的《靶向HER2乳腺癌诊疗中国专家共识(2023版)》中,专家组推荐曲妥珠单抗治疗失败后的患者优先选择DS-8201。
DESTINY-Breast 04 研究显示,在HER2低表达的不可切除和/或转移性乳腺癌患者中,无论患者是否为激素受体阳性,相比医生选择的化疗,DS-8201均能显著改善HER2低表达转移性乳腺癌患者的PFS和OS。
图源:摄图网
在安全性方面,DS-8201安全性数据与已知的安全性特征一致,且相比化疗可改善患者生活质量,总体获益大于风险。基于这些研究成果,目前DS-8201已被NCCN、ASCO等指南推荐为HER2低表达晚期乳腺癌标准治疗。
在《靶向HER2乳腺癌诊疗中国专家共识(2023版)》中,专家组认为,HER2低表达患者,应先根据HR状态,接受其相应的标准治疗。
HR阳性的HER2低表达患者,推荐参考HR阳性乳腺癌治疗原则,选择内分泌治疗,若治疗失败,可考虑选用DS-8201;
HR阴性的HER2低表达患者,推荐参考三阴性乳腺癌治疗原则,选择紫杉类、铂类等的化疗药物,若治疗失败,可考虑选择DS-8201。
在美国,DS-8201已被FDA批准用于治疗HER2低表达乳腺癌、HER2阳性胃癌和胃食管结合部腺癌患者、携带HER2突变的非小细胞肺癌患者等适应症。
2022年8月,国家药品监督管理局药品审评中心也受理了DS-8201在中国的第二个适应症上市申请,拟用于治疗既往在转移性疾病阶段接受过至少一种系统治疗或在辅助化疗期间或完成辅助化疗之后6个月内复发的不可切除或转移性HER2低表达乳腺癌成人患者。
04 结语
关于DS-8201的介绍我们就到此结束了,不知你是否对它有了更为深入的了解呢?我们相信,随着DS-8201的上市,将有更多乳腺癌患者能够从中受益,获得新的生存希望!
收藏
回复(4)参与评论
评论列表
























