喜讯!又一联合治疗方案获肝癌一线治疗的优先审批!
上周,国家药品监督管理局审评中心(CDE)又放出了一个大招——信迪利单抗联合贝伐珠单抗用于既往未接受过系统治疗的不可切除或转移性肝细胞癌的上市申请拟纳入优先审批。
图片来源:CDE官网
据悉,此次获得优先审批的原因主要基于一项名为ORIENT 32 的研究。
ORIENT 32是由复旦大学中山医院樊嘉领头,全国多家医院参与的一项随机、开放、Ⅲ期对照临床试验。此外,该试验也是全球首个达到主要研究终点的PD-1抑制剂联合治疗用于晚期以乙肝病毒感染(HBV)相关性肝癌为主要研究对象的临床研究。
试验一共纳入例如571例中国肝癌患者,且将这些患者随机分为索拉非尼组和信迪利单抗联合贝伐珠单抗组,经过随访研究发现:
信迪利单抗联合贝伐珠单抗组的中位OS(总生存期)明显高于索拉非尼组(尚未观察到 vs 10.4个月,P值<0.0001),联合治疗还能降低43.5%的进展风险,中位PFS也得到了(无进展生存期)显著提高(4.5个月 VS 2.8个月,P值小于0.001)。
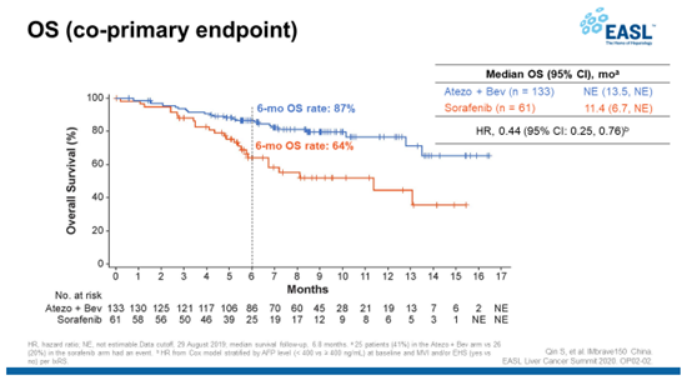
此外,在所有亚组分析中,联合治疗组的总生存期和无进展生存期都要高于索拉非尼组,且不良反应可控,安全性良好。
需要注意的是,该研究曾在2020年欧洲肿瘤内科学会亚洲年会(ESMO ASIA)线上会议已经被以优选口头报告的形式公布,可见该研究也得到了国际认可。
我国肝癌患者和国外的不同,我国肝癌患者绝大多数都是由于乙型肝炎引起的,而此次试验纳入的患者人群也多是乙肝引起的肝癌,更符合我国国情。而且此次研究结果也显示出了优于索拉非尼的临床效果,如果能获批,或将成为我国肝癌患者一项新的选择。
此外,信迪利单抗和贝伐珠单抗都已经纳入医保,尽管未获批肝癌适应症,但其价格也较为低廉。
收藏
回复(0)举报
参与评论
评论列表
按投票顺序
相关推荐
热点推荐
2013-11-19 14:23:04
爸爸确诊病情已经有11个多月了。一共做了8次大化疗,2次小化疗,以及35次放疗,上月返医院检查“瘤子”没有了。这一路走来,有多少的艰辛与泪水。在这里与大家分享爸爸的治疗过程。起初,拿到病例报告的时候,
2013-11-19 14:31:01
妈妈患肺癌已经有三年了,这三年来一直在接受治疗到现在,下面是妈妈检查以及治疗的过程。2010年10月,妈妈体检出肺癌IV期,纵隔淋巴转移,肝部转移,去省肿瘤医院复查,做了PET-CT,结果一样,省肿瘤
2013-11-19 15:04:43
2011年11月,妈妈被诊断肺癌,我在网上浏览了很多帖子,学到了很多,看到了一批又一批共同奋斗在抗癌战线上的战友。这15个月走下来,越来越体会到抗癌之路的艰辛,今天发个帖子,记录一下妈妈的治疗经过,也
























