ALK笔记:靶向治疗碎碎念

♥ ALK检测
» 靶向治疗用药以基因检测为依据,尽量使用组织,除非必要不建议血液或胸水。
血液检测结果一:检测不出变异基因

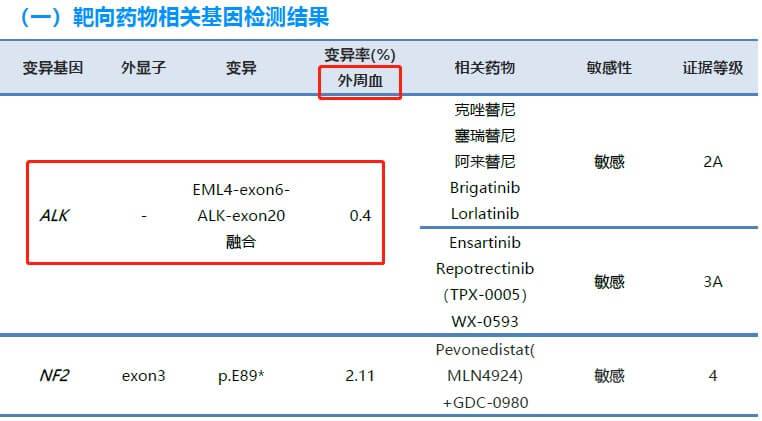
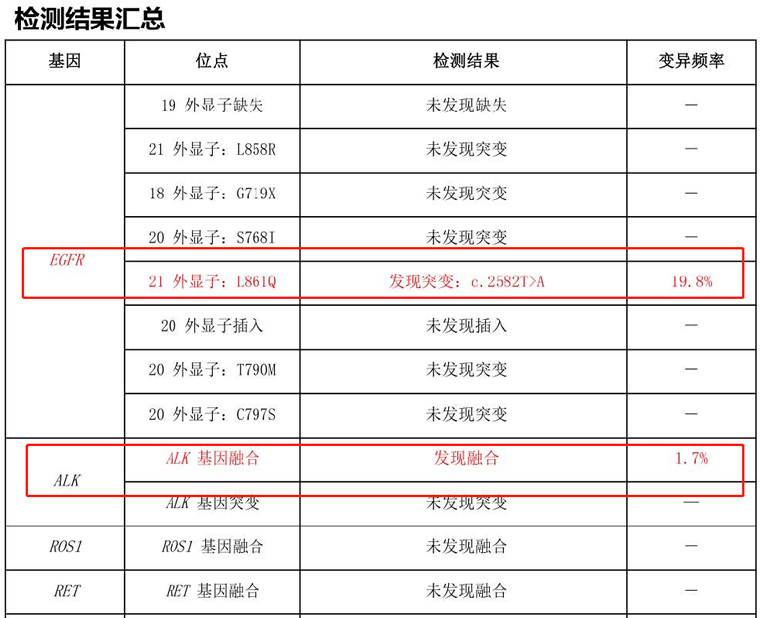
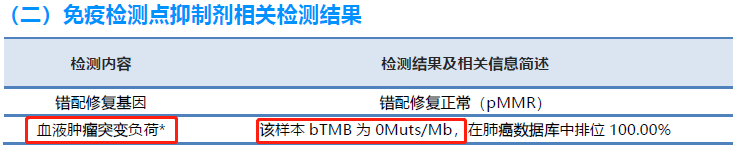 血液检测结果二:检测出驱动基因,检测丰度值低
血液检测结果二:检测出驱动基因,检测丰度值低
» 免疫组化(IHC)是ALK检测的重要方法,检测报告中VENTANA IHC (D5F3):ALK(加号 ),表示使用罗氏ALK免疫检测试剂盒检测ALK融合阳性,有ALK融合基因突变,对ALK靶向药敏感。其中D5F3是ALK抗体名称,VENTANA为罗氏收购的美国一家专业检测公司,VENTANA ALK (D5F3)表示免疫组化检测使用的是罗氏VENTANA重组兔源单克隆抗体试剂盒。
» ALK突变以腺癌为主,少量鳞癌,小细胞目前还没有发现。
» ALK突变理论上有三种:点突变,融合和扩增。在实际的基因检测中以融合为主,少量点突变,单纯的ALK扩增病例不常见。其中点突变对靶向药不敏感,扩增加量可能有效,融合即我们通常所讲的钻石突变,并非所有的ALK融合对靶向药敏感,有小部分融合突变原发耐药。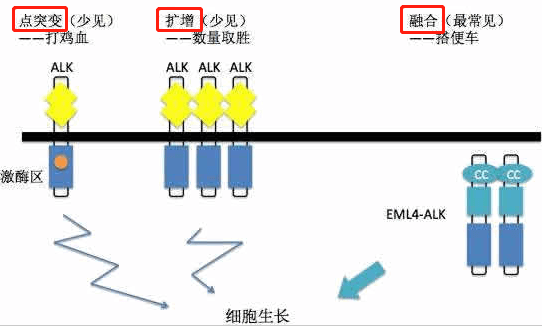
» 非小腺ALK融合伴侣以EML4为主,EML4-ALK占90%-95%,根据EML4断裂融合位置分为不同的亚型。E6:A20表示EML4从6号外显子位置断裂,ALK从20号外显子处断裂,倒位拼接形成融合基因突变,即V3亚型。各亚型中V1占比43%,V3占比40%,有研究报道V1PFS最优,也有报道V2最优,有研究报道V3对劳拉敏感,优于其他亚型,也有报道V3对劳拉PFS最短。以上均为小样本研究,没有确定结论,亚型的分类对PFS/OS没有决定性作用。
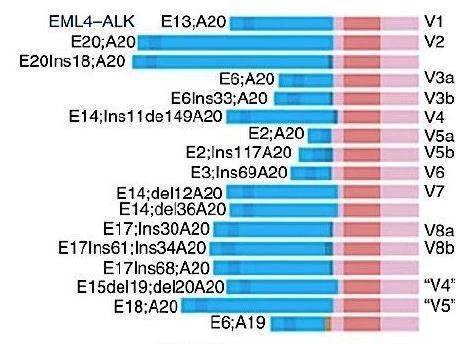
» 非EML4-ALK类型(至少113种)占ALK融合的5%-10%。ALK致癌发生在ALK激酶端,磷酸化异常激活胞内信号通路,融合伴侣起到取代配体的作用,其中多数融合伴侣与EML4视同一致,对靶向药敏感,无PFS和OS的明显差异。可与ALK融合致癌的基因如下:
» ALK通常与单一的融合伴侣在5'端发生融合,燃石最新的NGS测序研究显示,在ALK融合过程中发现有5'端和3'端同时与两个不同基因发生融合的情况,即ALK相互/非相互融合,可能和不良预后相关。

» ALK/EGFR双驱动,概率小,对比单一的ALK驱动,耐药快,预后较差。双突变有两种情况:1.一部分癌细胞EGFR驱动,另一部分ALK驱动。2.同一癌细胞内既有EGFR通路又有ALK通路。可选择的用药方法有四种:1.EGFR-TKIs,2.ALK-TKIs,3.同时使用双靶向,4.轮换使用两种靶向药。但是以上两个问题都无法确定如何选择获益最大化,不仅仅是以检测丰度来确定,因人而异~
♥ ALK中晚期的治疗方案
» ALK突变相比EGFR等其他癌变驱动基因,恶性程度高,术后复发频率高。
» 检测到ALK融合,仍有小概率对靶向药不敏感的原发耐药,或短期内对各种靶向药耐药。
» 非小腺Ⅲ期:
1.可手术的Ⅲ期N0,术后根治性同步放化疗。
2.Ⅲ期N1预期可完全切除的可在术前做新辅助治疗后手术,然后根治性同步放化疗。
3.Ⅲ期N2预期无法完全切除的,在根治性同步放化疗后辅助爱药(度伐利尤单抗)治疗。
4.Ⅲ期不可手术指南方案是同步放化疗后度伐利尤单抗两年维持治疗,但是在实际治疗中发现同步放化疗后使用爱药进展,更换为靶向治疗方案。
» ALK的Ⅲ期不可手术根治性治疗方案关键点在于爱药是否有效维持,爱药没有有效抑制,则同步放化疗达不到根治目的。爱药的效率与PDL1表达相关,虽然爱药对免疫表达阴性也有一定概率有效,高表达有效概率更高。确定方案时可参考PDL1表达值来选择,高表达首选同步放化疗联合爱药,低表达可考虑一线阿来替尼靶向。
» ALK中晚期现实世界的治疗方案要复杂的多,主要包括: 3A术后空窗,一线化疗,一线克唑替尼,一线阿来替尼,一线色瑞替尼,一线同步放化疗联合爱药免疫治疗,一线化疗联合免疫治疗(含OY双免疫)和抗血管生成全家桶方案等。治疗过程中有先化疗再靶向,完全耐药后联合免疫的方法;有先免疫治疗,后线靶向;有在靶向期间穿插放化疗,手术,介入消融等方法;有免疫高表达90 靶向治疗,也有免疫表达阴性免疫治疗的。无法确认最优治疗方案。
♥ 指南中的靶向治疗
» 指南为各病友群大咖们所不齿,常年作为个性化治疗的反面教材各种背锅,但是指南是医生的红宝书,规范治疗要听医生的,由此推论为指南还是要看的。
» NSCLC.NCCN.V6(2020.6.15更新)ALK-Ⅳ期靶向治疗方案:一线首选阿来替尼。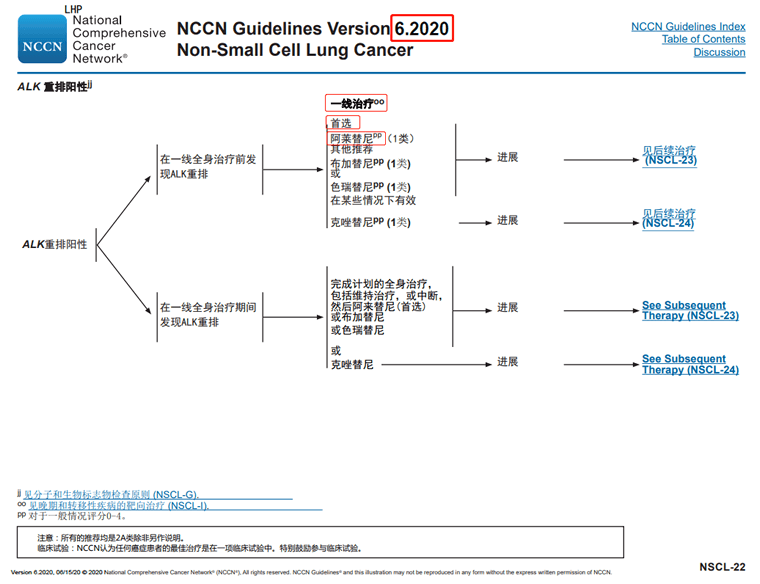
» CSCO.2020 ALK-Ⅳ期靶向治疗方案:阿来替尼(优先推荐)
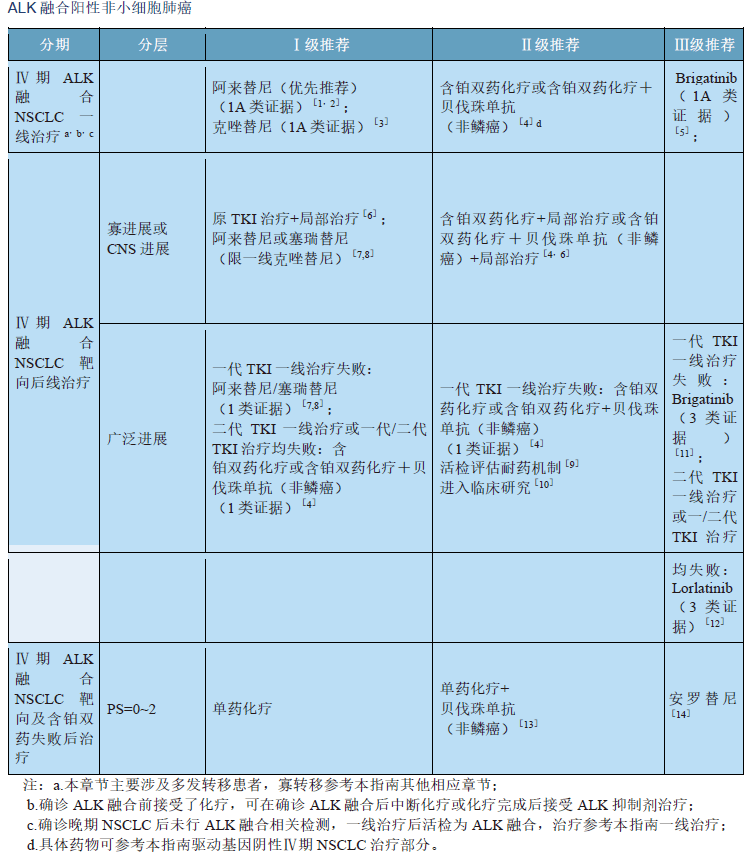 » 一线克和一线阿来替尼。
» 一线克和一线阿来替尼。
阿来替尼是三大指南的一线推荐首选,也是目前最好的ALK靶向药,一线选择主要是颅内控制好,治疗效果好,副作用小,但是相比一线克少用一代药,在病友观察中没有完全实现宣传的超长mPFS。阿来医保前一线选择的关键是经济因素,医保后一线选择的重点是一线阿来替尼的数据仍不够成熟。考虑到一线克有长期使用和CR的概率,可以多用一代药,仍然建议同时保留一线克的选择。具体到个人选择一线克还是一线阿来,暂时没有成熟数据支持。一线克序贯和一线阿来的选择并不是简单的PFS相加,需要考虑到患者自身的肿瘤异质性情况和用药过程中病灶产生的不同变化。总的来说两种方案有小区间的PFS差异,没有OS区别,原则上参考指南和接受主治医生建议。
♥ 靶向治疗
» 靶向药信息(2020.6)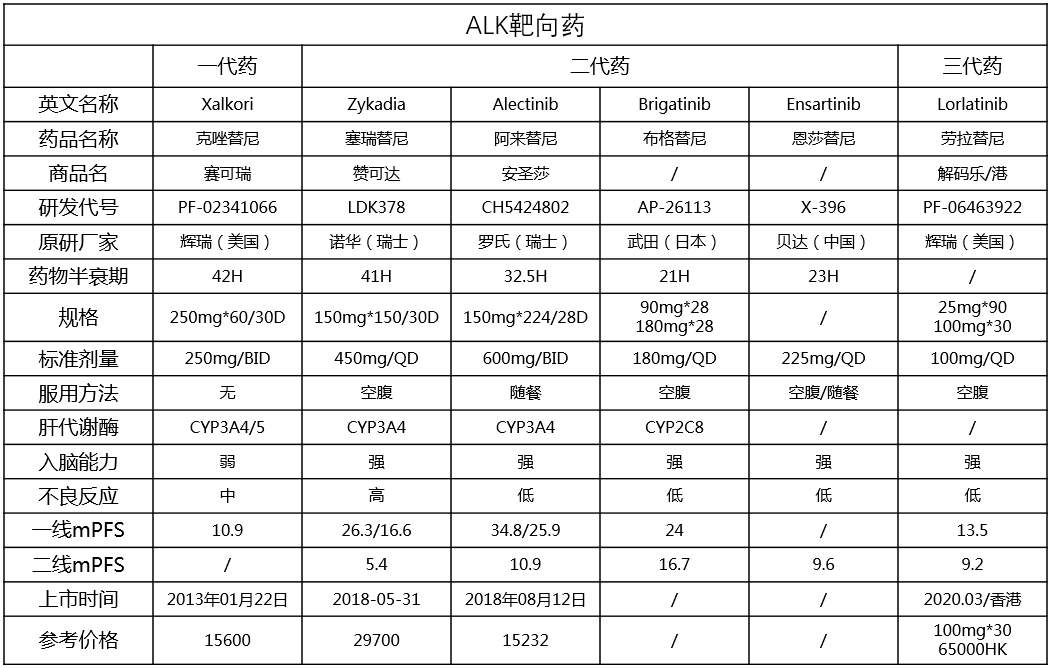 » mPFS的对比
» mPFS的对比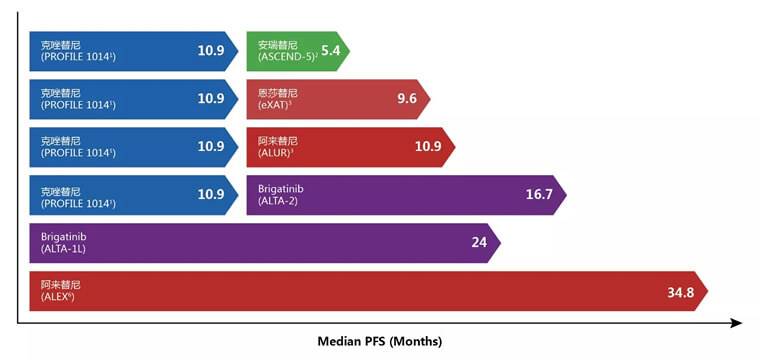 » 靶向药服用应严格按照药物使用说明的用法用量正确服用,不建议自行减量,停用,轮换,脉冲等方法。
» 靶向药服用应严格按照药物使用说明的用法用量正确服用,不建议自行减量,停用,轮换,脉冲等方法。
» 建议服药第一个月入院随访,对比确认疗效和是方案确定。后面随访2-3月一次,骨扫间隔半年以上,吃克脑核磁三个月一次,其他靶向药脑核磁可以半年一次。随访检查项目:CT,脑核磁,腹部B超,心电,血常规,肝肾,肿标等。靶向平稳期,通常CT平扫和血常规必选项,其他项目可轮换做,不是每次随访都必须全套,没有实质性意义。对于每次都开全家桶,且必增强的医生需要留意。
» 靶向治疗在原研过程中经过三期临床试验,且审批保证安全才能用于临床,对多数人药物的毒副作用安全可控。副反应处理轻度可耐受观察即可,中度用药,重度减量或停用。ALK靶向药常见副反应重点关注重度肝损和间质性肺炎。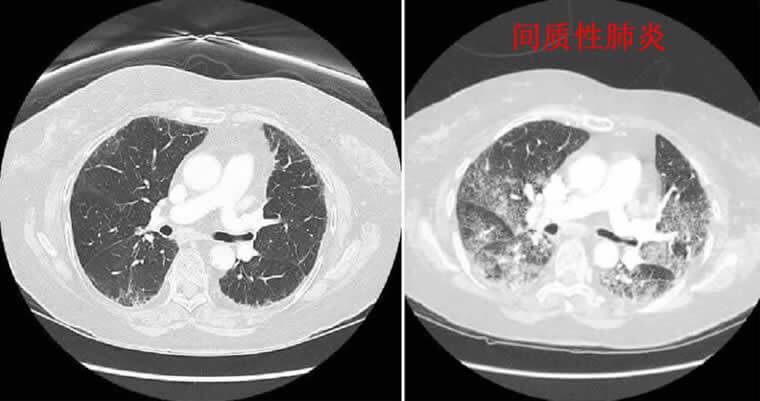
» ALK靶向药随餐服用,用药期间可以服用中药调理,与感冒药,消炎药,抗病毒药物以及激素类药物不冲突,一般建议是靶向药与其他药物服用间隔两小时以上。
» 靶向药耐药标准是正常服用ALK-TKIs一个月内影像判定全面进展(原发灶参考标准,增大20%以上)。局部进展(包含克颅内病灶)不一定耐药,可以在继续原方案基础上进行局部治疗。肿瘤是否进展或耐药以影像结果为准,体感和指标仅做参考,不作为病情的诊断和治疗依据。
» 靶向药耐药后,一线克可以直接换二代,一线阿来或二代药耐药必须基因检测,确定耐药机制和继发耐药基因。
» 一代和二代耐药机制不同,WT为未知突变,ALK突变即病友所讲的耐药基因突变。
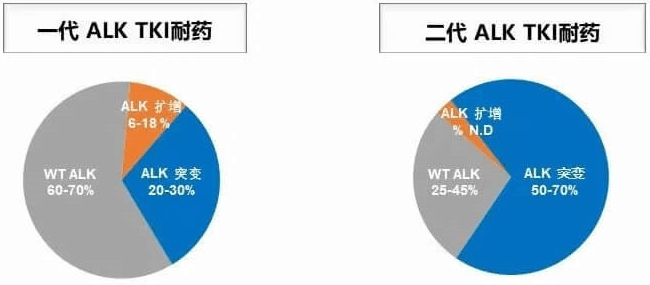
» ALK靶向药的耐药机制有继发性耐药,旁路激活和扩增,以继发性耐药为主,各靶向药常见敏感靶点和耐药靶点如下图。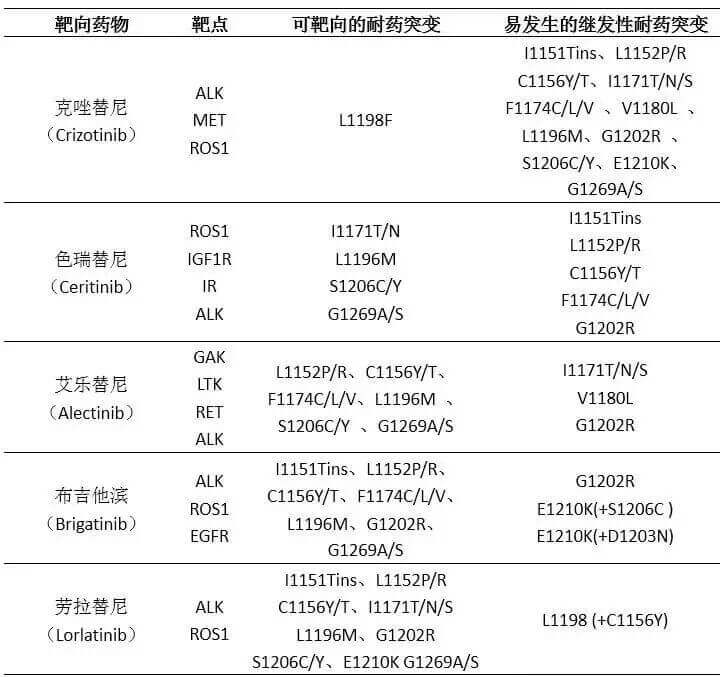
» 各耐药基因发生的概率:
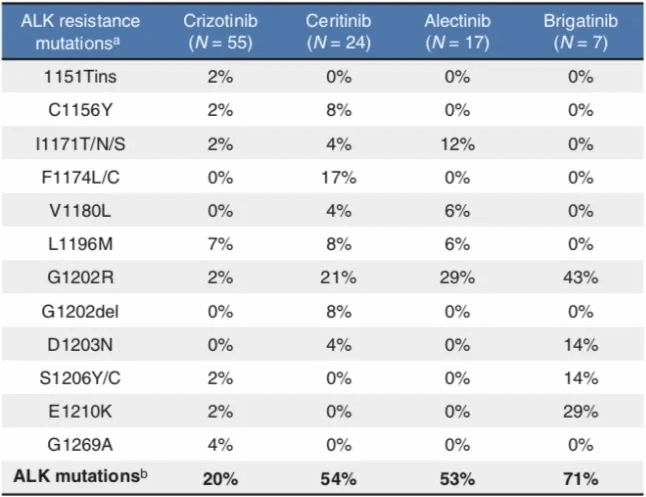
» 耐药后各靶点对应的敏感靶向药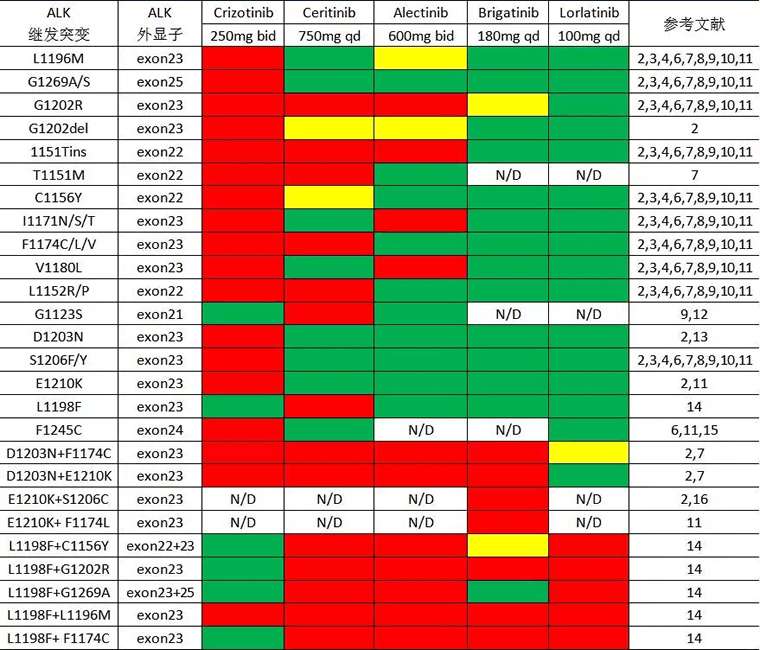
» 各靶向药对靶点的敏感程度
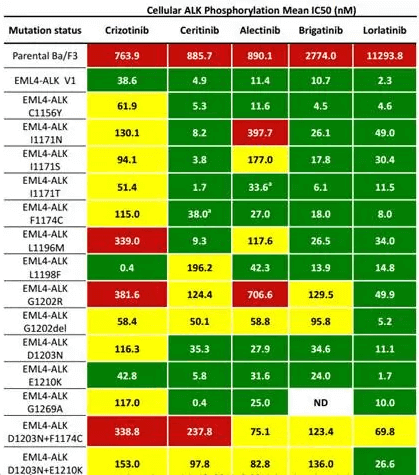
♥ 靶向药耐药后策略
» 一线克唑替尼: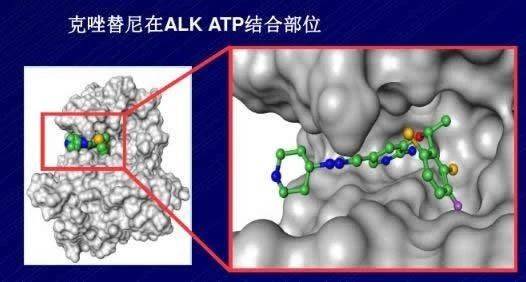
克唑替尼治疗过程中随访需要脑核磁检查。用药影像发现肺部病灶有进展,首先做脑核磁检查。
1. 颅内进展,其他病灶稳定,脑部放疗后继续克。
2. 颅内多发进展,病灶负荷大,不管克是否耐药,应及时更换二代药。
3.颅内无病灶,无其他远端转移,肺部病灶缓慢进展,克联合单药培美或贝伐延缓耐药。
4.克耐药机制以WT为主,对二代药敏感,非必须再次活检和基因检测,考虑到经济因素,能省则省。
» 一线阿来替尼过程中,有间质性肺炎或副作用不耐受必须停药的情况下,阿来没有耐药可以吃回克。有病友在吃克后经主治医生推荐直接入组三代劳拉,节约了费用,但是错过了关键的二代药很可惜。以上两种特殊用药顺序暂不确定对PFS和OS的影响。
» 阿来替尼和骨转
骨转移放在阿来替尼耐药前,因为阿来替尼对ALK专一靶点少,全身抑制效果好,对骨转移控制一直差强人意。
1.双膦酸盐药物(保骨针)属于骨科药,不可用于预防性骨转移,有骨转建议使用。
2.地诺单抗和唑来磷酸对骨转抑制效果无差异,保骨针对肿瘤抑制和骨转引起的疼痛效果不明显。
3.为防止双膦酸盐长期使用导致的下颌骨坏死,保骨针一般使用一年后二代三代互换使用,有数据显示,使用一年后每月滴注和三个月滴注效果相同。
4.部分阿来骨转和阿来进展检测出MET扩增,由MET引起的骨转可考虑:克唑替尼单药,阿来替尼联合280(NC280卡马替尼),阿来替尼联合184(卡博替尼)。克和280是一类met抑制剂,280是met单靶点,副作用小,抑制效果不如克。在克和280都不能有效抑制met的情况下使用二类met抑制剂184。184没有上市,医生通常不会推荐。
5.骨转移早发现早治疗,有疼痛时必须使用止疼药。能够抑制骨转和缓解疼痛的主要方法是放疗,其中非承重骨放疗,承重骨有破坏做骨水泥。
6.骨转进展保骨针和止疼药要用,治疗优先考虑放疗,或尝试184。
» 阿来替尼的ALK继发性耐药突变:
阿来替尼的ALK继发性耐药突变都位于ALK基因第23外显子,最常见同时也是耐药性最强的是溶剂前沿突变G1202R,通过空间位阻限制TKI结合激酶活性部位;其次是V1180L突变(减弱范德华力)和I1171N/S/T突变(氢键断裂)
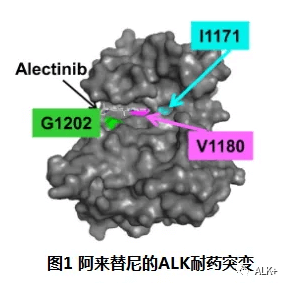
G1202R位阻形成耐药:如图蓝色部位
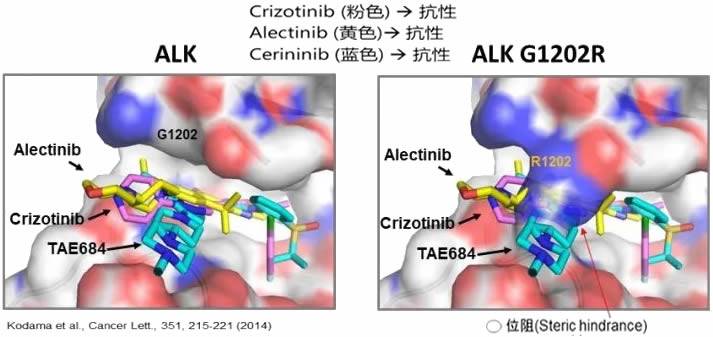
阿来替尼常见耐药基因: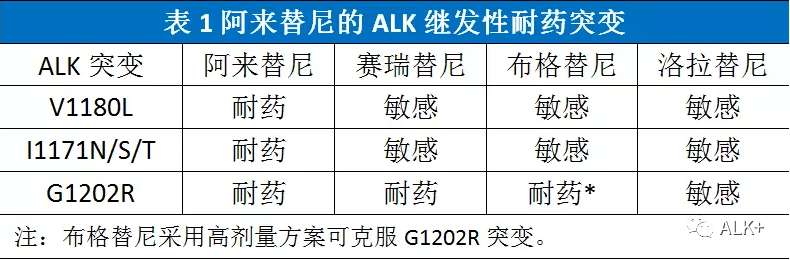
» 阿来替尼耐药后常用策略:
化疗,维持原方案局部治疗,或阿来加量至900BID。
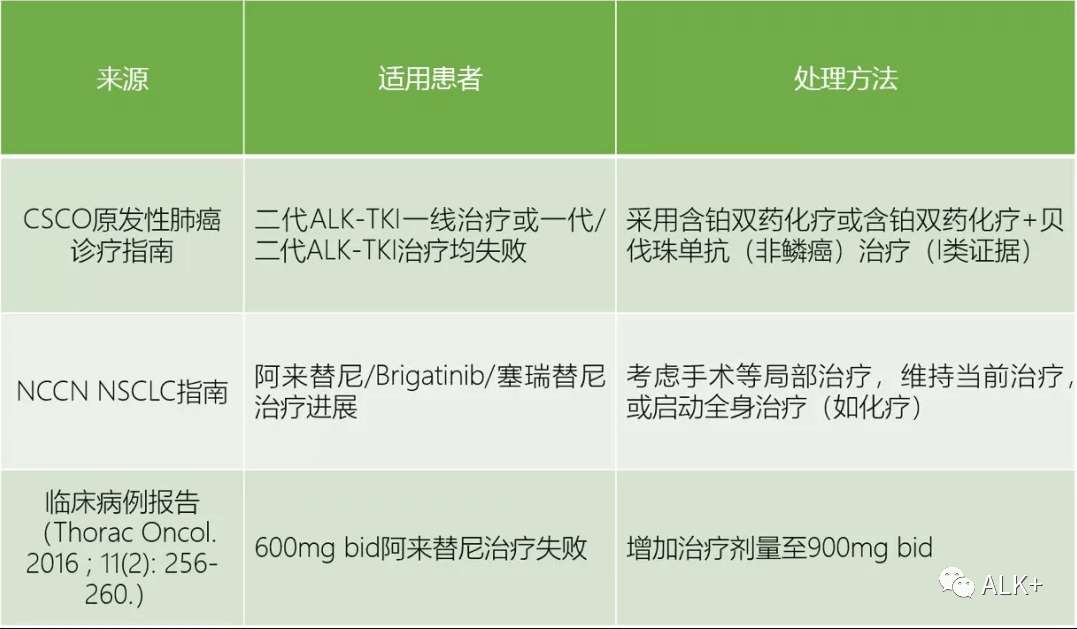
» 阿来替尼→序贯其他ALK-TKI:色瑞或AP
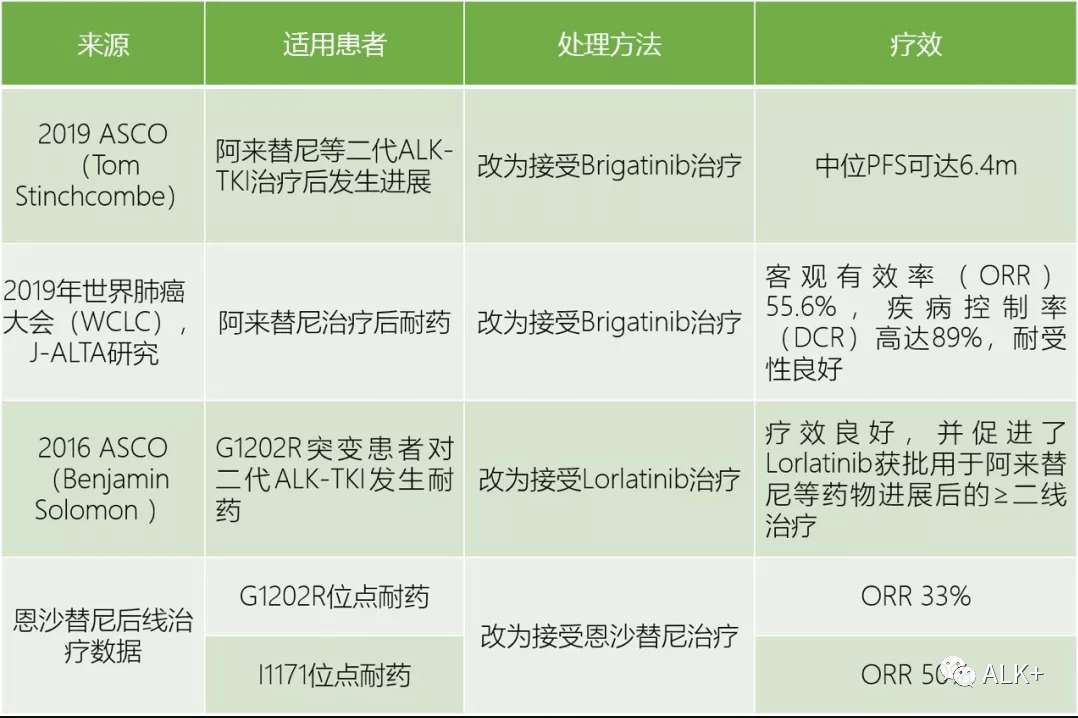
» 阿来替尼耐药后序贯使用布格替尼(AP26113)的疗效:
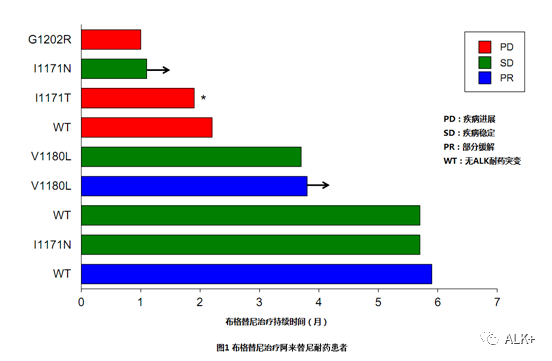
» 阿来替尼→序贯其他治疗手段:
1. ALK-TKI获得性耐药,即非ALK依赖性耐药。机制之一为细胞内旁路激活,此类耐药如有可针对靶点,首选靶向治疗,如EGFR/MET/BRAF/ROS1等靶向药物。
2. 无可用靶向药物时,若PD-L1≥1%,可采用Atezolizumab(Atezo)等免疫单药;若PD-L1不详,不妨采取二线免疫联合治疗。常用升级治疗方案依次为:化疗—化疗 贝伐珠单抗(Bev)—Atezo 化疗—Atezo 化疗 Bev。
3. 当耐药机制属于组织学、表型等改变时,可选择对症治疗或联合治疗。
» 阿来替尼 联合策略:
1. 耐药机制为ALK依赖性耐药中的GCN↑/基因扩增时,可选择ALK-TKI联合Hsp90抑制剂克服ALK基因拷贝增加/扩增耐药。
2. 阿来替尼耐药后,联合贝伐珠单抗继续治疗。2期临床研究证实,阿来替尼耐药后,联用贝伐珠单抗能带来进一步的生存获益:中位总生存期(OS)为32m,DCR达67%。
3. 阿来替尼耐药后,联合化疗继续治疗。多中心回顾性研究显示,在化疗基础上继续联合二代ALK-TKI的患者,相较于单纯接受化疗的患者,PFS更长(6.8m vs 3.2m)。
» 阿来替尼耐药后策略图示:
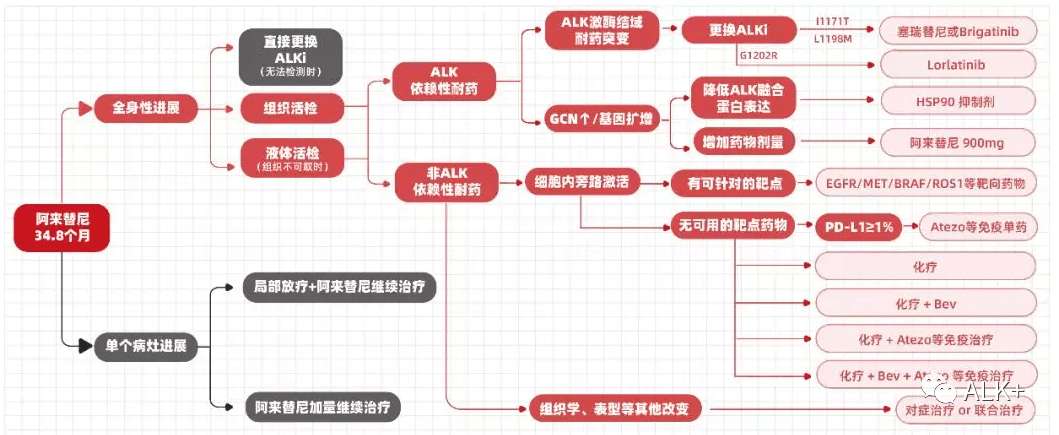
» 阿来替尼耐药后需要再次基因检测:
ALK阳性NSCLC患者在使用二代ALK-TKI耐药后,应该进行二代测序,以决定后续用药方案。
» 其他二代药耐药策略:
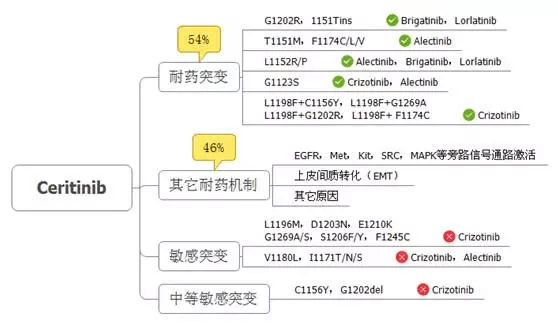
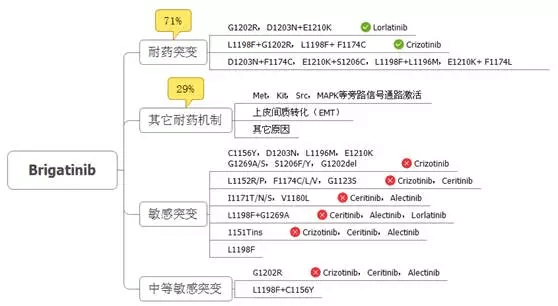
» 劳拉替尼/3922
香港上市时间:2020/03
参考价格:100mg*30,65000HK/月,约合5.94万。
用法用量100mg/qd,目前病友使用原料药较多,爬坡用量。
ALK保底神药,涵盖了ALK激酶端大部分的突变靶点,颅内抑制效率高,但是中枢神经毒性和高胆固醇的副作用发生率较高,不耐受可暂停或减量,缓解后继续使用。
经过多线治疗,肿瘤异质性增加,劳拉耐药机制复杂,以复合耐药为主。需要再次基因检测,目前已知有13种耐药组合可以重回一代/二代逆转劳拉耐药,但缓解效率有限。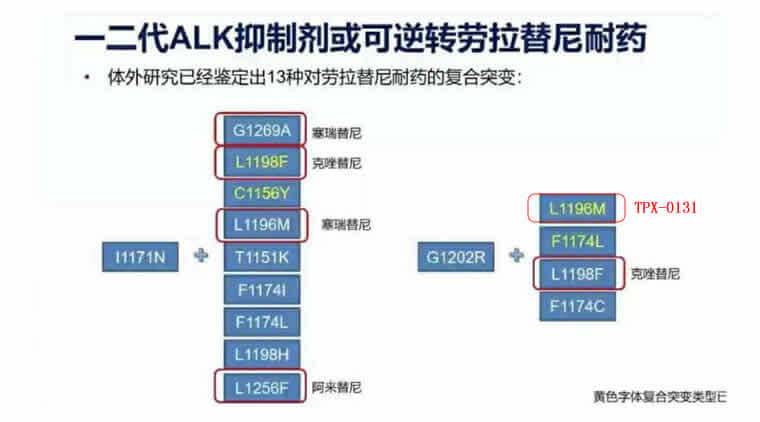
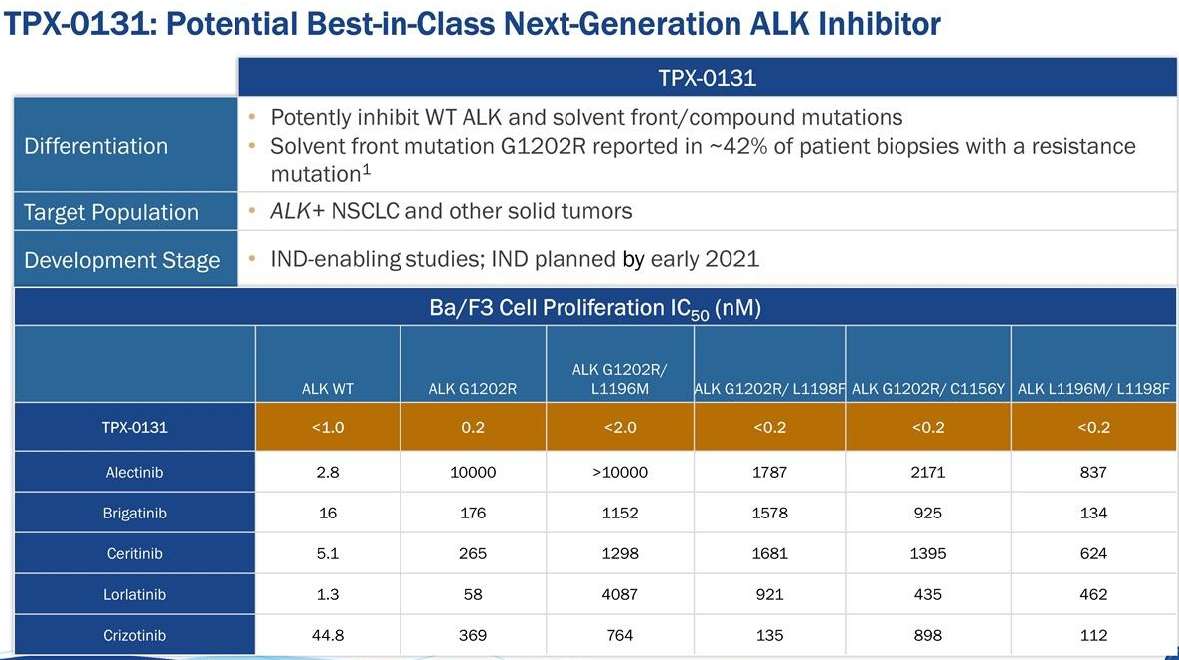
» 在路上的TPX-0131:
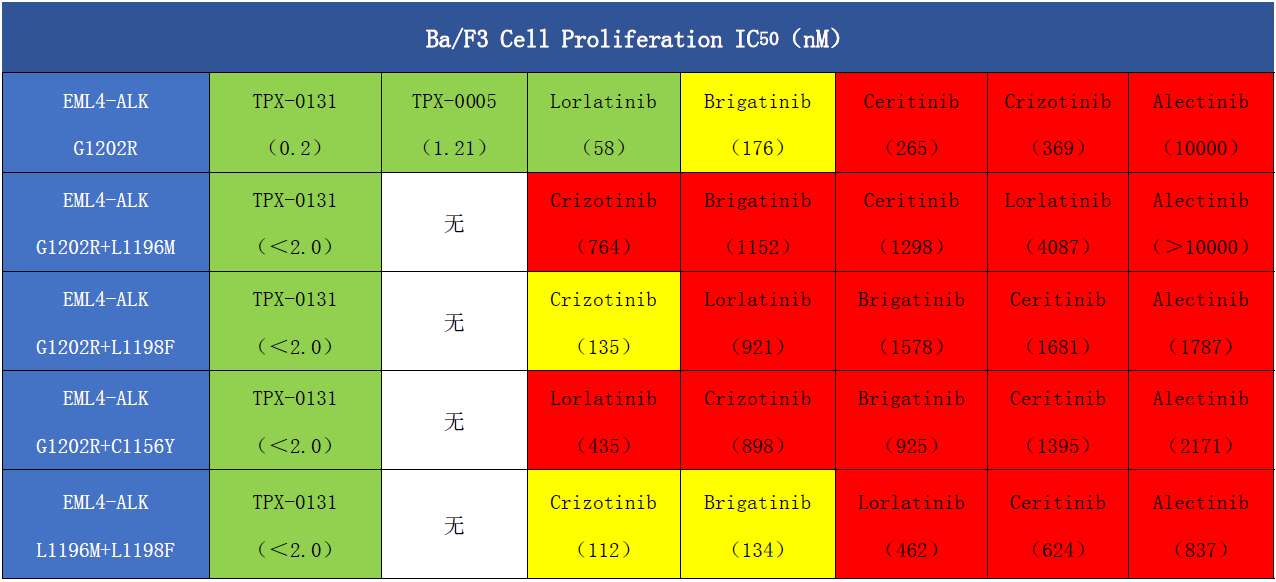
由克唑替尼研发者崔景荣博士主导设计的ALK四代药TPX-0005(洛普替尼),临床实验没有ALK获益,对ROS1显示较好的抑制效果,成为ROS1四代药。TPX-0131为劳拉耐药后的复合突变带来新的希望,尤其对于难以抑制的G1202R和L1196M复合突变有效。信息如下图:
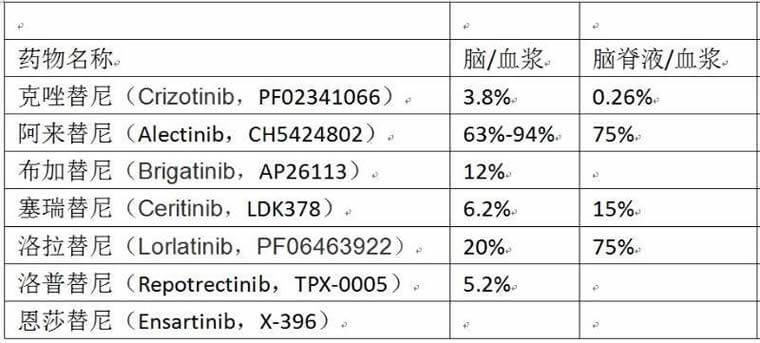
» ALK靶向治疗中的颅内抑制:
ALK靶向药中除了一代克唑替尼因为血脑屏障入脑效率低外,其他靶向药都可以入脑有效抑制,其中以阿来替尼和劳拉替尼入脑最强。加上放疗技术的快速发展,ALK在颅内控制相对较好。但也出现了阿来替尼有效,无法抑制颅内进展的情况,需要联合放疗治疗。
对于颅内进展较为险恶的脑膜转,脑核磁增强检查也很难发现,一般通过腰穿确认,虽然有鞘内注射的方法,可以缓解症状但是无助于改善生存期,预后不良,期待更有效的方法。
♥ ALK的免疫治疗
1.有效率低,通常不会单药,免疫有效也可能是化疗作用,联合治疗初期无法确定是化疗作用还是免疫效果。
2.靶向耐药快,高表达,免疫治疗有效率高。
3.靶向治疗效果好,免疫表达90以上,属于拯救过银河系的人,上帝又开门又开窗。
4.同步放化疗加爱药。
5.耐药后含铂双药联合阿特珠和贝伐全家桶
6.化疗联合O加Y双免疫
突破指南晚期ALK阳性一线靶向治疗的建议,目前有ALK病友尝试一线放化疗加爱药,一线免疫治疗或耐药后免疫治疗,以及双免疫方案,部分显示有效,结果如何尚需验证。通过对ALK病友免疫治疗的跟进分析,ALK的免疫治疗效果与PDL1表达相关度高于是否驱动基因阳性。
♥ ALK靶向治疗碎碎念
1.多种治疗方案,未来可期,但各种治疗方案对生存期的影响不确定,无法确认适合自己的最优方案。
2.除了药物治疗,抗癌的目标是长期带瘤生存,一半治一半养,规范治疗少走弯路。
3.靶向治疗有PFS的差异,没有OS的区别,OS不是各种治疗的PFS相加,治疗结果因人而异。
4. 出现意外的情况包括:随访不及时,脑转,间质性肺炎,严重细菌感染,颈部淋巴结,靶向药不敏感,术后感染,ALK伴KRAS或TP53高丰度,身体情况不好有并发症,体质不佳评分低,肺部病灶进展导致的呼吸衰竭,经济因素等。大约有一半原因并非肿瘤进展造成的。
5.病情观察不能仅仅以可测量病灶大小来衡量,应考虑到肿瘤的恶性程度,扩散程度和不可见病灶。
6.化疗是不可忽视的重要治疗手段,日常调理养好身体,有部分对化疗敏感长期化疗的病例。
» 结束语:生命的尊严和质量应高于治疗,重生之后,生命的价值和深度应高于长度。

声明:
1.以上部分图片来源于网络,如有侵权,请联系删除,信息为病友经验交流,仅供参考,不做任何治疗相关依据。
2.水平有限难免错漏,敬请理解~
收藏
回复(89)参与评论
评论列表
 虚拟的登山鞋
虚拟的登山鞋 欢喜的香蕉
欢喜的香蕉