肌肉减少症的营养治疗
肌肉减少症的营养治疗
(一)肌肉减少症的流行病学及定义
肌肉减少症的概念最初来自于对健康衰老人群的观察,临床发现,随着年龄的增加,老人出现体力、体能下降,进而发现与其骨骼肌肌量减少及功能减退有关,诊断为老年性肌肉减少症(sarcopenia)[1]。据统计,在60~70岁年龄段的老龄人口中,肌肉减少症的发病率为5%~13%; 在80岁以上的老龄人口中,其发病率则高达11%~50%「2]。国内研究显示,上海人群的老年性肌肉减少症发病率为男性12.4%(DEXA诊断) 和23.6% (生物电阻抗法,bioimpedance analysis, BIA诊断),女性4.8% (DEXA诊断)和11.8% (BIA诊断);中国台湾城市人群肌肉减少症的发病率为14.4%[3-5]。
肌肉减少症分为生理性及病理性两类,生理性肌肉减少症如老年性肌肉减少,活动减少如久坐等所致肌肉减少,病理性肌肉减少症又分为良性与恶性两种。
2010年,EWGSOP提出了肌肉减少症定义的欧洲共识。该定义为:肌肉减少症是进行性、广泛性的骨骼肌质量及力量下降,以及由此导致的身体残疾、生活质量下降及死亡等不良后果的综合征[1],并提出了诊断标准,见表10-1[1]。
表10-1 EWGSOP肌肉减少症的诊断标准(2010版本)
以下三条标准符合第1条及第2、3条中任意一条即可诊断为肌肉减少症
1.骨骼肌质量减少未定义
2.骨骼肌力量下降非利手握力<40kg(男性),<30kg(女性)
3.身体活动能力下降步速<0.8m/s
注:*尽管EWGSOP没有对肌肉量减少进行定义,但是一般可以采用如下标准:
1与同年龄、同性别、同种族的正常人相比,肌肉量下降2个标准差(2SD)
2四肢骨骼肌指数(appen-dicular skeletal muscle index,SMI)男性<7.26kg/㎡,女性<5.45kg/㎡
EWGSOP在2019年发表的共识中提出了对肌肉减少症定义的更新[6],实际是对既往肌肉减少症分为肌肉减少症前期、肌肉减少症期和重症肌肉减少症期的内容进行了定义(表10-2),即检测到肌肉量的下降即存在"肌肉减少症"可能,同时存在低肌肉力量、低肌肉重量(含量)或低肌肉质量(密度)则诊断为"肌肉减少症"。肌力、骨骼肌质量以及体能三者的下降,被认为是严重的肌肉减少症。
表10-22018年EWGSOP肌肉减少症的定义更新
当检测到低肌肉力量(1)时,可能会出现肌肉减少症。低肌肉重量(含量)或质量(密度)(2)的存在确诊
肌肉减少症。当检测到(1)低肌肉力量、(2)低肌肉重量或质量和(3)低肌肉机体功能同时存在时,肌肉
减少症被认为是严重的。
(1)低肌肉力量
(2)低肌肉重量或质量
(3)低肌肉机体功能(即体能)
EWGSOP同时进行了肌肉减少症的诊断标准更新(表10-3)

注:ASM,appendicularskele-talmusclemass,四肢骨骼肌量;ASMI,appendicularskele-talmusclemassindex,四肢骨骼肌指数;ASMI=ASM/heighet²; SPPB, short physical perfor-mance battery,短时体能组合;TUG,timed up and go test,起立-行走试验
(二)肿瘤肌肉减少症的概念及与肿瘤恶液质的区分
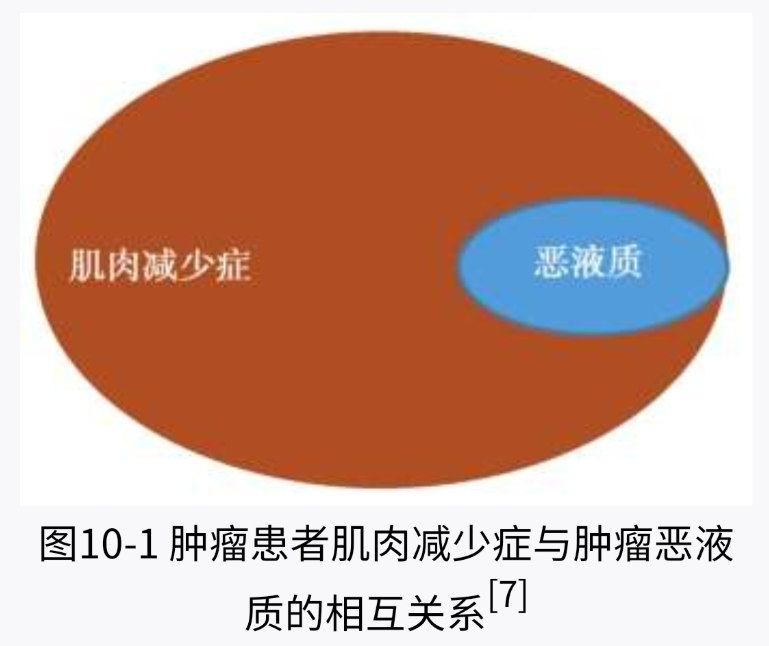
目前没有专门的肿瘤肌肉减少症的定义。首先需要辨析的是肿瘤患者肌肉减少症与恶液质的相互关系。肌肉减少是肿瘤恶液质的重要特征,但肿瘤患者在没有达到恶液质状态时也可能出现肌肉减少。即肿瘤患者有肌肉减少症不一定有恶液质,但肿瘤恶液质患者一定有肌肉减少(图10-1) [7]。恶液质以体重丢失、骨骼肌进行性下降以及炎症状态(或厌食)为特征。而肿瘤肌肉减少症患者没有厌食或炎症状态,其体重也不一定下降。肿瘤患者的肌肉减少症另有一个重要特征是,部分肿瘤患者同时存在骨骼肌减少和脂肪(包括内脏脂肪和皮下脂肪)的增加,因而,肿瘤患者可能表现为体重不下降甚至增加。
(三)肿瘤肌肉减少症具有不良临床结局
肌肉减少症作为一种进行性的全身性骨骼肌疾病,可能会导致不良后果,包括跌倒、骨折、身体残疾和死亡率。肿瘤患者出现骨骼肌减少,不论伴有或不伴有脂肪的变化(脂肪减少、不变或增加),均与患者不良临床结局相关,因此是重要的值得关注的临床问题。预防或改善肿瘤患者的骨骼肌减少有助于改善临床结局。
有研究表明,超重或肥胖患者中的肌肉减少是胰腺癌患者的不利预后因素[8];结直肠癌择期手术患者的骨骼肌量少是住院时间延长的危险因素 (IRR, 1.27; 95%Cl 1.12~1.43),骨骼肌量少联合内脏脂肪(visceral obesity,VO)、肌肉减少和肌肉脂肪变性(myoste-atosis),其延长住院时间的风险为2.98 (OR:2.98; 95%CI1.06~5.46; P=0.038) [9]。 肿瘤患者的肌肉减少性肥胖(sar-copenic obesity)是呼吸道肿瘤、消化道实体肿瘤患者不良临床结局的预测因子[10],而皮下脂肪增加可能是肿瘤患者死亡的独立预测因子[11]。另外,国内余震教授团队的系列研究也显示,肌肉减少症和内脏脂肪增加是消化道肿瘤患者术后近期并发症和远期生存的独立危险因素[12-18],其中包括超重或肥胖患者及无营养风险的患者[19, 20]
(四)肿瘤肌肉减少症的评估
1.骨骼肌量的评估
围度测量和人体成分分析是评价机体骨骼肌肌量的两种方式。围度测量包括上臂肌围和小腿肌围。上臂肌围通过测量上臂围和皮褶厚度后计算得来。小腿围也一定程度反映下肢骨骼肌的肌量,但由于没有测量小腿皮褶厚度以及相应的计算小腿肌围的公式,因此小腿围只能作为参考。通过人体成分分析获得骨骼肌量主要包括以下检测手段:CT、MRI、DEXA、BIA以及B超。EWGSOP共识推荐的是CT、DEXA以及BIA[6]。
CT扫描:L3水平的CT扫描结果反映躯干的骨骼肌量,在临床研究中较多被应用于研究骨骼肌量、骨骼肌减少与不良临床结局的关系。CT测量L3水平SMI,即腹部CT第三腰椎平面骨骼肌面积/身高的平方来计算得出的骨骼肌含量。Prado CM等[19]在1473例肺癌及消化道肿瘤患者中研究发现,CT测量L3水平骨骼肌指数所显示的骨骼肌消耗(有无肌肉减少症),结合体重丢失以及骨骼肌的变薄,可以很好地预测患者生存,且不依赖于BMI。Stene GB等[21]的研究显示,35例接受姑息性化疗的晚期非小细胞肺癌患者在未接受任何恶液质治疗的情况下,近半数患者在化疗期间肌肉质量稳定或增加,提示化疗并未引起患者的骨骼肌减少。目前国际上没有统一的肌肉减少症L3SMI临界值标准(cut-off),更无适合亚洲人群的cut-off值。国内余震教授团队通过对937例胃癌患者进行长期随访发现,肌肉减少症能很好地预测患者的5年生存率,并得出肌肉减少症L3SMI cut-off值男性为40.8cm2/m2,女性为34.9c㎡/㎡[15],该标准目前已被国内外的研究广泛引用或应用[22-24]。不同疾病、不同种族,肌肉减少症诊断的cut-off值存在差异,未来需要更多高质量大样本的研究来验证不同人群肌肉减少症诊断cut-off值的可靠性。
DEXA:DEXA已是常规的人体成分检测手段。1999年开始,美国国家健康与营养调查项目 (The National Health and Nutrition Examination Survey,NHANES) 将全身的DEXA检查纳入8岁以上年龄段健康人营养监测项目,并在美国国家疾病预防控制中心 (Center for Disease Control,CDC) 网站公布[25]。中国台湾学者用DEXA前瞻性研究了34例头颈部肿瘤患者化疗前后以及化疗后2个月的全身瘦体组织(lean body mass,LBM)、脂肪量(fat body mass,FBM)以及骨量 (bone mineral con-tent),结果发现,仅躯干的骨骼肌量有改变,而其余部位(四肢)的肌肉、全身脂肪量及骨量没有变化。JacksonW等[26]用DEXA检测了12例进展期头颈部鳞癌患者在放化疗前、治疗期间及治疗后的人体成分,结果发现,治疗期间LBM较基线下降了10.2%,FBM下降了11.1%,治疗结束后LBM趋于正常,而FBM继续下降。Wallengren O等[27]在779例晚期肿瘤患者的DXA数据中,诊断出有471例患者在过去2年中有肌肉丢失,结果显示肿瘤患者的肌肉丢失与年龄、性别、肿瘤类型以及炎症状态相关。
BIA: BIA通过测量骨骼肌的电阻抗计算四肢及躯干骨骼肌量,以得到四肢骨骼肌指数(muscale index) [3-6]。
2.对肌力的评估
握力(grip strength)是常用、简便且成本低廉的测量肌力的方法,也被临床研究广泛采用,用于检测肌力与临床结局的相关性以及干预的效果评价[28]。呼吸峰值流速(peakexpi-ratory flow,PEF)又称最大呼气流量,是指测定肺活量过程中,气体从肺部通过口腔用力呼出达最快时的瞬间流速。结合PEF(反映肌力)、BIA (肌量)与常态步速(usualgaitspeed,反映体能) 能全面诊断肌肉减少症[6]。
3.对体能的评估
建议进行肌肉功能性测量,即对体能进行测量来评估肌肉减少症的严重程度。推荐的体能评估方法包括:短时体能测试组合 (short physical performance battery,SPPB) [29,30]、起立-行走试验(timed up and go test, TUG)[31]和400m步行测试[32]。
4.综合评估
鉴于肌肉减少症的诊断需要评估其肌量、肌力及体能水平,因此,诊断肌肉减少症需要结合这三方面的指标[6]。不同的测量工具获得的骨骼肌水平不同,其诊断得到的肌肉减少症的发病率也有不同,因而诊断一定要结合具体的检测方法(或测量工具)。
肌肉减少症的营养治疗
(一)抗阻运动
尽管肌肉减少症的发病原因及病理生理机制仍然没有完全阐明,但是有一点非常明确,缺乏身体活动(physical activity,PA)或PA水平下降是所有肌肉减少症的共同的主要原因之一。所以,PA对肌肉减少症的作用意义重大,不仅可以预防、减缓肌肉减少症,还可以有效治疗肌肉减少症。运动 (锻炼) 是PA的一种,是一种主动的、以增强体质为目的的PA。对所有人,尤其是老人,与其他任何干预手段相比,运动是一种最为有效的改善生活质量、提升身体功能、减少/减缓慢性病 (包括肌肉减少症及肿瘤)的措施。运动的方式方法很多,其中以抗阻运动(resis-tance exercise,RE)对肌肉减少症最为有效。
LenndersM等[33]研究证实,在进行为期24周的运动干预后,老年男性和女性的坐立时间(与身体功能成反比)较干预前分别下降了18%±2%和19%±2%<0.001)、糖化血红蛋白水平较干预前均显著降低(P<0.02)、肌纤维的横截面积均显著增加(P<0.01)。研究结论认为,老年人群进行阻力训练后可以预防肌肉质量的下降,同时显著提高肌肉力量。
Zampieri S等[34]研究发现,运动可显著改善老年人群骨骼肌生物学指标及肌纤维超微结构。Zampieri S等对经常进行体育锻炼的老人 (每周常规锻炼3次以上)、同等年龄仅进行日常活动的健康久坐老人及经常进行体育锻炼的年轻人 (平均年龄27岁)分别进行了研究,发现经常锻炼的老人的骨骼肌形态及功能、肌纤维超微结构以及线粒体功能等生物学指标与经常进行体育锻炼的年轻人较为相似,而缺乏运动的老年人群上述各项指标均出现较为明显的退化。研究得出结论:体育锻炼可以显著延缓年龄相关的骨骼肌功能衰退。
Henwood TR等[35]报告,社区老人高速度抗阻训练8周后,肌肉力量显著增强,P<0.01;仰卧起立 (floor rise to stand-ing)增加10.4%±11.5%,P=0.004; 6m 步行增加6.6%±8.2%, P=0.010; 坐位起立 (repeated chair rise)增加 10.4%±15.6%,P=0.013;上举 (lift and reach) 增加25.6%±12.1%,P =0.002。结论认为:渐进性抗阻训练(progressive resistance train-ing,PRT)对老人是安全有效的,可以显著改善肌肉力量、肌肉强度及体能,从而提高并改善生活质量。
Galvão DA等[36]的研究证实,通过RE和有氧运动的组合,可有效对抗晚期前列腺癌雄激素抑制疗法 (androgen suppres-sion therapy,AST) 对于骨骼肌的负面效应。57位接受AST的前列腺癌患者被随机分为两组,其中试验组29人接受RE和有氧运动训练,对照组28人接受常规治疗。在观察终点(12周后)观察瘦体组织、肌力、心肺功能、生活质量等指标。结果显示,试验组瘦体组织较对照组显著增加 (上肢,P<0.001;下肢,P=0.019),运动尚可提高生活质量 (P=0.022),降低体内C反应蛋白水平(P=0.008)。RE对时间及设备的要求并不高,每周两次,每次30min,徒手(如伏地挺身、俯卧撑)或借助健身器械(如弹力带)等即可完成训练。此外,还有研究直接观察到RE对大腿中部肌肉横断面面积、膝伸肌扭矩的改善作用。
Liu CK等[37]报道了PA干预对提高老龄(70~89岁) 肌肉减少症人群 (n=177) 机体活动能力的影响。研究者对老年肌肉减少症患者进行了以步行为基础的为期12~18个月的PA干预,包括有氧、力量、平衡和灵活性等训练。研究人员发现,PA干预后老年肌肉减少症患者的步行速度及机体活动评分显著上升。研究得出结论:PA干预可显著提高老年肌肉减少症患者的骨骼肌功能及机体活动能力。
PA同时是恶液质或骨骼肌减少症患者维持肌肉质量的主要手段之一。最近的一项系统性综述显示,在筛选了3000多份文献后发现,大多数研究只在肿瘤患者中进行了运动训练,而不是在肿瘤恶液质患者中进行锻炼[38],证实了在肿瘤患者中进行PA的安全性和广泛性。少数研究调查了运动训练干预对肿瘤恶液质患者的影响。
Sasso JP等[39]针对非恶液质的肿瘤患者给出了运动处方:设定运动心率为最大心率50%~75%的运动量为目标,运动频率为每周运动2~3次,持续10~60min,时间周期为12~15周。
(二)蛋白质摄入
增加蛋白质摄入是肌肉减少症的主要营养干预方式。肌肉蛋白质合成 (muscle protein syn-thesis,MPS)与肌肉蛋白质分解(muscle protein breakdown,MPB)的动态平衡是维持骨骼肌肌量 (skeletal muscle mass)的重要保障,是机体严密调控的结果。RE及摄入蛋白质增加肌肉蛋白质合成主要是通过哺乳动物雷帕霉素靶向蛋白 (mam-malian target of rapamycin,mTOR)通路实现的,p70S6激酶 (p70S6 Kinase,p70S6K) 是mTOR通路的主要下游产物,负责启动蛋白质翻译,与肌肉大小的长期变化有关,所以,p70S6K常常用作MPS的代表。氨基酸尤其亮氨酸是mTOR通路的主要营养调节物质,可增加MPS。人体对MPS的调节要比对MPB严密得多,正因如此,研究上常常用MBS作为观察对象,而不是MPB。蛋白质摄入不仅促进MPS,而且呈剂量效应关系。
D'Souza RF等[40]观察了46例男性老人,RE后立即口服无能量饮品 (安慰剂)或含10g、20g、30g、40g乳清蛋白饮品,观察肌肉活检标本运动前、运动后2h及4h氨基酸水平、p70S6K磷酸化情况,发现单纯RE降低了肌肉内BCAA水平,而口服10g、20g乳清蛋白防止了BCAA的下降,大剂量(30g、40g)乳清蛋白则显著增加了肌肉BCAA水平;运动后2h p70S6K (Thr389)表达情况、肌肉内亮氨酸含量与乳清蛋白摄入量呈显著正相关(r=0.51,P<0.001; r=0.32, P=0.026) 。D'Souza RF等的研究非常明确地说明蛋白质补充能够促进MPS,而且具有剂量效应关系。此后,人们关心的下一个问题是选择什么样的蛋白质?乳清蛋白还是酪蛋白?动物蛋白质还是植物蛋白质?
Wilkinson SB等[41]比较了等氮、等能量、宏量营养素配对的豆饮品和乳饮品对RE后肌肉蛋白质代谢的影响,发现两种饮品均导致正净蛋白平衡(net pro-tein balance,NPB),但是乳饮品的NPB曲线下面积及肌肉内分数合成率 (fractional synthesis rate,FSR)显著大于豆饮品。说明豆、乳均具有良好的肌肉维护及增强作用,但是乳的作用更大、更强。BurdNA等[42]将14名老年男性志愿者分为两组,分别口服20g乳清蛋白或酪蛋白,发现口服两种蛋白后,血浆BCAA及亮氨酸浓度均显著升高,峰值在口服后60min,但是乳清蛋白组升高更加显著(P<0.05),乳清蛋白组大腿MPS比酪蛋白组更高(P<0.05)。结论认为,乳清蛋白比酪蛋白可以更好地促进蛋白质合成,其机制可能与乳清蛋白组血浆BCAA及亮氨酸水平更高有关。ReitelsederS等[43]报告口服乳清蛋白后血浆胰岛素及亮氨酸水平、真核转录因子4E结合蛋白显著高于酪蛋白组。
在维护肌肉并促进肌肉蛋白质合成方面,乳清蛋白优于酪蛋白、乳蛋白优于豆蛋白。蛋白水解物可以更好地发挥作用。其机制在于口服乳清蛋白或乳蛋白后,血浆胰岛素、BCAA及亮氨酸水平更高。除此之外,Mitchell CJ等[44]还在p70S6K磷酸化方面找到了答案。他们招募13名60~75岁男性志愿者,下肢剧烈RE后,立即口服30g大豆蛋白或碳水化合物,分别于休息状态、空腹及运动后2h、4h活检肌肉,以Western blot检测p70S6K磷酸化状况,并与以前口服30g乳清蛋白或安慰剂的数据进行比较发现:乳清蛋白口服组运动后2h、4h p70S6K磷酸化均增强;而大豆蛋白口服组只在运动后2h p70 S6K磷酸化增强,4h则无此作用;碳水化合物口服无增强p70 S6K磷酸化作用。结果提示:乳清蛋白可以持续促进蛋白质合成,而大豆蛋白的作用时间则较短。
临床上,口服蛋白质制剂有整蛋白制剂及水解物(短肽,游离氨基酸)制剂两种,哪一种制剂对肌肉合成更好呢?TangJE等[45]比较了快消化蛋白 (水解乳清蛋白、分离大豆蛋白)与慢消化蛋白 (胶质酪蛋白) 对MPS的影响,青年健康志愿者单腿剧烈RE后随机分为3组,立即分别口服等氮水解乳清蛋白、分离大豆蛋白或胶质酪蛋白,发现乳清蛋白组血浆必需氨基酸(essential amino acid,EAA)、BCAA及亮氨酸水平显著高于豆蛋白及酪蛋白组 (P<0.05),休息时(非运动腿)快消化蛋白组(乳清蛋白、豆蛋白)MPS高于慢消化蛋白组 (酪蛋白)[乳清蛋白=(0.091±0.015) %/h,豆蛋白= (0.078±0.014) %/h,酪蛋白 = (0.047 0.008) %/h],乳清蛋白组 MPS比酪蛋白组高93% (P<0.001),比豆蛋白组高18% (P<0.067) ; RE后MPS情况与休息时类似 (乳清蛋白>豆蛋白>酪蛋白),乳清蛋白组比酪蛋白组高122%(P<0.001),比豆蛋白组高31%(P<0.05)。豆蛋白组休息时、运动后MPS均高于酪蛋白组(休息时高64%,运动后高69%,P均<0.001)。结果认为蛋白水解物可以更好地发挥作用,无论是休息时还是运动后,快消化蛋白比慢消化蛋白能够更高地诱导肌肉蛋白质合成;尽管都是快消化蛋白,乳清蛋白比豆蛋白更好地诱导运动后的肌肉蛋白质合成。其机制主要与蛋白质消化速度有关,也可能与亮氨酸浓度有一定的关系。
另外,整蛋白(分离乳清蛋白)和蛋白水解物(水解乳清蛋白) 复配的肠内营养制剂乳清蛋白粉,可能更有益于诱导肌肉蛋白质合成[46]。
(三) β-羟基-B-甲基丁酸盐
HMB是一种五碳有机酸,是必需氨基酸亮氨酸代谢过程中产生的天然产物。HMB可能通过减少炎症反应来增加蛋白的合成,增加IGF-1并通过激活雷帕霉素靶蛋白 (mammalian target of rapamycin,mTOR)促进蛋白质转化;HMB也可能通过负调节泛素-蛋白酶体通路以及减弱半胱天冬酶的活性来减少蛋白质分解。另外,HMB可能增加卫星细胞活性,增强肌肉再生能力[47]。可能对肿瘤肌肉减少症的预防和治疗有益处。
Nissen SL等[48]发现HMB是唯一可减少肌肉蛋白分解的有效成分。花超等[49]给300例65岁以上社区老人(营养不良组)服HMB (2.6g/d),发现口服90天后四肢肌肉组织较对照组增加,差异有统计学意义。HMB补充剂可以增加老人肌肉含量,有预防肌肉减少的作用,提升机体功能和生活自理的能力。添加乳清蛋白和HMB的强化蛋白复合粉III型有助于保护肌细胞膜,延缓肌疲劳,提升肌耐力,抑制肌蛋白分解[50]。HMB还被证明有助于促进伤口愈合[51];保留卧床期间的肌肉量[52];减轻炎症反应、缩短ICU住院时间、降低死亡率[53];有效预防晚期肝癌患者索拉非尼相关的手足皮肤反应[54];增加IV期肿瘤患者瘦体组织[55]。
(四)维生素D
维生素D与骨骼肌细胞表面的维生素D受体结合,促进肌蛋白合成及钙离子内流。低维生素D水平可导致明显的2型肌纤维萎缩,现已有相对充分证据提示低维生素D水平与肌肉减少症发生密切相关,但对于维生素D补充疗法是否能改善肌肉功能仍存争议。
目前关于维生素D干预肌肉减少症的随机临床研究证据主要来自对非肿瘤的老年性肌肉减少症的研究,且研究结论不一致。Latham NK等[56]2003年报道的一项多中心随机临床研究显示,口服维生素D单剂300000IU (108例) 与口服安慰剂(144例)相比,其3个月的身体状况评分以及6个月内的跌倒次数均无显著差异。2018年Cuel-lar WA等[57]报道的一项RCT研究显示,对老人群给予12个月的维生素D补充治疗后,骨骼肌(腹直肌、腹横肌、内斜肌、外斜肌等腹部肌肉)的大小(肌肉收缩后的厚度)和功能与安慰剂组相比均无显著的组间差异。而2019年Wang J等[58]发布的基于人口的横断面研究(n=5 012)显示,50岁以上男性人群中,惯用手握力与血清中25羟维生素D浓度显著相关,揭示维生素D对中老年男性骨骼肌功能具有显著影响。2005年SatoY等[59]报告的随机临床试验则得出了完全相反的结论,96例脑卒中后偏瘫的老年女性患者,随机分为每日口服维生素D1000 IU组或安慰剂组,随访2年,结果发现,所有患者血浆25羟维生素D基线水平均低(<10ng/ml)。维生素D治疗后,血浆25羟维生素D、1,25-二羟维生素D水平明显升高,跌倒次数减少59% (95%CI 28%~81%; P=0.003),2型肌纤维数量及体积增加。髋关节骨折发生率4/48(安慰剂组)、0/48 (维生素D组),P=0.049。结论认为:小剂量维生素D长期口服有助于防止2型肌纤维萎缩,从而增强肌力,进而防止跌倒及髋关节骨折。但无肿瘤肌肉减少症患者的维生素D干预研究。
(五) 肌酸
磷酸肌酸(creatine phos-phate)是骨骼肌中能量的储备形式,而肌酐是骨骼肌内磷酸肌酸的代谢物,骨骼肌持续产生肌酐,因而临床上通过血液及尿中肌酐水平反映健康及疾病个体的骨骼肌及蛋白质代谢。但研究显示,在结直肠癌患者中,血液肌红蛋白及肌酐水平并不能反映骨骼肌量及有氧运动能力[60]。给予水化肌酸能提高肌肉磷酸肌酸水平,从而可能有助于提高运动能力[61]。Chrusch MJ等[62]在30例年龄超过70岁的老年男性中开展了一项双盲安慰剂随机对照研究,发现肌酸加训练组与安慰剂加训练组对比,前者能有效提升腿力、爆发力及耐力。在一项针对65~86岁老人的研究发现,补充14天肌酸可改善最大等距握力 (maximal isometric grip strength)以及疲劳时的工作能力[63]。低剂量肌酸联合蛋白质补充剂可增加瘦体组织及上臂力量[64]。研究显示,结合运动,肌酸有助于增强肌肉减少患者的运动效果。但尚缺乏对肿瘤患者进行肌酸干预以防治肌肉减少的临床研究。
(六)肉碱
肉碱(L-carnitine)是一种具有生物活性的低分子量氨基酸,人体中的肉碱超过90%存在于骨骼肌中。肉碱是体内,尤其是肌肉内,代谢长链脂肪酸所必需的营养素。食物可提供一部分肉碱,人体肾脏及肝脏也可内源性合成。研究显示肿瘤患者血浆肉碱水平下降,可能与肿瘤恶液质患者的肌肉减少有关[65]。以防止肿瘤患者肌肉减少为目的肉碱干预临床研究尚未见报道。有2项动物研究提示肉碱可能通过促进肉碱脂酰转移酶活性,改善恶液质的肌肉减少[66,67]。
(七)药物
多种可能有助于改善肿瘤患者肌肉减少的药物主要基于对肿瘤恶液质患者的研究,其机制可能在于促进肿瘤患者的肌肉合成代谢和抑制分解代谢。
非甾体的选择性雄激素受体调节剂(selective androgen re-ceptor modulators,SARMs)类药物近年研究较多,它们具有促进合成代谢的作用,却无甾体类药物的不良反应,在治疗肿瘤患者的肌肉减少中初见成效[68]。其中Ostarine在肿瘤恶液质患者的肌肉减少中被证实确有效果[69, 70]
一种促胃液素类似物RC-1291的随机临床试验研究显示其具有促进食欲及肌肉蛋白质合成代谢的作用,可达到改善总体重、瘦体组织及握力的效果[71]。
(八) 鱼油
鱼油是一种从多脂鱼类提取的油脂,富含ω-3 PUFA (DHA和EPA),对心血管、视力、认知功能及骨骼健康具有良好的改善作用[72-74]。近期,越来越多的证据表明,ω-3 PUFA具有促进骨骼肌合成代谢的作用,对老年人群补充ω-3 PUFA,具有预防和治疗肌肉减少症的作用[75-77]。2019年DupontJ等[78]对ω-3与肌肉减少症之间的关系进行了系统性的总结与分析,发现对绝经后妇女给予6个月的鱼油(每天1.2gEPA和DHA)补充治疗后,其步行速度显著增加;对65岁以上健康老年人群给予8周的鱼油(每天1.86g EPA和1.5g DHA) 补充治疗,可以大幅度增加骨骼肌蛋白质合成;对60~85岁的老年人群给予6个月的鱼油补充治疗,可显著增加其下肢肌肉含量和骨骼肌功能。
(九)综合干预
2010年发表的肌肉减少症预防与处理专家共识指出[79]:运动(RE及有氧运动均可)结合足量的蛋白质、能量摄入是防治肌肉减少症的关键措施,单纯的足量蛋白质补充只能减慢肌肉量的丢失,足量的蛋白质(富含亮氨酸的平衡氨基酸以及肌酸)摄入可增强肌力。25羟维生素D水平下降时需补充维生素D。
肌肉减少症的营养治疗
1.肿瘤患者建议在进行营养评估时,同时进行肌肉减少症的诊断。(B)
2.建议用DEXA、生物电阻抗或CT扫描评估肿瘤患者骨骼肌肌肉量。(A)
3.需要关注伴有体脂肪(包括腹部脂肪及体脂肪)增加的肿瘤肌肉减少症患者,因为其往往预测不良临床结局。(B)
4.对于有体重丢失(或有营养不良)的肿瘤肌肉减少症患者,建议补充足量的蛋白质、能量,有助于预防甚至逆转肿瘤肌肉减少症。(A)
5.蛋白质的补充肿瘤肌肉减少症患者推荐的总蛋白质摄入量为1.2~1.5g/(kg·d)(B) ;推荐蛋白质补充时补充平衡氨基酸,尤其建议在饮食中增加富含亮氨酸的平衡必需氨基酸 (B);乳清蛋白优于酪蛋白,乳蛋白优于豆蛋白,蛋白水解物可能更好地发挥作用(C)。老年肿瘤患者的肌肉减少症可能需要更多的蛋白质摄入,以保证蛋白质合成(A)。
6.肌酸的补充 肌酸有助于增强肌肉减少患者的运动效果。(C)
7.维生素D的补充所有肌肉减少患者均应该检测25羟维生素D水平(A)。维生素D补充可成为肌肉减少症的联合治疗措施之一(B)。
8.运动治疗 (体育锻炼/运动疗法)流行病学研究证实了体育锻炼对肿瘤患者健康的正面作用;有氧运动可以改善生命年质量 (quality of life years),其成本效益比良好;短期的阻抗训练可以提高肌力及步速;RE和有氧运动建议每周3次,每次20~30min。(B)
9.药物治疗 可能是肿瘤肌肉减少症患者的新的选择。(B)
10.联合治疗 联合药物、营养和运动的综合疗法可能是防治肿瘤患者肌肉减少的最有效办法。(C)
收藏
回复(1)参与评论
评论列表
























