肿瘤治疗期间恶心和呕吐的预防与治疗
肿瘤治疗期间恶心和呕吐的预防与治疗
Franziska Jahn 糖果读书笔记
2025年03月03日 12:09 北京 1人
肿瘤治疗期间恶心和呕吐的预防与治疗
好雨知时节,当春乃发生。随风潜入夜,润物细无声。-- 杜甫《春夜喜雨》
背景
恶心和呕吐是肿瘤治疗常见且令人痛苦的副作用。尽管采取了预防措施,仍有40% 至50% 的患者会经历恶心,20% 至30% 的患者会出现呕吐。因此,抗恶心药物的预防和治疗对于改善患者生活质量和防止如肿瘤消耗症等后遗症具有重要意义。
方法
这里提供的建议基于国际和国家的指南,并结合通过在PubMed和Cochrane Library数据库中进行有选择搜索获取的文献进行更新,特别关注自德国临床实践指南发布以来过去5年内发表的随机对照试验和.meta分析。
结果
基于对治疗相关和患者特定风险因素的识别,风险调整后预防和治疗方法得以制定,包括女性和年轻年龄等因素。静脉肿瘤治疗被分为四个风险等级(最低、低、中等、高),而口服肿瘤治疗则分为两个等级(最低/低、中等/高)。在放疗中,辐射场的选择至关重要。最常用的抗恶心药物包括5-HT3受体拮抗剂(5-HT3-RA)、NK1受体拮抗剂(NK1-RA)和地塞米松;奥氮平作为辅助或救援药物被证明是有益的。关于在使用包括免疫检查点抑制剂的药物组合治疗的患者中使用类固醇的讨论存在争议,因为这可能会降低治疗反应。苯二氮平类药物、地美辛等也被提及,大麻素可以作为备用止吐药,针灸/压穴、姜和渐进性肌肉放松是可能的替代方法。
结论
目前针对接受经典化疗方案或联合放疗和化疗的患者,已有详细、有效、适应风险特征的恶心和呕吐预防与治疗算法。对于在门诊环境中进行多天口服肿瘤治疗的患者,最佳症状控制仍然是一项挑战。
恶心和呕吐(呕吐)是显著影响患者生活质量的症状。尽管进行预防,接受癌症系统治疗的患者中约有20% 至30% 会出现呕吐,40% 至50% 会出现恶心。这些治疗的不良反应带来了额外的风险,因为它们加重了食欲减退和体重下降,从而增加了癌性消耗症的风险,后果深远。尽管近年来针对接受经典化疗药物的患者恶心和呕吐的预防与治疗已建立起复杂的推荐方案,但新抗肿瘤药物的快速发展,尤其是口服多日方案,给止吐药物的预防带来了新的挑战。哪些癌症药物需要止吐药物的预防?推荐使用哪些止吐药物?它们应使用多长时间?
肿瘤恶病质的风险
呕吐和恶心加剧了食欲丧失和体重减轻,从而增加了癌性恶病质的风险。
定义
恶心和呕吐症状群的定义基于症状出现的时间。
本文概述了经典化疗和放疗的基本原则和建议,以及针对“现代”癌症化疗药物的呕吐风险分层和抗恶心药物预防及治疗的建议。
学习目标,阅读完本文后:
(1)了解癌症患者恶心和呕吐的重要鉴别诊断; (2)能够制定合理的抗恶心药预防计划; (3)熟悉用于预防、治疗和急救治疗的有效抗恶心药物。
方法
在撰写本文过程中,纳入了国际和国家指南。通过在PubMed和Cochrane图书馆进行选择性文献更新搜索,检索了过去5年内发布的随机对照试验和Meta分析,这些文献是在S3指南《癌症患者支持治疗》发布后出现的。
定义
在癌症治疗过程中,食欲丧失、恶心和呕吐形成一个相互关联的症状复合体。经典定义是基于症状出现的时间:急性症状是指在治疗当天发生的症状,而延迟症状是指在治疗后最多出现5天的症状。
急性呕吐/恶心:发生在化疗或放疗后的前24小时内。从病理生理学角度来看,这一时间段内的恶心和呕吐主要是由小肠的内源性嗜铬细胞释放的血清素触发的。
延迟呕吐/恶心:发生在癌症治疗后24小时至5天内。传递物质P在其中发挥了重要作用,它主要存在于延髓区。
预期性呕吐/恶心:由于在先前的化疗或放疗过程中经历了呕吐和恶心的负面体验,导致的通过经典条件反射形成的“学习”症状。
当面对经历多天治疗方案的患者持续重叠的“急性”和“延迟”症状时,这一理论构建的局限性便显而易见。
合并症的指征
恶心和呕吐常常是合并症或并发症的指征。如果抗恶心药的救助疗法无效,则必须仔细考虑多种可能的鉴别诊断。
鉴别诊断
癌症患者的恶心和呕吐可能有多种原因,常常是合并症或并发症的表现。如果观察到与癌症治疗之间的时间关系,应考虑重新审视所选择的抗恶心药物预防方案,并确认患者是否按时服用了药物。如果不清楚是否存在时间关系,或者在长期治疗期间突发新症状,或者救助疗法无效,则必须仔细考虑多种可能的鉴别诊断。
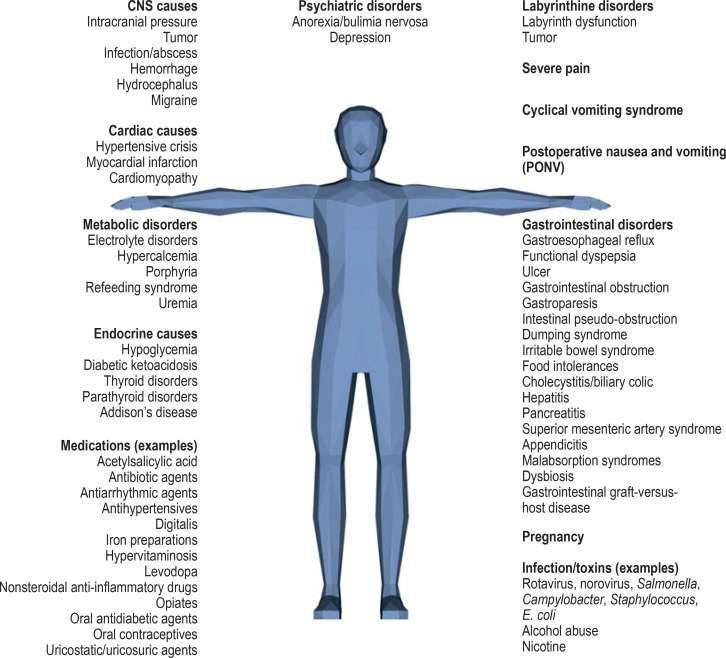
风险因素
癌症治疗期间恶心和呕吐的风险主要由治疗的类型和强度决定,但个体患者相关的风险因素也起着重要作用。
Ø化疗相关的风险因素
癌症化疗期间的恶心和呕吐风险(“化疗引起的恶心和呕吐”,CINV)主要取决于所施用治疗的呕吐诱发潜力。静脉给药、高剂量、较快的给药速度或密集剂量治疗方案也可能增加CINV的风险,但这些因素在呕吐风险分类中并未考虑。
对于静脉给药的单一药物,呕吐风险分为四个类别(图1),从微弱的呕吐风险(在没有预防措施的情况下呕吐率小于10% )到高风险呕吐,其中在没有预防措施的情况下呕吐的风险超过90% 。药物的活性成分的风险特征决定了推荐何种预防措施。
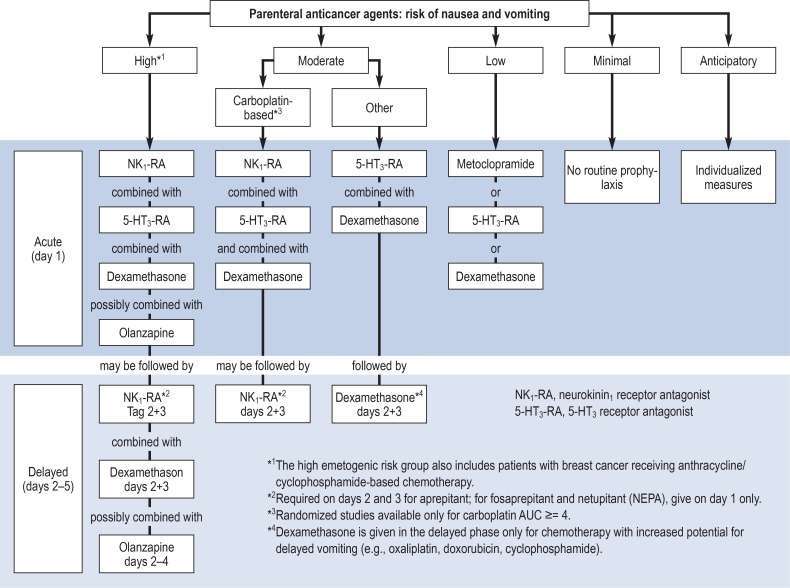
治疗的类型和强度决定了恶心和呕吐的风险
癌症治疗期间恶心和呕吐的风险主要由治疗的类型和强度决定。
自2020年以来,美国临床肿瘤学会(ASCO)和全国综合癌症网络(NCCN)的指南小组将口服化疗药物的分类限制为两个风险类别:高/中等风险和最低/低风险(eTable 2, Figure 2)。鉴于关于恶心/呕吐的信息常常缺失,未能区分严重程度的不同,以及关于研究数据(来自三期研究)中抗恶心药物预防措施的不明确性,这种简化是合理的。
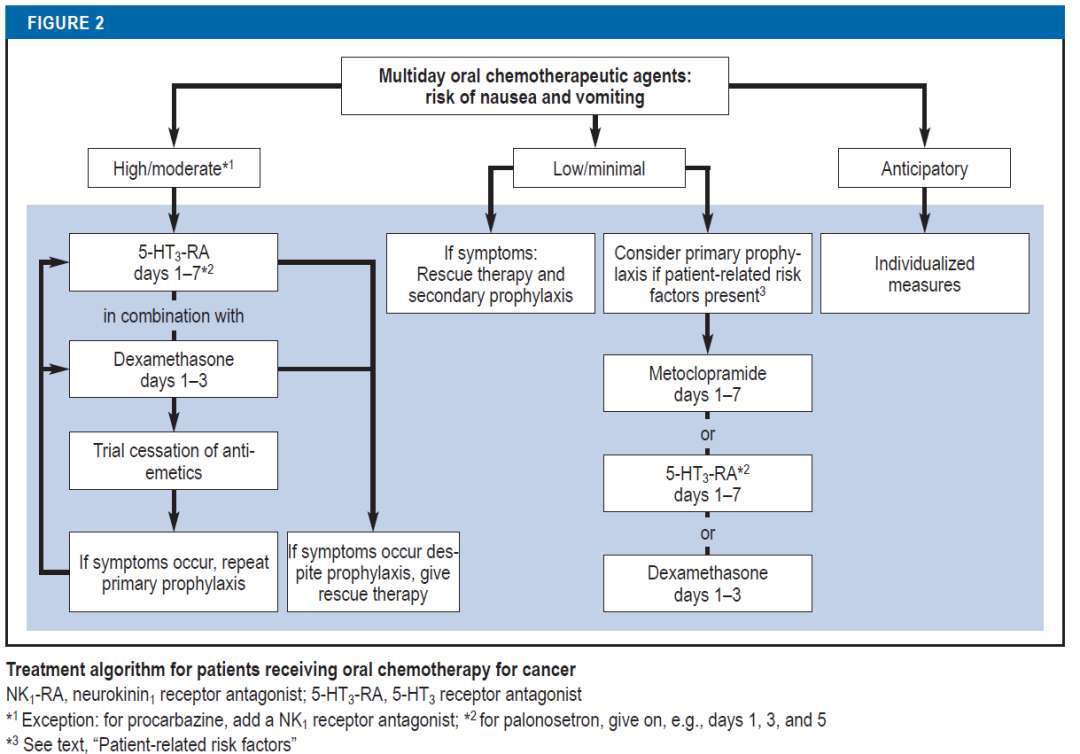
在联合治疗的情况下,具有最高呕吐性潜力的药物决定抗恶心药物的选择。将两种具有相同呕吐性潜力的药物联合使用,并不会增强呕吐的风险(例外情况是基于蒽环类药物/环磷酰胺的乳腺癌化疗,该治疗被评估为具有高度呕吐性)。
抗恶心药物预防的选择
在联合治疗中,具有最高致吐潜力的药物决定抗恶心药物预防的选择。
Ø放疗相关的风险因素
放疗引起的恶心和呕吐(RINV)的频率和严重程度主要取决于肿瘤位置、放疗体积、个体及总剂量、剂量分割和放疗技术。
多国癌症支持治疗协会(MASCC)/欧洲医学肿瘤学会(ESMO)和美国临床肿瘤学会(ASCO)的指南推荐将辐射区域评估为最重要的治疗相关风险因素,并区分为四个风险组(表1,图3)。目前,预防建议中没有其他风险因素。

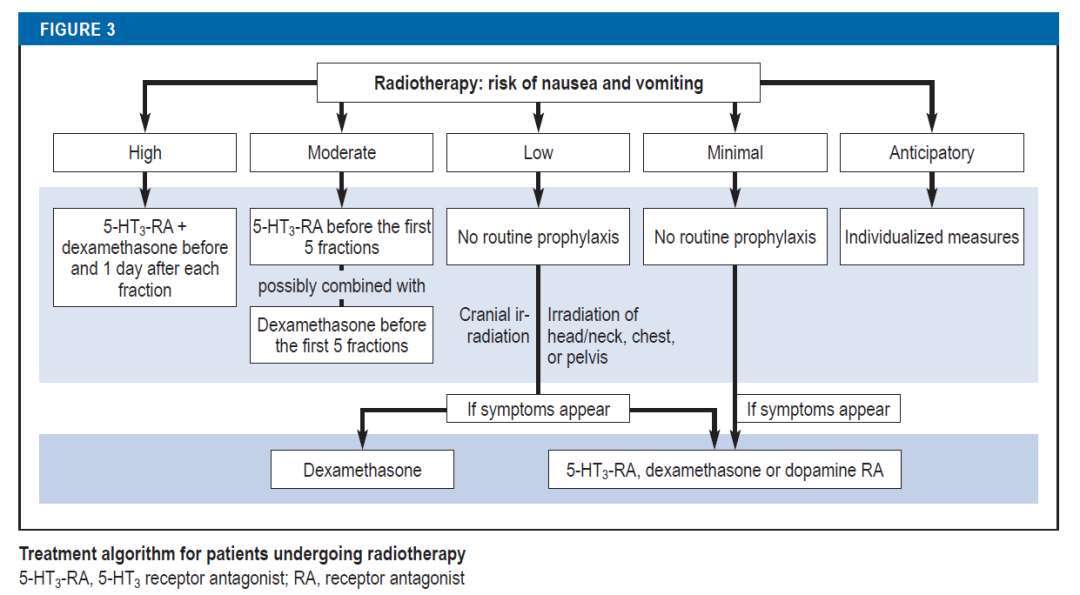
重要的治疗相关风险因素。
当前的指南推荐将辐射区域评估为最重要的治疗相关风险因素。
Ø患者相关的风险因素
迄今为止,个体患者相关的风险因素主要是在研究中回顾性识别的。在癌症治疗前经历过其他形式的恶心或呕吐的患者,例如晕动病或孕期恶心与呕吐,面临着在癌症治疗期间增加恶心和呕吐的风险。对于女性、年轻患者、易焦虑倾向以及健康状况较差的患者,亦描述了增加的风险。
在接受放疗的患者中,报道的额外患者相关风险因素包括同时或近期接受化疗、癌症晚期以及在之前的治疗中经历过恶心和/或呕吐。到目前为止,患者相关的风险因素在预防治疗算法中仅起次要作用(图1-3)。
疗效评估
必须在每个新周期开始之前评估抗恶心药物预防的疗效,以便进行最佳调整。
恶心和呕吐的预防
在癌症治疗的准备过程中,应重视抗恶心药物的预防,并进行规划。在每个新周期开始之前,必须评估其疗效,以便进行最佳调整。在联合治疗中,具有最高致吐潜力的药物决定风险类别(图1,Figure 2)。
Ø抗癌药物/化疗
静脉注射高度致吐化疗(建议仅针对一天的治疗,除非另有说明)
蒽环类药物和环磷酰胺的联合使用
在患有乳腺癌的女性中,蒽环类药物和环磷酰胺的联合使用被归类为高度致吐性(即容易引起呕吐)的治疗方案。
Ø药物的致吐性
**高致吐性药物**:像顺铂(cisplatin)、卡莫司汀(carmustine)、达卡巴嗪(dacarbazine)或美法仑(melphalan)这类药物,通常具有较高的致吐潜力,也就是说患者使用这些药物后,出现呕吐等不良反应的可能性较大。
**特定组合的致吐性**:对于乳腺癌女性患者而言,蒽环类药物(anthracyclines)与环磷酰胺(cyclophosphamide)联合使用时,也被认为具有高度致吐性。
Ø预防呕吐的措施
**预防方案及效果**:一种预防呕吐的方案是由5 - HT₃受体拮抗剂(5 - HT₃ - RA)、NK₁受体拮抗剂(NK₁ - RA)以及地塞米松(dexamethasone)组成。采用这种方案,能够预防大约70% 到80% 的患者出现急性呕吐。
**不同药物方案的比较**:在一项三期临床研究中,NK₁ - RA组的患者完全缓解率(即没有呕吐等不良反应)显著高于标准治疗组。具体来看,NK₁ - RA组有72.7% (样本量为260)的患者达到完全缓解,而标准治疗组只有52.3% (样本量也是260)的患者达到完全缓解,两组之间的差异具有统计学意义(P < 0.001)。
**奥氮平的进一步改善作用**:尽管奥氮平(olanzapine)可能会带来一些镇静的副作用,但加入奥氮平后,能够进一步提升预防呕吐的效果。纳瓦里(Navari)等人在2016年开展的一项研究,对比了奥氮平(样本量为192)和安慰剂(样本量为188)。结果表明,在急性期、延迟期以及整个观察期间,奥氮平组的完全缓解率都显著高于安慰剂组。具体数据为:急性期奥氮平组86% ,安慰剂组65% (P < 0.001);延迟期奥氮平组67% ,安慰剂组52% (P = 0.007);整体上奥氮平组64% ,安慰剂组41% (P < 0.001)。
Ø后续给药安排
**延迟性呕吐和恶心的预防**:为了防止化疗后延迟出现的呕吐和恶心,地塞米松以及在合适的情况下奥氮平,应该在化疗后的第2天到第4天继续使用。如果选择阿瑞匹坦(aprepitant)作为NK₁ - RA,那么在化疗后的第2天到第3天也需要使用。
**5 - HT₃ - RA在延迟期的无效性**:相比之下,在延迟期阶段,加入5 - HT₃ - RA并不会带来任何改善效果。
Ø静脉注射中等致吐性化疗药物,包括药物种类、预防措施以及不同指南的建议:
1. 药物种类
**中等致吐性化疗药物**:包括蒽环类药物(如阿霉素)、环磷酰胺,以及铂类衍生物奥沙利铂和卡铂。这些药物的致吐风险处于中等水平,既不像高度致吐性药物那样在化疗后极易引起呕吐,也不像低致吐性药物那样很少引起呕吐。
2. 预防措施
**推荐的预防方案**:对于中等致吐性化疗,建议使用两种药物的组合进行预防,即5-羟色胺3受体拮抗剂(5-HT3-RA)和地塞米松。5-HT3-RA能够阻断5-羟色胺与5-HT3受体的结合,从而减少呕吐的发生;地塞米松则通过抗炎等机制发挥止吐作用。
**延迟症状的预防**:在化疗后的几天内继续使用止吐药物以预防延迟性恶心和呕吐,仅在已知具有延迟性恶心和呕吐风险的药物治疗时才有用。例如,对于奥沙利铂、阿霉素或环磷酰胺治疗,可在化疗后的第2天和第3天给予地塞米松。
3. 指南建议
**特殊药物的处理**:在S3指南“支持性治疗”以及MASCC/ESMO和ASCO指南中,卡铂(AUC≥4)在中等致吐性药物中具有特殊地位,其致吐风险高于80% 。在这种情况下,为了预防第1天的急性恶心和呕吐,建议在5-HT3-RA和地塞米松的基础上增加神经激肽1受体拮抗剂(NK1-RA)。NK1-RA可以阻断P物质与NK1受体的结合,从而进一步降低呕吐的发生率。而对于后续几天的延迟症状预防则不需要。
推荐的预防措施。
对于中等致吐性化疗,推荐的预防措施是使用5-HT3受体拮抗剂和地塞米松的两药联合治疗。
对于低致吐性或极低致吐性的静脉化疗,如果治疗的致吐风险较低,可以在治疗当天预防性地使用5-羟色胺3受体拮抗剂(5-HT3-RA)、甲氧氯普胺或地塞米松。如果恶心和呕吐的风险极小,那么通常不需要进行预防性治疗。不过,如果患者出现了相关症状,当然需要进行解救治疗,并且从下一个治疗周期开始就需要进行预防性治疗了。
**Checkpoint inhibitors(免疫检查点抑制剂)**
- **致吐风险**:被归类为低或极低致吐性药物。
- **止吐治疗**:如果需要止吐治疗,优先选择5 - HT₃受体拮抗剂(5 - HT₃ - RA)或甲氧氯普胺。
**静脉注射高致吐性多日化疗**
- **研究数据**:大多数可用的研究数据是针对5天PEB(顺铂、依托泊苷、博来霉素)方案的。
- **治疗方案**:5 - HT₃受体拮抗剂、NK₁受体拮抗剂(NK₁ - RA)和地塞米松的三联组合优于双药组合,因此是明确的推荐方案。
**高剂量化疗**
- **治疗方案**:对于高剂量化疗,也推荐5 - HT₃受体拮抗剂、NK₁受体拮抗剂和地塞米松的三联组合。
- **奥氮平的使用**:在给予高剂量化疗并进行自体干细胞支持的情况下,可以添加奥氮平,但对于接受异体干细胞移植的患者,似乎从添加奥氮平中获益不大。
Ø连续口服化疗
口服化疗药物的致吐潜力依然是决定性因素。这些药物通常需要长期服用,这带来了一个挑战:在大多数情况下,长时间持续同时进行止吐治疗变得不太可行,所以治疗需要根据个体情况来定。到目前为止,这一领域缺乏随机研究,因此建议大多是基于专家共识(见图2、Figure 2)。
**口服高致吐性/中等致吐性化疗**
这个组别的典型代表药物有波舒替尼、替莫唑胺以及口服的环磷酰胺。对于止吐预防,建议采用5 - HT₃受体拮抗剂(第1 - 7天)和地塞米松(第1 - 3天)的组合。如果在尝试从治疗的第8天开始停止预防后出现恶心和呕吐,那么可以重新开始预防。
口服抗癌化疗药物丙卡巴肼具有很高的致吐风险,它是一个例外。在这种情况下,采用5 - HT₃受体拮抗剂、NK₁受体拮抗剂和地塞米松的三联组合是值得的。
Ø#口服低/极低致吐性化疗药物的定义
**药物范围**:所有免疫检查点抑制剂都属于口服低/极低致吐性化疗药物的范畴。
-**致吐风险**:这类药物引发恶心和呕吐的可能性相对较低。
预防性止吐治疗的适用情况
- **特定患者**:对于那些本身就有较强恶心和呕吐倾向的患者,才需要进行预防性止吐治疗。例如,有些患者可能由于自身的生理或心理因素,更容易出现恶心和呕吐的症状,对于这类患者,提前进行止吐预防是有必要的。
- **单一风险因素的考量**:仅仅存在一个风险因素,如女性性别,通常不足以成为进行预防性止吐治疗的理由。因为女性虽然在整体上可能比男性更容易出现恶心和呕吐,但这种差异并不足以保证每个女性患者都需要预防性治疗。还需要综合考虑其他因素来判断患者是否真的有较高的恶心和呕吐风险。
症状出现后的应对措施
- **补救治疗**:如果患者在治疗过程中出现了恶心和呕吐的症状,那么就需要进行补救治疗来缓解这些症状,帮助患者减轻不适。
- **后续预防**:从下一次治疗周期开始,就需要对患者进行预防性止吐治疗。这是为了防止在后续的治疗中再次出现恶心和呕吐的情况,提高患者的治疗体验和生活质量。
##与静脉化疗的相似之处
- **症状处理原则**:在处理恶心和呕吐症状方面,口服低/极低致吐性化疗药物与静脉化疗是相似的。无论是哪种给药方式,当患者出现相关症状时,都需要及时进行补救治疗,并且在后续的治疗中采取预防性措施。
Ø放疗过程中预防恶心和呕吐的抗呕吐药物预防建议,根据4个风险等级来组织的:
**高风险——全身照射**:对于接受高风险恶心和呕吐的放疗患者,建议从治疗当天放疗前开始,直至放疗后1天,使用5-羟色胺3受体拮抗剂(5-HT3-RA)和地塞米松进行双重预防。到目前为止,还没有进行过关于NK1受体拮抗剂(NK1-RA)给药的随机试验。不过,有一个例外,那就是在与顺铂同时进行的放化疗中,证据明显支持在5-HT3-RA和地塞米松的基础上加入NK1-RA。
**中等风险——上腹部、胸椎/腰椎、神经轴**:对于中等风险恶心和呕吐的放疗,应在第1至第5天的每次放疗前给予5-HT3受体拮抗剂(5-HT3 RA),此外,也可以在第1至第5天给予地塞米松。
**低风险——骨盆、颅骨、头/颈部、胸部**
低风险患者仅在出现症状时才接受抗恶心药物。如果在颅部照射期间出现恶心和呕吐,推荐使用地塞米松。如果在头部/颈部、胸部或盆腔区域照射期间出现症状,可以使用5-HT3受体拮抗剂、地塞米松或多巴胺受体拮抗剂(DRA)。
**最小风险 – 四肢、乳房**
对于恶心和呕吐风险最小的放射治疗,不提供抗恶心药物预防。如果出现恶心,可以使用地塞米松、DRA或5-HT3受体拮抗剂。
放射治疗中的救助治疗
在放射治疗中,尚未用于预防的药物可作为救助治疗。初始优先选择5-HT3受体拮抗剂。尽管奥氮平作为化疗诱导恶心呕吐(CINV)的救助抗恶心药物已得到确立,但尚未对其在放疗诱导恶心呕吐(RINV)中的角色进行研究。然而,根据类比,预计它在此方面也会有效。
联合化放疗
在化疗与放疗联合的情况下,风险分类基于化疗或放疗的风险,以高者为准。如果进行同步的顺铂化疗放疗,则有确凿的证据支持在5-HT3受体拮抗剂和地塞米松的基础上添加NK1受体拮抗剂。
Ø预期性呕吐的产生原因
预期性呕吐是源于在治疗过程中经历恶心和呕吐,尤其对于那些有特定风险因素的患者来说更容易出现,这些风险因素包括本身就有容易恶心的倾向或者对治疗存在恐惧心理。
### 预防预期性呕吐的方法
- **药物预防方面**:从治疗的第一天起就提供有效的止吐预防措施,这是预防预期性呕吐的关键步骤之一。此外,在向患者解释治疗方案时,也要向其说明包括计划性止吐在内的支持性策略。
- **心理干预方面**:如果预期性呕吐还是发生了,那么单靠药物来治疗它的效果是有限的,比如使用苯二氮䓬类药物等。此时推荐采用行为疗法策略,像脱敏疗法、催眠或者渐进性肌
抗恶心药物
以下抗恶心药物可供使用(表2):
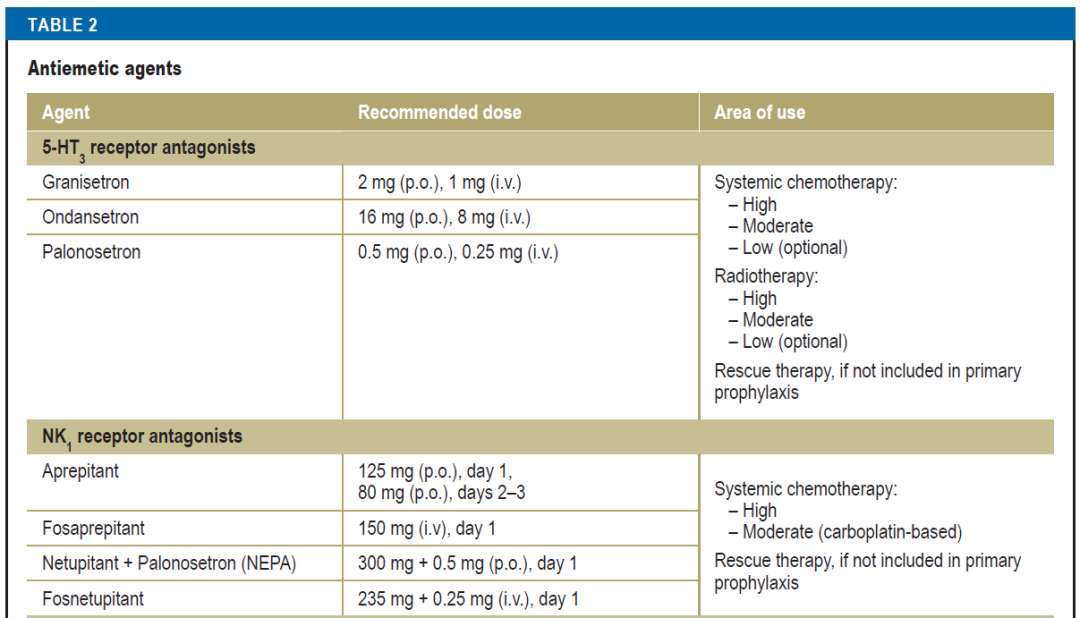
5 - HT₃受体拮抗剂(5 - HT₃ - RAs)
预防癌症治疗期间的急性恶心和呕吐方面非常有效。对5 - HT₃ - RAs进行的直接比较研究表明,它们在疗效上基本相当,尽管帕洛诺司琼在延迟期显示出疗效。Saito等在帕洛诺司琼组的555名患者中,有315名(56.8% )在延迟期出现完全反应,而在格拉司琼组的559名患者中,有249名(44.5% )出现完全反应(P < 0.0001)。不良反应包括头痛(10% 到20% )和便秘(10% 到20% ),还可能出现无症状且短暂的心电图变化,如PR间期延长、QTc时间延长和QRS波群增宽。这些心电图变化目前尚未在帕洛诺司琼中被描述。
1. **5 - HT₃受体拮抗剂(5 - HT₃ - RAs)**:这是一类药物,主要用于预防癌症治疗(如化疗等)过程中出现的恶心和呕吐症状。它们通过阻断5 - HT₃受体发挥作用,因为5 - HT₃受体与恶心和呕吐的生理机制有关。
2. **直接比较研究表明它们在疗效上基本相当**:这意味着对不同5 - HT₃ - RAs进行的头对头比较研究发现,这些药物在预防急性恶心和呕吐方面的总体疗效是相似的,没有哪种药物明显优于其他药物。
3. **帕洛诺司琼在延迟期显示出疗效**:延迟期是指癌症治疗后24小时之后的阶段。帕洛诺司琼与其他5 - HT₃ - RAs相比,在这个延迟期阶段对于预防恶心和呕吐的效果更好。
4. **Saito等(2009)的研究数据**:该研究比较了帕洛诺司琼和格拉司琼两种药物。在帕洛诺司琼组的555名患者中,有315名(56.8% )在延迟期出现完全反应,即没有恶心和呕吐的症状;而在格拉司琼组的559名患者中,有249名(44.5% )出现完全反应。P < 0.0001表示这种差异在统计学上具有显著性,说明帕洛诺司琼在延迟期的疗效确实优于格拉司琼。
NK1受体拮抗剂(NK1-RAs)
- **预防作用**:NK1受体拮抗剂在预防延迟性恶心和呕吐方面特别有效。
- **常见副作用**:更常见的副作用包括疲劳(17% )、嗳气(14% )和呃逆(4.5% )。
- **药物相互作用**:在德国可用的NK1受体拮抗剂是CYP3A4的中等强度抑制剂,因此对于接受高致吐性治疗的患者,必须减少地塞米松的剂量(表2显示了减少后的地塞米松剂量)。到目前为止,尚未证实与环磷酰胺、多西他赛、长春新碱或依托泊苷等细胞毒性药物存在相互作用。
糖皮质激素
- **预防作用**:糖皮质激素(通常是地塞米松)是止吐预防的重要组成部分,尽管其作用机制尚未完全明确。
- **常见副作用**:观察到的糖皮质激素的不良反应包括短期睡眠障碍(45% )、消化问题(27% )、不安(27% )、食欲增加(19% )、体重增加(16% )和痤疮(15% )。
### 糖皮质激素的使用情况
- **等效剂量替换**:如果在方案中包含等效剂量的糖皮质激素(8毫克地塞米松相当于大约40毫克泼尼松),则可以省略用于止吐的地塞米松。
- **免疫检查点抑制剂与致吐化疗的联合治疗**:对于由免疫检查点抑制剂和致吐化疗组成的联合治疗,使用糖皮质激素进行止吐预防目前存在争议,因为有可能会降低对癌症治疗的反应。ASCO指南(支持使用糖皮质激素)和NCCN指南(反对使用糖皮质激素)得出了不同的评估结果。我们建议对于免疫检查点抑制剂与致吐化疗的联合治疗采用糖皮质激素预防。免疫检查点抑制剂的单药治疗不需要使用糖皮质激素,因为整个这类药物现在被归类为低致吐性。在CAR - T细胞治疗的调理方案中,止吐预防不应包括糖皮质激素。
奥氮平
- **预防作用**:奥氮平是一种非典型抗精神病药,最初作为救援止吐药使用,但现在建议用于高致吐性化疗的主要预防。5毫克剂量(第1 - 4天)应作为首选,因为它提供了相当的止吐效果,并且安全性更好。
- **副作用**:作为一种非典型抗精神病药,奥氮平很少出现锥体外系副作用,尽管它具有镇静作用。偶尔,奥氮平会延长QTc时间,这在与其他药物联合使用时必须加以考虑。作为救援药物,奥氮平是首选,明显优于甲氧氯普胺。然而,奥氮平尚未获得CINV(化疗诱导的恶心和呕吐)的批准。
5. **不良反应**:这些药物可能会引起一些不良反应,如头痛和便秘,发生率在10% 到20% 之间。此外,还可能出现一些无症状且短暂的心电图变化,包括PR间期延长、QTc时间延长和QRS波群增宽。这些心电图变化可能提示心脏电生理方面的一些改变,但目前尚未在帕洛诺司琼中观察到这些变化,这可能意味着帕洛诺司琼在心脏安全性方面相对较好。
Metoclopramide(甲氧氯普胺)
- **重要性下降**:作为一种多巴胺2受体拮抗剂(dopamine2 RA),甲氧氯普胺在治疗恶心呕吐中的重要性已经显著降低。
- **剂量限制**:由于存在严重的不良反应,甲氧氯普胺的最大日剂量必须限制为每千克体重0.5毫克(mg/kg),对于成年人来说,最大剂量为每天三次,每次10毫克。
- **适用情况**:它可以用于低致吐风险化疗的初级预防以及救援治疗。
- **不良反应**:常见的不良反应包括疲劳、腹泻和内心不安。锥体外系运动障碍和迟发性运动障碍较为罕见,尤其是在年轻患者中。
Benzodiazepines(苯二氮䓬类药物)
- **非主要抗恶心药物**:这类药物本身并没有主要的抗恶心效果。
- **辅助作用**:但它们的抗焦虑作用和镇静效果使其在预防预期性呕吐方面有效。对于焦虑的患者,苯二氮䓬类药物可以作为初级预防的辅助药物。
Dimenhydrinate(茶苯海明)
- **救援性抗恶心药物**:作为H1受体拮抗剂,茶苯海明适合用作救援性抗恶心药物,但不适合用于预防。
- **常见副作用**:嗜睡是其常见的副作用。
Cannabinoids(大麻素类药物)
- **救援性抗恶心效果**:大麻素类药物可以作为有效的救援性抗恶心药物。
- **可能的副作用**:已经描述了多种可能的副作用,从嗜睡到欣快、幻觉和抑郁不等。
- **临床试验数据**:在一项关于口服四氢大麻酚/大麻二酚(THC/CBD)大麻提取物的随机二期交叉试验中,已经发表了积极的试验数据。一项三期研究已经启动,但结果尚未公布。
**预防和治疗的替代方法**
**针灸和指压**:针灸和指压是通过使用针灸针、指压带或拇指刺激手腕上的心包穴P6。一项对随机对照试验的荟萃分析表明,针灸和指压在急性期对恶心有较小的缓解效果(SMD = -0.18,95% 置信区间:[-0.31;-0.05],P < 0.01),但对呕吐的发生率没有影响。根据“癌症患者治疗中的补充医学”S3指南,针灸或指压可以作为减少恶心和呕吐的额外措施来考虑。
**生姜**:在细胞抑制药物治疗期间,生姜的止吐效果研究数据存在矛盾。补充医学的S3指南将生姜列为“可以给予”的选项(最大每日剂量1克,片剂或粉末)。
**渐进性肌肉松弛**:渐进性肌肉松弛被推荐用于治疗预期性呕吐。这种做法涉及身体肌肉群的依次紧张和放松。它被认为是一种副作用较少的程序,可以通过健康保险公司和其他组织提供的课程,或者借助书籍和光盘来学习。
结论
过去20年止吐药物的发展,显著减轻了癌症化疗期间的恶心和呕吐情况。癌症治疗中的止吐预防,不仅是以患者为中心的护理的重要组成部分,而且对癌症治疗的成功至关重要。
欢迎点赞、转发、在看,给我鼓励,如果觉得本文有用请关注我!陪你一起成长,一起努力,一起春看花,夏看荷,秋看枫,冬看松,糖果读书笔记,带您领阅世间美好。
参考文献:Dtsch Arztebl Int. 2022 May 27;119(21):382-392.doi: 10.3238/arztebl.m2022.0093.
收藏
回复(4)举报
参与评论
评论列表
按投票顺序
谢谢分享
举报
2025-03-19 14:05:59 有用(0)
回复(0)
加油
举报
2025-03-19 09:49:40 有用(0)
回复(0)
 绿柳青青
绿柳青青谢谢分享
举报
2025-03-19 09:59:39 有用(0)
回复(0)
举报
2025-03-19 13:36:19 有用(0)
回复(0)
相关推荐
热点推荐
2013-11-19 14:23:04
爸爸确诊病情已经有11个多月了。一共做了8次大化疗,2次小化疗,以及35次放疗,上月返医院检查“瘤子”没有了。这一路走来,有多少的艰辛与泪水。在这里与大家分享爸爸的治疗过程。起初,拿到病例报告的时候,
2013-11-19 14:31:01
妈妈患肺癌已经有三年了,这三年来一直在接受治疗到现在,下面是妈妈检查以及治疗的过程。2010年10月,妈妈体检出肺癌IV期,纵隔淋巴转移,肝部转移,去省肿瘤医院复查,做了PET-CT,结果一样,省肿瘤
2013-11-19 15:04:43
2011年11月,妈妈被诊断肺癌,我在网上浏览了很多帖子,学到了很多,看到了一批又一批共同奋斗在抗癌战线上的战友。这15个月走下来,越来越体会到抗癌之路的艰辛,今天发个帖子,记录一下妈妈的治疗经过,也
























