PD-1单抗用于非小细胞肺癌一线治疗?还早,还早!
先说一段旧闻,大约半个月前施贵宝公司宣布其PD-1单抗(Opdivo)在一项名为Checkmate-026的非小细胞肺癌三期临床研究失败,该研究以PD-L1表达>5%为标准,招募了541位、初治晚期肺癌患者,分别使用Opdivo或一线标准含铂方案化疗,结果显示该研究的主要研究终点无进展生存期两组未见显著差异,其他次要研究终点也均未能观察到PD-1单抗在一线治疗中对比标准化疗有其优势。投资者随即对此结果做出剧烈反应,施贵宝一度损失市值250亿美元。而主要竞争对手默沙东(拥有另一PD1单抗,Keytruda)市值增长150亿美元,另两家拥有PD-L1单抗的公司--罗氏与阿斯利康市值也随之分别增长约30和60亿美元。
那么纳武单抗(Nivolumab,Opdivo)是否真的就如同资本市场上的反应的那样,一跌到底,无法翻身呢?我们查阅到了国际著名免疫学期刊《Immunotherapy》(免疫治疗)杂志8月刊发表了一篇将有关纳武单抗治疗非小细胞肺癌(NSCLC)的诸多临床研究进行汇总分析(一种研究者将各个研究的原始数据进行高级统计分析的方法,较单一发布研究的统计效力、证据级别更高),接下来由我们复习一下有关纳武单抗治疗非小细胞肺癌的汇总研究结果。
纳武单抗治疗非小细胞肺癌的汇总分析 ¹
本文将9个符合要求的纳武单抗治疗非小细胞肺癌的临床研究数据进行汇总分析,探寻纳武单抗治疗非小细胞肺癌的疗效究竟如何,还有肿瘤表面PD-L1的表达能否作为其疗效预测的生物标记物。
不卖关子,结论先行:纳武单抗用于NSCLC二线治疗,患者一年生存率可达到41%,优于多西他赛--当前NSCLC二线化疗的标准治疗方案,而当纳武单抗用于非小细胞肺癌的一线治疗时,病人的一年生存率则可达到76%。综合一线和二线治疗的数据,PD-L1阳性(>5%)的病人纳武单抗治疗客观反应率更高,而在二线治疗中即使PD-L1< 1%的病人使用纳武单抗相比于多西他赛仍然有一定程度的获益,PD-L1的表达更适合作为非鳞癌病人预测纳武单抗疗效的生物标记物,而鳞癌病人使用纳武单抗可以无须考虑PD-L1的表达情况。
癌细胞的产生和发展依靠基因突变的获得和积累。癌细胞突变的基因会产生异常的蛋白质,成为被免疫系统识别的抗原。正常情况下免疫系统通过识别这些抗原就可以识别癌细胞并消灭它们,就跟消灭病原体一样,然而癌细胞的特征之一就是有能力逃避免疫系统的识别。
那么癌细胞是如何逃避免疫系统的识别呢?其中一个途径是利用PD-1,即细胞程序性死亡受体1,PD-1是T细胞(免疫系统最强的战士)表面的受体(类似于锁孔),当它跟正常细胞上的配体(PD-L1或PD-L2,类似钥匙)结合就会使T细胞停止攻击正常细胞。癌细胞上也有PD-L1,所以即使免疫系统识别出癌细胞,T细胞仍然不会攻击它。因此PD-1及其配体PD-L1就成为免疫治疗药物的重要靶点,抑制这些靶点的药物也被称为免疫哨卡抑制剂。
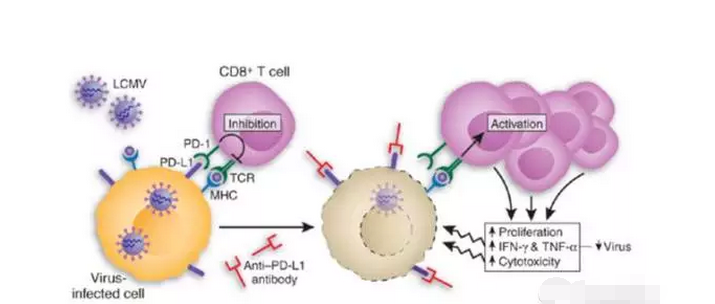
纳武单抗就是一类完全人源化的PD-1单克隆抗体,纳武单抗卡在T细胞表面的PD-1上,阻挡癌细胞表面的PD-L1与PD1结合(类似堵住锁孔),这样即使癌细胞表面有PD-L1 的表达,T细胞仍然会攻击癌细胞。纳武单抗及类似的免疫哨卡抑制剂已经有相当多的治疗各种癌症的临床研究开展。
全球因癌症死亡的病人,肺癌是第一大死因。美国国家癌症学会SEER数据库的数据显示:57%的病人确诊NSCLC时已经是IV期(有远处转移)(而这个数据与Haalthy调查的中国肺癌调查惊人的相似),而这些患者的五年生存率则十分不理想。
中国肺癌患者初诊时的分期
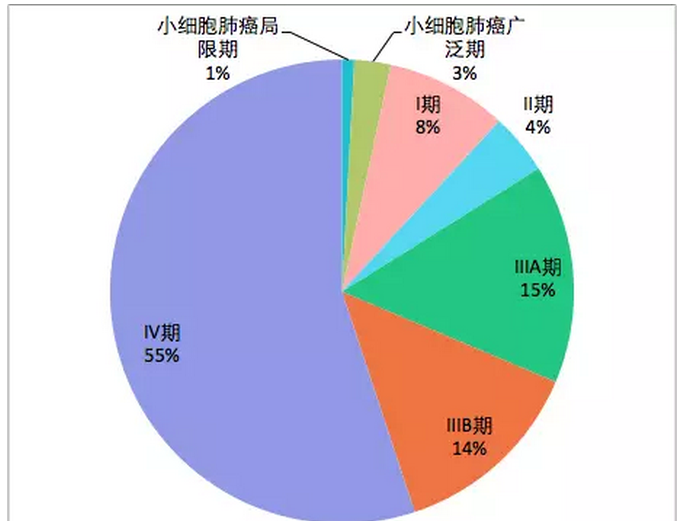
近十年来随着新的靶向疗法的发展,NSCLC的治疗已经有了一定改善,但目前常用的靶向药物如口服酪氨酸激酶抑制剂都只针对具有特定基因变异的肿瘤有效,而NSCLC二线治疗的选择仍然相当有限。针对这种现状,纳武单抗最初的临床研究设置成NSCLC的二线治疗,并获得肯定的疗效。USFDA(美国食物及药品管理局)根据两个大型III期临床研究结果批准纳武单抗用于NSCLC(包括鳞癌与非鳞癌)的二线治疗,与此同时肿瘤表面的PD-L1表达作为预测纳武单抗这类免疫哨卡抑制剂疗效的生物标记物在科学界仍然有争议,相关的研究结果也互有出入。考虑到上述的情况,研究者决定搜集过往纳武单抗的临床研究数据进行汇总分析,评估纳武单抗的疗效和安全性及肿瘤表面的PD-L1表达情况是否可以有效预测纳武单抗的疗效。纳武单抗一线治疗研究者只找到一个临床研究,而研究中还有纳武单抗联合易普利单抗(Ipilimumab,一种CTLA-4抑制剂,另一免疫哨卡抑制剂),可能会对分析结果有干扰,但研究者仍然纳入了本研究,分析显示纳武单抗用于一线治疗ORR达29%,1年OS率是76%。纳武单抗耐受良好,全部副作用发生机率是40%,大都可以控制,尤其是早期发现时更易处理。至于免疫反应引起的危险的3-4级肺炎发生率是5%。研究者通过电子数据库和医学会议论文搜索从2000年到2015年6月有关纳武单抗临床研究的信息,最终筛选得到9个符合要求的临床研究,涉及2102个患者。研究者主要将9个临床研究的ORR(客观反应率)、24周PFS(无进展生存)率以及1年OS(总生存)率进行汇总分析。至于PD-L1阳性的标准,研究者综合各研究后定为PD-L1表达>5%。研究者又根据治疗的线程和肿瘤组织学分类对这些数据进行汇总分析。
纳武单抗用于二线治疗总体ORR是17%,鳞癌ORR更高,达到21%,非鳞癌则是15%。1年OS中,非鳞癌是48%,鳞癌是32%,总体1年OS率是41%,出现这样的结果可能是因为鳞癌基因突变更多,免疫系统更容易识别,所以有效率更高,但其后续治疗手段有限,导致生存期受到影响。耐受性方面25%的病人有3-4级副作用,有2%的病人出现肺炎,3-4级肺炎则是0.7%。相比多西他赛来说,纳武单抗在ORR、24周PFS率、1年OS率均胜出。
PD-L1的表达与疗效的关系方面,PD-L1阳性(>5%)病人有更高的ORR,达到27%,而阴性病人ORR则是13%。PD-L1阳性病人24周PFS率和1年OS率比阴性病人高,但总体没有统计学差异。相比多西他赛,即使PD-L1表达<1%的病人,ORR也跟多西他赛相似,而OS仍有延长趋势。PD-L1更适合作为非鳞癌病人预测纳武单抗疗效的生物标记物,而对于鳞癌病人,无论PD-L1状态如何使用纳武单抗均能获益。
总结:
1、纳武单抗用于NSCLC二线治疗优于多西他赛;
2、纳武单抗用于NSCLC一线治疗有其前景,但需要更多研究验证;
3、纳武单抗耐受良好,副作用只要及早发现和处理,总体可控
4、PD-L1表达可以一定程度上预测纳武单抗治疗的客观反应率;
5、非鳞癌病人PD-L1阳性使用纳武单抗获益更大,而鳞癌病人使用纳武单抗则无须考虑PD-L1状态。
1. Aguiar PN Jr, Santoro IL, Tadokoro H, et al. A pooled analysis of nivolumab for the treatment of advanced non-small-cell lung cancer and the role of PD-L1 as a predictive biomarker. Immunotherapy. 2016 Sep;8(9):1011-9.
点评:
说一千道一万,这个汇总分析的结果综合既往总计9个研究、2000多名研究患者的数据,属于从更高级别循证医学证据证实纳武单抗在二线治疗中对比既往的标准治疗多西他赛的多方面优势依然不可撼动,并且药物相关不良反应可控(只是可惜 “经济学”毒性还是较大),所以在当前的临床实践中,在经济条件允许的条件下,纳武单抗在二线治疗中还是靠谱、很靠谱的。但在一线治疗中,由于这个不作死就不会死的Checkmate-026研究的失败(那也是施贵宝自作把研究入组标准定义为PD-L1表达大于5%即可,此时把其类似研究KEYNOTE-024的入组标准定义为PD-L1表达大于50%的默沙东正在厕所偷笑),暂时还不建议患者在一线治疗中进行盲目尝试。因为无论KEYNOTE-024的研究效果如何,也不建议贸然参考一个同样药物(Opdivo)失败而另一个同样药物(Keytruda)又获得成功的研究结果,因为临床研究也都存在假阳性概率,只是大或小。一个靠谱的方案决策者都是要参考多个类似的研究结果,才会谨慎改变临床推荐,而一般不会以一个或两个研究的结果为参考直接应用于患者,尽管肿瘤细胞表面PD-L1表达大于50%(其实这样的患者比例很低,具体多低?过几天告诉大家)貌似暂时看着像略微靠谱的生物标记物,可将来的事情谁会知道呢?
既然提到了PD-1治疗,那么就还是不得不提PD-L1的表达是否是一个疗效预测指标,综合诸多当前研究结果来看,笔者的建议是,鳞癌患者要是从追求生存获益的角度来看,PD-L1的表达兴许并不重要,但要是从获得肿瘤缩小的把握度来看,PD-L1的表达那可是非常重要,具体证据不在这里一一列举了;至于非鳞癌患者,PD-L1的表达肯定是要测,并且要十分规范的测,可能有人会问,这东西还有不规范的么?当然有了,现在从各项已发表研究中就可以查阅得到,Dako公司分别与施贵宝与默沙东合作制定了评定标准不同的各自规范,而罗氏诊断与阿斯利康分别以Ventana方法来进行诊断,而其实FDA只批准了Dako公司的PD-L1 IHC 22C3 pharmDx为Keytruda的伴随诊断,其他诊断方式都还尚未获批,说明其可参考意义其实就仍然不确定。那么国内哪家靠谱?国内么?别问我,我不会说的。其实,PD-1单抗的疗效预测指标,远远不应该仅仅是肿瘤细胞表面的PD-L1表达那么简单,谁让免疫系统那么地复杂呢?例如肿瘤浸润的淋巴细胞(TIL)数量及其表面PD-L1表达情况(这点要表扬罗氏公司,类似研究做得很好),肿瘤微环境中除了PD-1/PD-L1通路之外的其他免疫拮抗点,例如TIM-3,BTLA等等的表达,还有这几天火起来的CD47等等,理论上全都可以预测PD-1/PD-L1通路抑制剂的疗效。当然现在还没确切的可以用于指导临床的证据,但相信很快就会有更加靠谱的PD-1/PD-L1通路抑制剂疗效预测指标及其组合问世。为什么呢?偷偷的透露点内幕消息,因为肿瘤免疫界内对PD-L1的表达可是又爱又恨,爱的是,PD-L1的确可以指导一部分患者的临床疗效,可恨的是PD-L1表达的疗效预测效力又真的没那么靠谱,有需求就有市场,大家可以静候佳音。
其实刚才说到的都只是来自肿瘤微环境当中影响PD-1/PD-L1通路抑制剂疗效的一部分因素,需要注意的是,患者本身机体内免疫状态也是非常的重要。其道理就是既然想通过患者自身的免疫细胞来对肿瘤细胞进行杀伤,具体指标评估来说,不外乎免疫细胞数量的多少、战斗力如何及对手是美、苏那么强大,还是大海对面那个弹丸小国,免疫细胞数量的多少及战斗力其实就是患者在接受免疫拮抗抑制剂治疗前的预存免疫状态如何。由于有的患者在治疗之前经历过很大剂量的多轮化疗,体质本身就很虚弱,免疫状态自然也不会理想,所以,把免疫治疗放在化疗之前来使用从理论上推断应该是个优选的治疗策略(但仍需多个临床研究证实,在当前阶段不建议尝试)。另外就是要老生常谈了,如何提升患者的免疫力?仁者见仁智者见智,这里不做展开,有的成功了,效果会有提升,有的失败了,出现了很严重的不可挽回的后果,治病不是打游戏,game over后没有机会可以投币再来。具体如何操作呢,请与具体医生成为真正的好朋友先。另外,PD-1单抗可以造成患者的淋巴细胞减少,这个大家都知道了么?这是单克隆抗体的一个特殊效应—ADCC造成,这里简单给大家介绍一下:ADCC全称为抗体依赖的细胞介导的细胞毒性作用,是指具有杀伤活性的免疫细胞(如NK细胞等)通过其表面表达的Fc受体(FcR)识别在了靶细胞表面的抗体尾段(抗体的头段与靶细胞表面的特定表位相结合),进而由免疫细胞经抗体介导而对靶细胞进行杀伤。所以,当单克隆抗体的靶点为肿瘤细胞时,就可以由免疫细胞经由单克隆抗体介导来对肿瘤细胞进行杀伤,鬼才知道一个单克隆抗体能把肿瘤细胞咋地,其实免疫细胞才是经由单抗杀灭肿瘤细胞的大功臣,这也就是临床中大多数以肿瘤细胞表面标记为靶点的单克隆抗体几乎都不单打独斗,因为效果实在是微乎其微,他们都得拽着化疗方案一起使用,因为只有化疗造成了一部分肿瘤细胞死亡、诱导机体产生免疫反应后,单克隆抗体才可以有效的激发免疫细胞对肿瘤细胞进行大面积杀伤。但是,可但是,当单克隆抗体的靶点为免疫细胞时,谁?说的就是PD-1,当PD-1单抗与免疫细胞表面相结合时,则不可避免的造成ADCC效应,其实结果就是免疫细胞之间进行互杀,所以Opdivo说明书上所体现的约一半的患者都会出现淋巴细胞减少,而16%的患者会出现严重的淋巴细胞减少就可以找到一部分的理论依据了。
淋巴细胞都没了,那要PD-1单抗何用(猴子被打跑了,剩跟铁棒又有何用?)?怎么破呢,一个办法就是敲掉PD-1单抗的ADCC效应,让免疫细胞之间相亲相爱,不要互相伤害(不知道据称有20多家国内企业在上马PD-1单抗,可有哪家可以做到这种me better的产品呢?);另一个办法当然就是换PD-L1单抗啊。PD-L1表达于肿瘤细胞表面,这样的话就可以让免疫细胞ADCC效应放心大胆的来吧,单药治疗也好,与化疗配合也好,越强越好,将肿瘤痛痛快快的杀杀杀吧。
收藏
回复(1)参与评论
评论列表
























