DS8201(Enhertu)新适应症HER2低表达乳腺癌获批中文说明书
HER2靶向抗体偶联药物(ADC)Enhertu(T-DXd,DS-8201)由靶向HER2的人源化单克隆抗体通过四肽可裂解连接子,与拓扑异构酶1抑制剂有效载荷连接组成。抗体偶联药物(ADCs)目前正在快速发展,为无数乳腺癌患者带来了新的治疗选择,无论是HR 、HER2-乳腺癌、HER2阳性乳腺癌还是三阴性乳腺癌均可受益。
一、DS8201(Enhertu)获批适应症时间表
2019年12月,美FDA批准了Enhertu上市,用于治疗接受过2种或以上抗HER2疗法的治疗的无法切除或转移性HER2阳性乳腺癌患者。
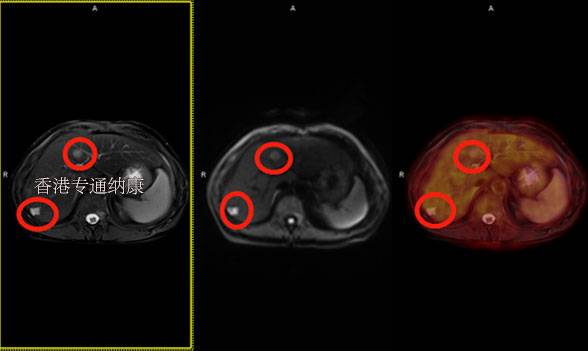
2022年5月5日,美FDA批准Enhertu扩展适应症,用于治疗无法切除或转移性HER2阳性乳腺癌患者,这些患者曾经接受过一种抗HER2靶向疗法的治疗。
2022年8月5日,美FDA批准抗体偶联药物(ADC)Enhertu新适应症,用于治疗无法切除或转移性HER2低表达(HER2-low)乳腺癌患者。
此次的批准,证明了Enhertu将重新定义转移性乳腺癌的分类和治疗,使肿瘤HER2表达水平较低的患者有机会从HER2靶向治疗中获益。
二、DS8201(Enhertu)中文说明书
品名:ENHERTU(DS-8201)
通用名:fam-trastuzumabderuxtecan-nxki
靶点:HER2
规格:100mg
美国首次获批:2019年12月
获批适应症:HER2阳性乳腺癌、HER2低表达乳腺癌、胃癌、肺癌
乳腺癌推荐剂量:5.4mg/kg,每3周静脉滴注一次(21天为一周期),直到疾病进展或不可接受的毒性。
储存条件:2℃至8℃冷藏
三、DS8201(Enhertu)不良反应
1、Enhertu治疗组最常见的任何级别不良反应
包括:恶心(76%)、疲乏(54%)、呕吐(40%)、脱发(40%)、贫血(39%)、便秘(34%)、食欲变差(32%)、肌肉骨骼痛(32%)、腹泻(27%)、腹痛(18%)、体重过轻(16%)、出血(16%)、头痛(15%)、上呼吸道感染(14%)、口腔炎(13%)、周围神经病变(13%)、皮疹(13%)、发热(12%)、间质性肺病(12%)、头晕(11%)、呼吸困难(10%)。
2、最常见的3级或4级不良反应包括:
贫血(10%)、疲乏(9%)、恶心(4.6%)、食欲变差(2.4%)、呕吐(1.6%)、腹泻(1.3%)、间质性肺病(1.3%)、肌肉骨骼痛(1.3%)、便秘(0.8%)、腹痛(0.5%)、头晕(0.5%)、口腔炎(0.3%)、发热(0.3%)、体重过轻(0.3%)、头痛(0.3%)、上呼吸道感染(0.3%)、呼吸困难(0.3%)。
收藏
回复(0)参与评论
评论列表
























