1A期肺腺癌中微乳头作为高危因素带来的影响
概述
我的母亲在2021年查出了肺腺癌,完全改变了我的生活,当我得知母亲是1A期的肺癌时,我稍稍松了口气,但是手术后病理中10%微乳头分外扎眼,让我一度窒息,因为医生说微乳头复发率非常高,所以让我们吃靶向预防。之后我便在各个地方搜集微乳头这个高危因素的资料,发现各种的公众号,资讯,科普短文都说微乳头是最不好的亚型,在早期也容易转移,哪怕存在1%的微乳头也影响预后。当然这句话放大了说没错,不过肿瘤是一个非常异质的东西,影响复发转移的因素非常多,那么有了微乳头成分,到底有多少影响?是否需要在1期患者中进行辅助治疗呢?
我写这篇文章的目的,是想从一些回顾性(已现在为结果,回溯到过去的研究)文章里,来理性分析对于1A期的患者,存在少量的微乳头比如5%-10%,那么这样的患者预后到底如何呢?真的很差吗?也希望可以让一部分有类似病情的患者们不用过于焦虑。
(作为一个刚主动认识肺腺癌的龙套,如有错误地方,请各位不惜吝啬的指出,也可以直接跳到后面看小结部分的结论)
如何评估微乳头带来的影响
作为一个毕业了很久的,平日里苦苦搬砖的复旦不知名计算机小硕,一开始我也是从各种中文翻译资料来补充知识,但是发现这些文章资讯中有一些成分被放大,并很少提及前置条件,让人一叶障目。所以联系了多年不联系的学弟,让把几篇相关的文献给下载了下来,进行了阅读。
那么,怎么正确评估微乳头带来的影响我的思路是:先从回顾性研究中直观的看微乳头带来的影响数据,再去研究微乳头的一些本质问题,比如生物学特性,产生的影响等。目前完成了第一部分,从几篇回顾性研究中看微乳头带来的影响,做法是
1. 首先看文章对微乳头占比的分类,比如按多少成分分类,有几个阈值点5%,10%,20%,50%(比较符合正太分布中的几个点)。如果分类的范围较宽,比如以>5%和<5%划分两类,那么其实就没有什么参考价值,最好每10%分一个组。其次看各个分类中的样本在不同的维度分布是否不同,比如分期占比,肿瘤大小,淋巴侵犯,胸膜侵犯。如果在某个维度的比例倾斜的厉害,比如胸膜侵犯,那么最终的预后差可能是由这个因素胸膜侵犯造成的,而不一定由微乳头造成的。
2. 看DFS(无病生存期)和OS(总生存期)复发曲线,如果DFS和OS具有统计意义(p<0.001),那么结果有参考价值。这里注意如果No.at Risk太少就没有参考价值。比如我认为少于100人的样本没有什么参考价值,并且造成DFS和OS的波动也大。所以在小于100人的样本,不但要看比例还要看绝对值。
3.最后需要看单变量和多变量因素。尤其是多变量,是量化各个不同高危因素影响高低的一个比较科学的对比方式,一般会遇到下面的情况
p<0.001,HR(风险比值)值低:说明是一个有统计意义的低风险因素。
p<0.001,HR值高:说明是一个有统计意义的高风险因素。
p>0.001,HR值高:说明这是一个高风险因素,但是特征在统计学上没有意义,所以即使HR值高,也不能说明这个因素是有意义的,只能在某个采样空间下作为参考。
p>0.001,HR值低:说明这是一个低风险因素,但是特征在统计学上没有意义,所以即使HR值低,也不能说明这个因素是有意义的,只能在某个采样空间下作为参考。
最后有几个小提问想和大家一起探讨一下
1:可否量化不同实验中微乳头带来的影响?
2:可否量化微乳头成分对预后的具体影响?比如我想知道所有条件都相同的情况下,有多少微乳头多带来了多少复发的概率?
文献
下面从一些文献资料里直观的看一下微乳头对1期患者的DFS(无病生存率),RFS(无复发生存率),OS(总生存率)上的差异。这些文章大多都是IIB类证据。综述文章 https://academic.oup.com/icvts/article/24/1/121/2835909?login=true
第一篇:Clinical implication of minimal presence of solid or micropapillary subtype in early‐stage lung adenocarcinoma
早期肺腺癌中实体或微乳头亚型极少存在的临床意义
内容
506 名接受根治性切除的肺腺癌患者。比较有和没有 实性/微乳头 亚型组(分别为 S/MP+ 和 S/MP-)以及 S/MP 比例≤5% (S/MP5) 组之间的临床特征。
分布
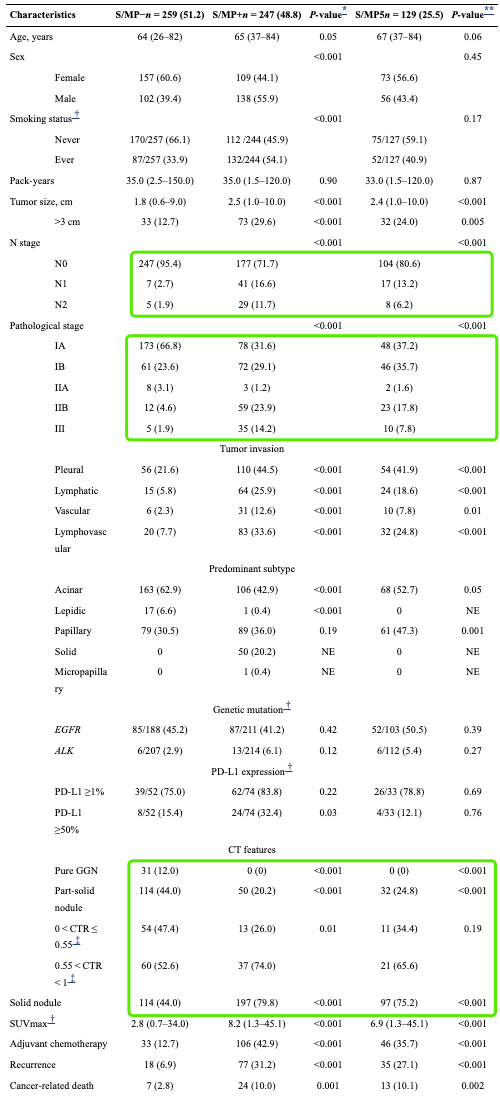
分组
微乳头阴性:A组
微乳头>=5%:B组
微乳头<5%:C组
分布不均匀的维度(A:B:C)
TNM
1A 66.8%: 31.6%: 37% (这还比个毛啊)
1B 23%: 29%: 35%
2A~3期 10.2%: 39.4%: 28%
N state
N0 95.4%: 71.7%: 80.6% (这还比个毛啊)
N1 2.7%: 16.6%: 13.2%
N2 1.9%: 11.7%: 6.2%
肿瘤大小 大小均值 1.8: 2.5: 2.4
CT特征 实性结节 44%: 79.8%: 75.2% (这还比个毛啊)
纯磨 12%: 0: 0
混磨 44%: 20.2%: 24.8%
混磨中的实性<0.55占比 47.4% 26.0% 34.4%
FFS&DS
FFS定义为手术后到复发的时间
DSS定义为手术后到和癌症相关的死亡时间
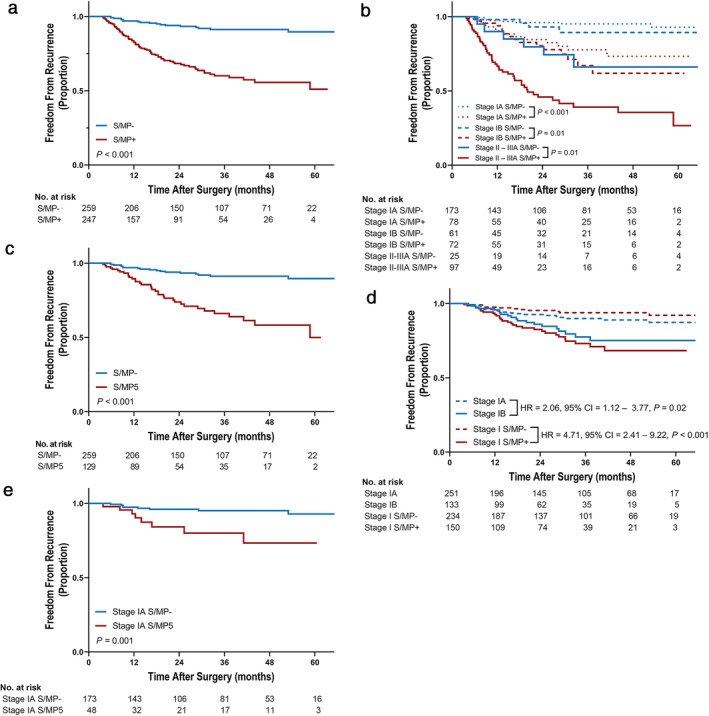
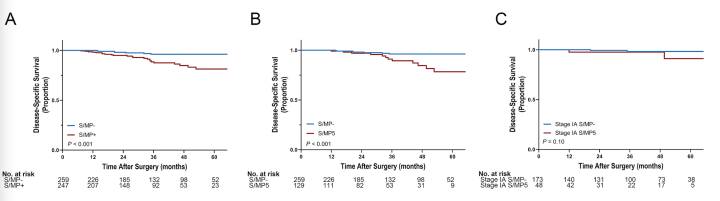
单变量&多变量
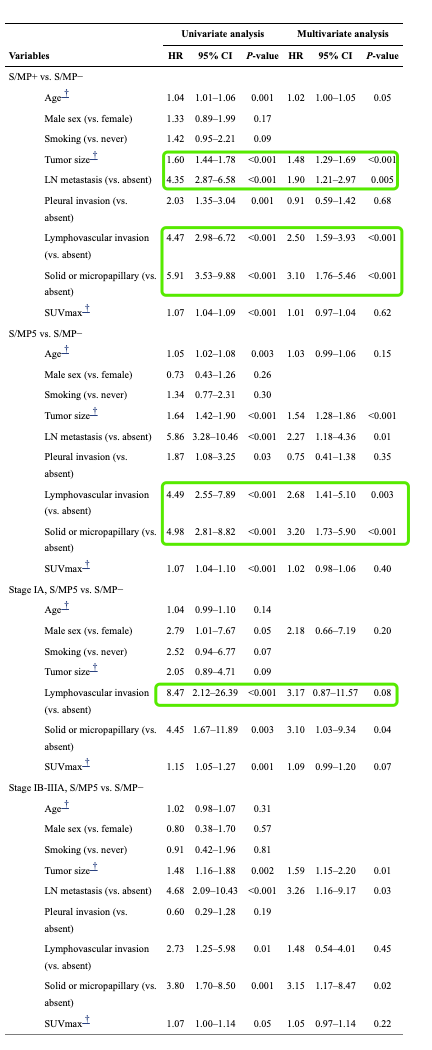
单变量
1A S/MP5 vs. S/MP− DFS:淋巴结转移 8.47,微乳头或实体>=5% 4.45
S/MP+ vs. S/MP− DFS: 淋巴侵犯 4.47,淋巴结转移 4.35,微乳头或实体>=5% 5.91
多变量
1A S/MP5 vs. S/MP− DFS:淋巴侵犯 3.17(p=0.08),微乳头或实体>=5% 3.10(p=0.04)
S/MP+ vs. S/MP− DFS: 微乳头或实体>=5% 3.10,淋巴侵犯 2.50
分析
微乳头阴性组中,大多是GGO(磨玻璃样结节),只有一半的实性结节,而在微乳头阳性的组中,大部分是实性结节。
微乳头阴性组中,1A期,无淋巴结转移的占比更高,而在微乳头阳性的组中,分期比较高,并且淋巴结转移的占比大。
这篇文章的样本,在不同维度上倾斜的非常严重,并且没有回答我之前脑海中的一个问题:到底是微乳头导致了淋巴结转移和更高的分期,还是微乳头的出现与淋巴结转移和更高的分期是独立的,如果只是因为淋巴结转移和更高的分期造成了DFS和OS的变差,那么如果某个人没有淋巴结转移,处于1A期,有少量的微乳头(不占优势)那么复发的概率是不是也不大?
第二篇:The Clinical Impact of Solid and Micropapillary Patterns in Resected Lung Adenocarcinoma
实体和微乳头模式在切除肺腺癌中的临床影响
The Clinical Impact of Solid and Micropapillary Patterns in Resected Lung Adenocarcinoma - PubMed
分布
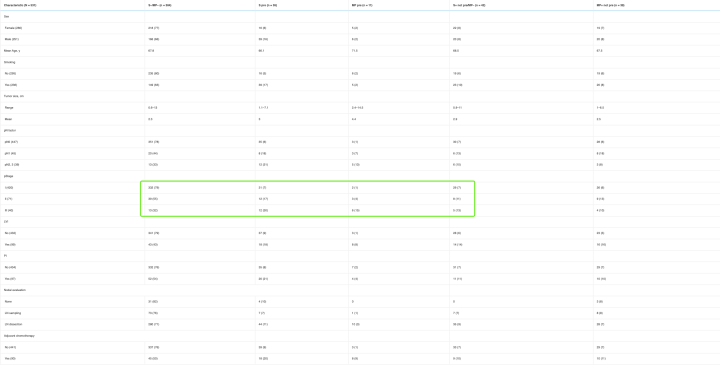
可以看到在不同的分组中,肿瘤分期,淋巴侵犯,淋巴结转移的占比都不同,微乳头实体组中,这些占比都非常高。
DFS&OS
RFS定义为手术后到随访发生复发,死亡的时间或者最后一次随访的时间
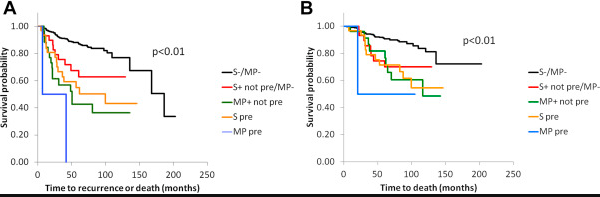
分析
这篇文章的微乳头组数据还是太少了,微乳头>5%组里,只有2个贴壁主型,7个腺泡型,其他的都是乳头型为主。并且在没有微乳头的组里,有43个是原位癌, 46个是微浸润,所以实际1A的数据,应该还要差些。
第三篇:Negative prognostic influence of micropapillary pattern in stage IA lung adenocarcinoma
微乳头模式对 IA 期肺腺癌预后的负面影响
Negative prognostic influence of micropapillary pattern in stage IA lung adenocarcinoma - PubMed
内容
本文描述1A期患者(实际上包含了1B到3A),然后将他们分成按微乳头比例<5%、5-30% 和 ≥30%的三组。比较他们的5年DFS和OS。
其中32 名 (9%) 患者出现复发;17例局部复发,12例远处转移,3例局部和远处转移。在 23 名死亡患者中,分别有 14 名和 9 名死于肺癌和其他疾病。
分布
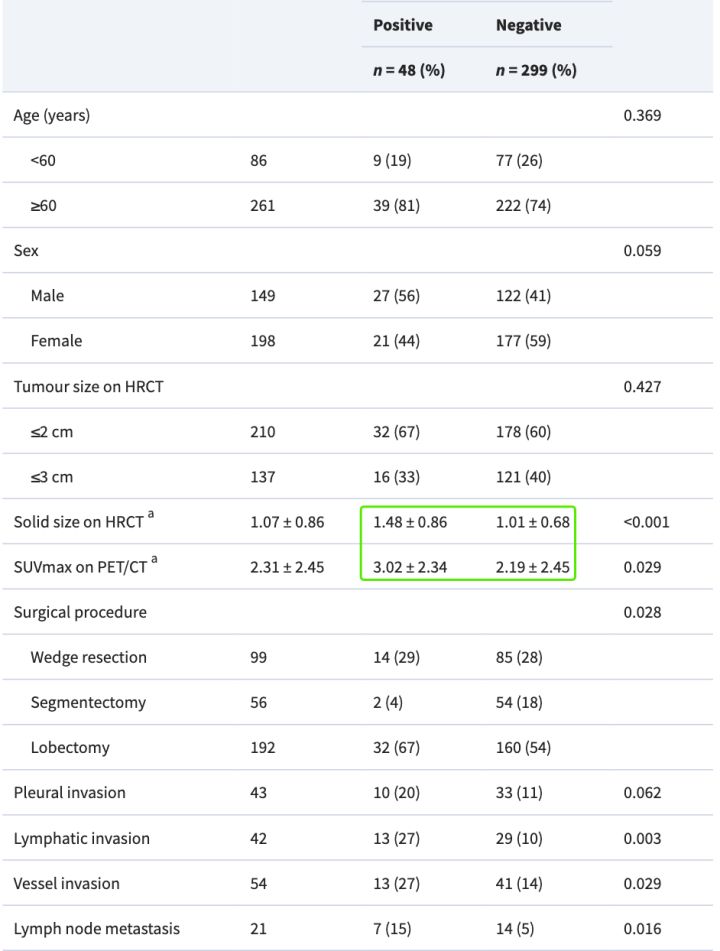
分布不均匀的维度
这里并没有特别不均匀的维度,所以文章数据整体(微乳头阴性阳性)有一定的参考值
结节在CT上的实性尺寸: 1.48 :1.01
DFS&OS
这里的DFS定义为手术后到随访过程中复发和死亡的时间
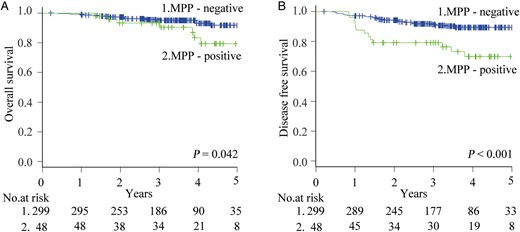
上图在所有1A中(注意No.at Risk里是299和48,也就是包括了刚才提到的1B到3A的病例)
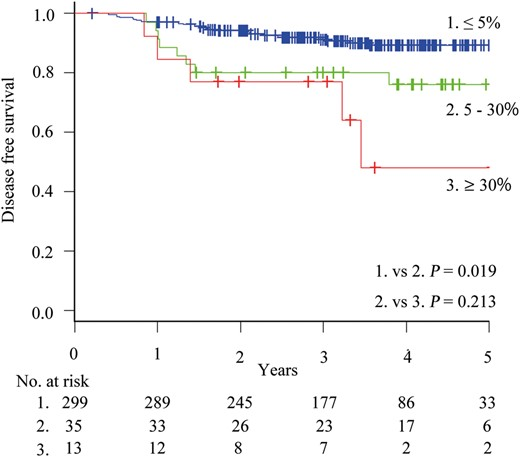
这里(上图)单独把<5%、5-30% 和 ≥30%分成了三组,但是5-30% 和 ≥30%的数据实在太少了。
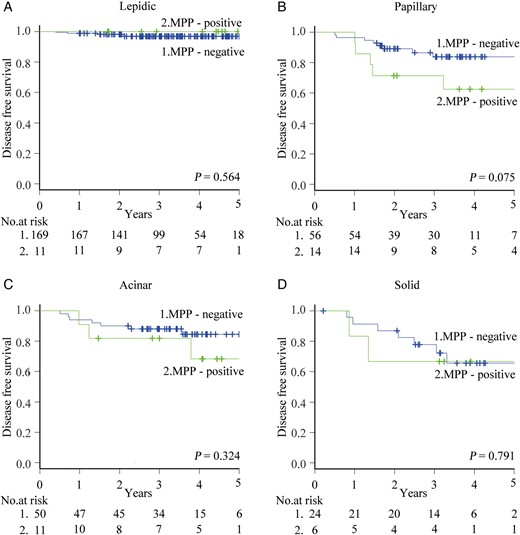
上面1A期各个主型中含有微乳头之后的效果,光从图像看,似乎贴壁为主的比较好,实体为主的较差。但是他们的样本个数只有11,14,11,6个,极度的有偏差,并且p值均>0.01,完全不具有参考价值。
单变量多变量
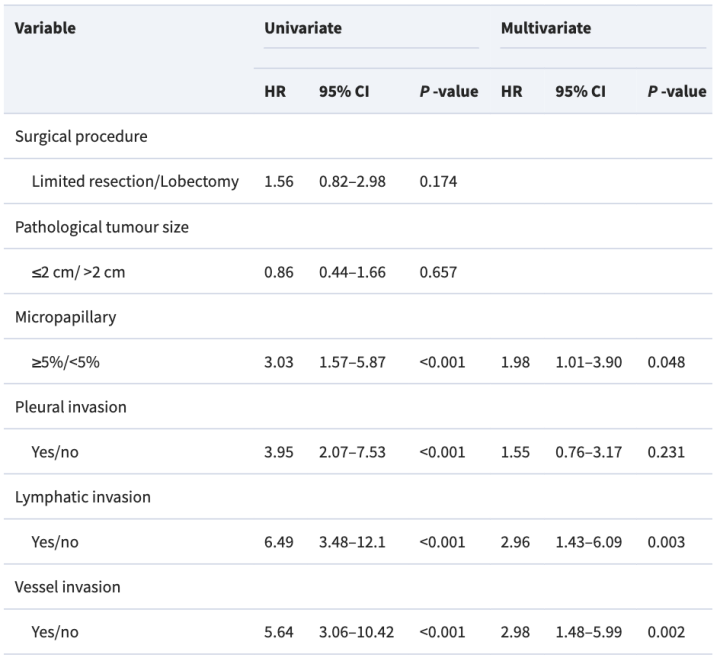
单变量
·DFS:胸膜侵犯 3.95,淋巴侵犯 6.49,血管侵犯 5.64,微乳头 3.03
多变量
· DFS:血管侵犯 2.98,淋巴侵犯 2.96,微乳头>=5% 1.98(p=0.048),胸膜侵犯 1.55(p=0.231)
分析
这篇文章的病例一些特征在微乳头阳性和阴性的分布上较均匀,所以有一定的参考价值。但是这里定义微乳头阳性的方式是用微乳头>=5%来做区分的,这划分的比较大了。我们知道对于>=20%微乳头来说危险成分要升级,但是对于10%以下的来说,我觉得无法从这篇文章中对比出来。
第四篇: A prognostic nomogram based on a new classification of combined micropapillary and solid components for stage IA invasive lung adenocarcinoma
基于IA期浸润性肺腺癌微乳头和实体成分的新分类的预后提名图
内容
这篇文章主要研究的是1A期实体和微乳头对预后的影响。将微乳头和实体按占比归为TPSM-low < 10%, 10%<=TPSM-M<40%, TPSM-H ≥ 40%。一共146 (24.5%)位复发以及79 (13.3%)死亡。(这个复发比例非常高,我一直认为是90%左右)
分布
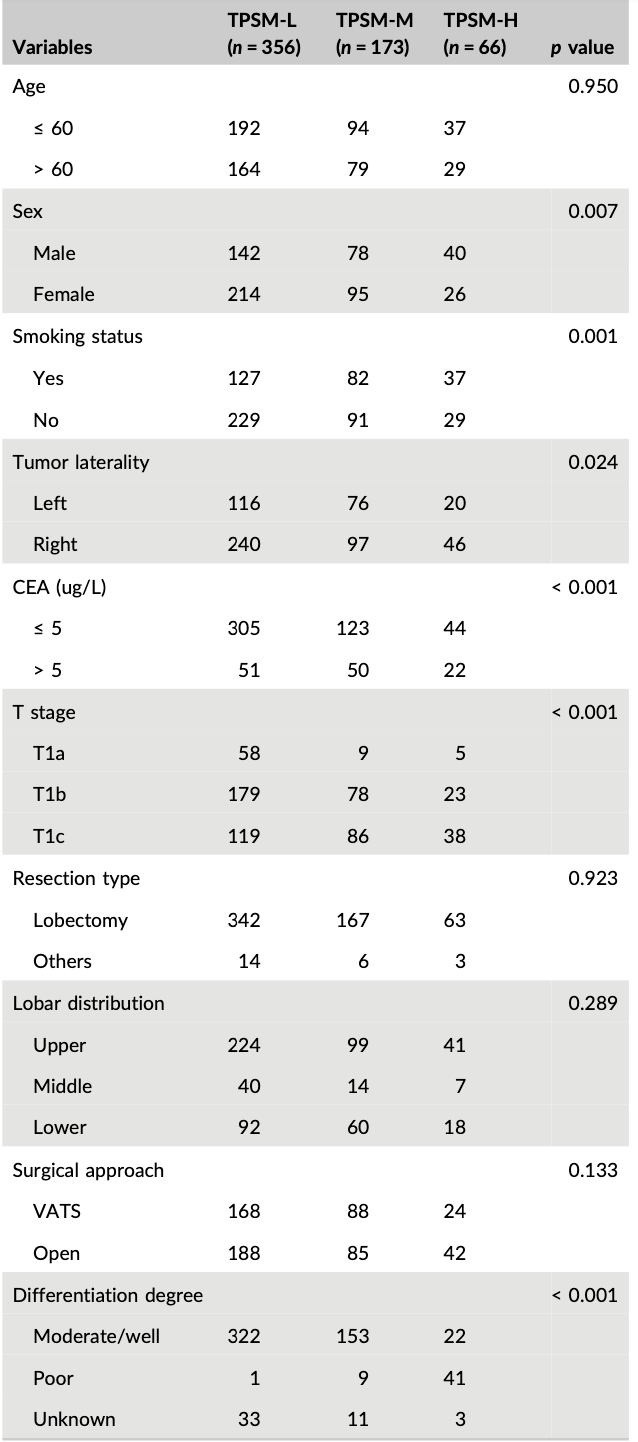
分布不均匀维度
肿瘤大小:TPSM-L: TPSM-M: TPSM-H 比分别为。可以看到,对于微乳头较高的两组,1A2和1A3的占比较高,那么本身的复发概率就会更高。
1A1: 16.3% : 5.2% : 7.6%
1A2: 50.2% : 45.1% : 34.8%
1A3: 33.4% : 49.7% : 57.6%
CEA:TPSM-L: TPSM-M: TPSM-H 比分别为。可以看到对于微乳头较高的两组,CEA>5的占比更高。
CEA <= 5: 85.7%: 71.1%: 66.7%
CEA > 5: 14.3%: 28.9%: 33.3%
DFS&OS
这里的DFS是指手术后到随访复发或者失联的时间(但是从KM曲线图中看出其实还是复发的时间)
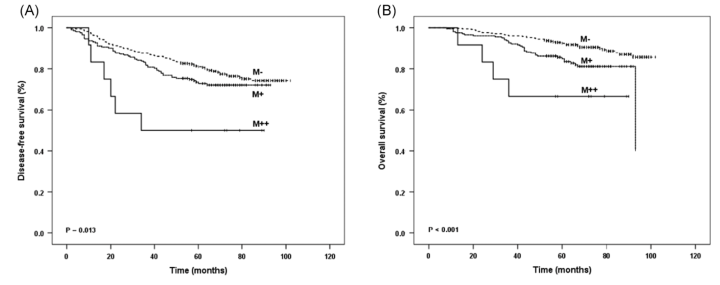
所有患者根据微乳头的占比DFS和OS
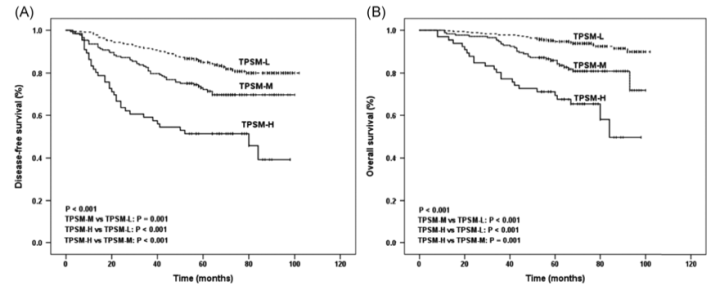
所有患者根据肿瘤风险程度的DFS和OS
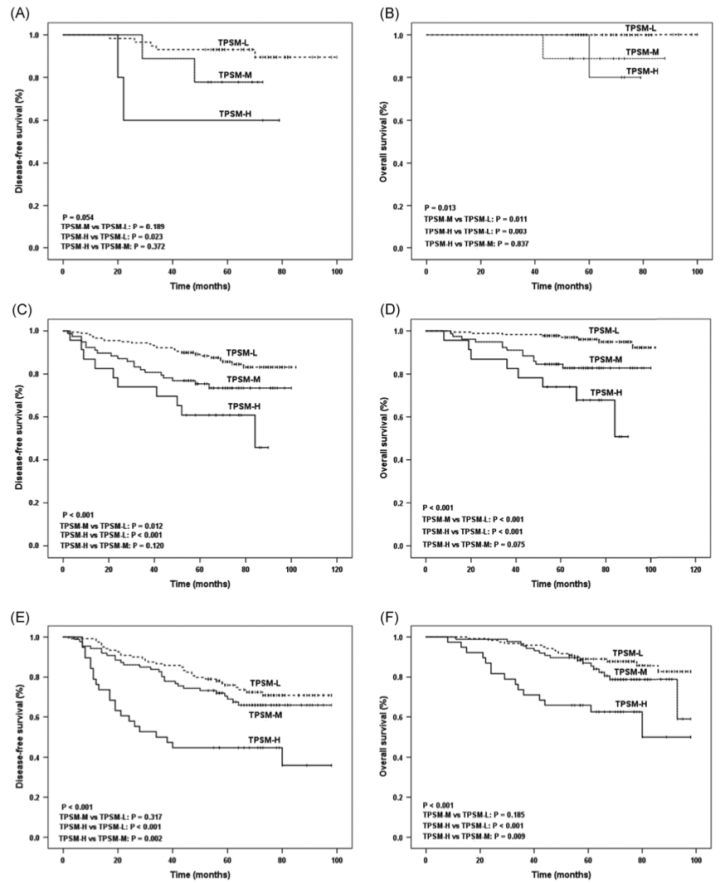
AB-T1a,CD-T1b, EF-t1c 中不同肿瘤为主体的DFS和OS
单变量&多变量因素
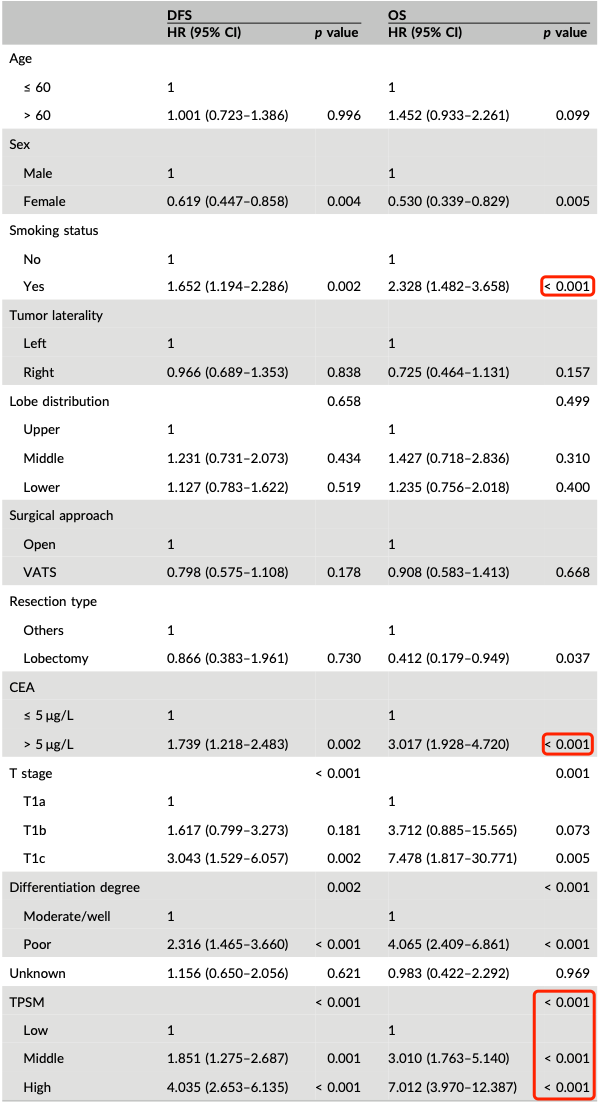
单变量HR(风险率)·
· DFS:微乳头>40% 4.035,T1c 3.043,10%<微乳头<40% 1.851,T1b 1.671(p=0.181),抽烟 1.652
· OS:T1c 7.478,微乳头>40% 7.020,T1b 3.712,CEA>5 3.017,10%<微乳头<40% 3.010,吸烟2.328
多变量HR
· DFS:微乳头>40% 4.142,T1c 2.369(p=0.017),10%<微乳头<40% 1.565(p=0.02),T1b 1.465(p=0.299)
· OS:T1c 4.847(p=0.032),微乳头>40% 4.389,T1b 3.712(p=0.153),10%<微乳头<40% 2.251
分析
这篇文章的数据有些倾斜,微乳头阴性组中1A1期的样本较多,可能也是影响DFS和OS的因素。
可以看出在1A1期,1A3中微乳头<10%和部分<40%的对比中,并没有多大的DFS差异(10%左右,整体还是在1A的大范围里)
第五篇:Procedure-specific prognostic impact of micropapillary subtype may guide resection strategy in small-sized lung adenocarcinomas: a multicenter study
微乳头亚型的程序特异性预后影响可指导小尺寸肺腺癌的切除策略:一项多中心研究
Therapeutic Advances in Medical Oncology, impact factor 7.03
内容
这是国内机构一篇研纯实性结节中微乳头占比对预后的影响,以及不同切除方式对预后的影响。
分布
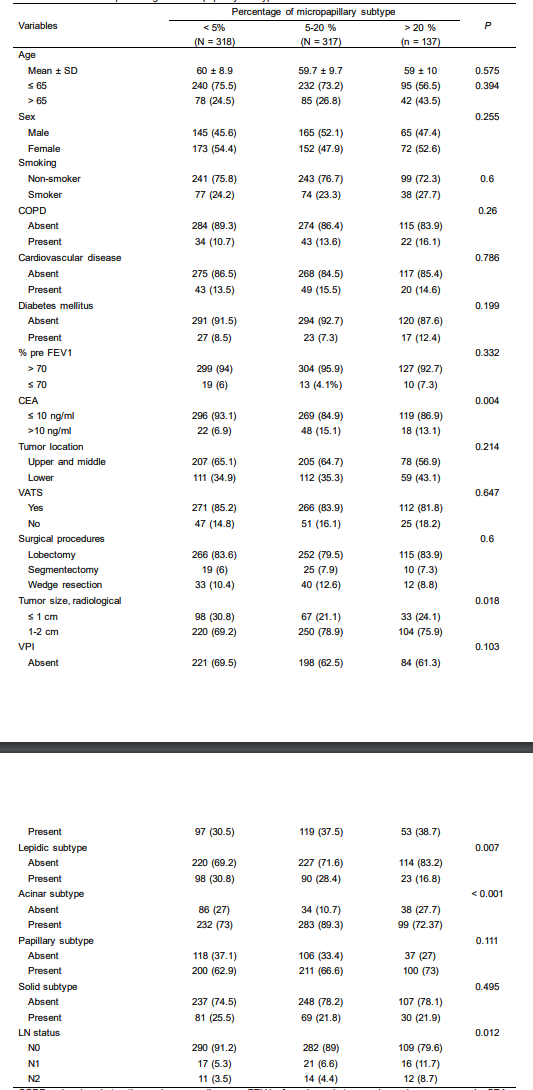
可以看到这里所有特征在不同组之间的分布非常的均匀,所以这篇文章的结果我觉得很有参考价值。
RFS&OS
RFS是指从手术到随访复发或者死亡的时间,正常死亡也会被算在里面
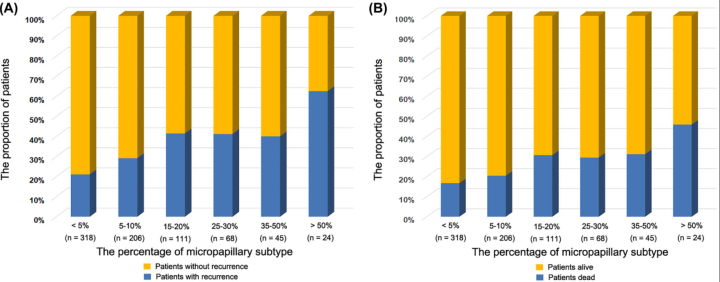
根据微乳头不同的RFS和OS
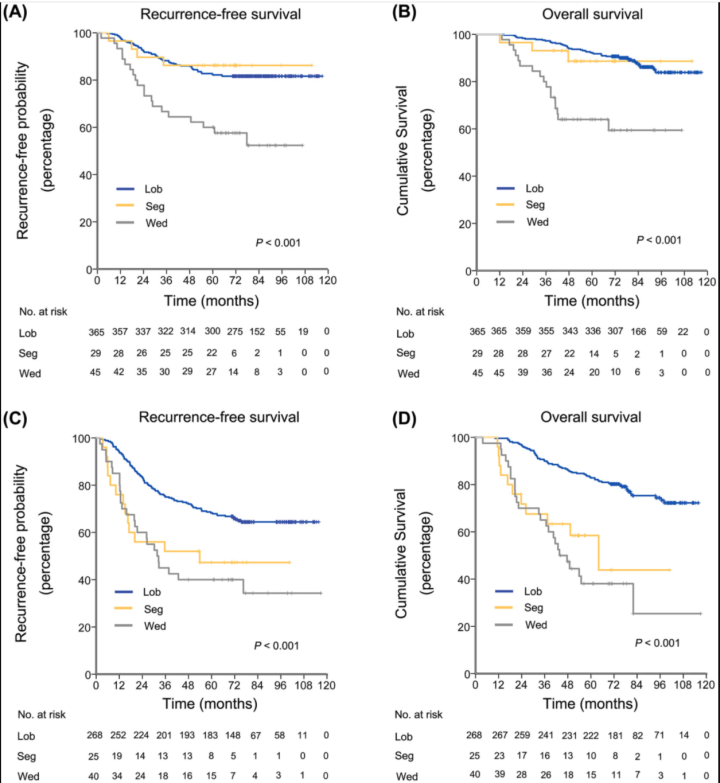 根据手术方式不同的RFS和OS
根据手术方式不同的RFS和OS
(a) RFS by surgical procedures in patients with lung ADCs ⩽2 cm with MIP ⩽5%; (b) OS by surgical procedures in patients with lung ADCs ⩽2 cm with MIP ⩽5%; (c) RFS by surgical procedures for patients with ADCs ⩽2 cm with MIP &amp;amp;amp;gt;5%; (d) OS by surgical procedures for patients with AD
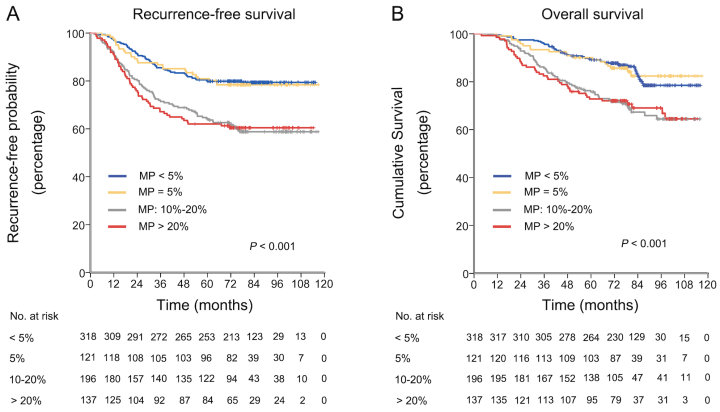
根据微乳头占比的RFS和OS
5年RFS
微乳头< 5% 82%
微乳头=5% 82%
微乳头10%~20% 60%
微乳头>20% 60%
5年OS
微乳头< 5% 86%
微乳头=5% 86%
微乳头10%~20% 75%
微乳头>20% 75%
可以看到,对于微乳头<5%和=5%的两组来说,没什么特别的差异,含有5%微乳头的朋友是不是安心许多呢?对于>=20%微乳头来说,复发死亡率就相对比较高了。
另外肺叶切除比肺段和楔形切除效果更好。
单变量&多变量因素
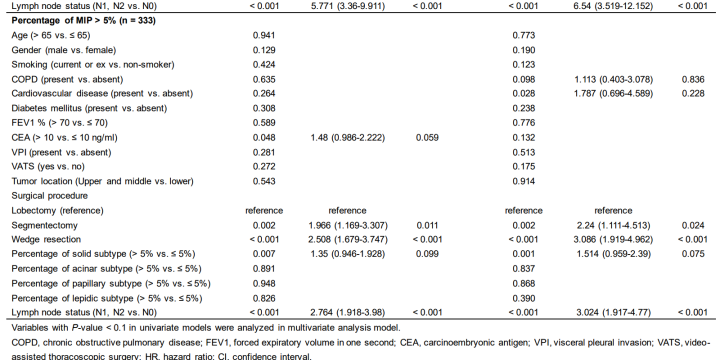
叶切和淋巴结侵犯是微乳头<5%和>5%之间的单变量和多变量因素。
分析
这一篇文章我认为写的非常好,并且是我看过文章中少有的几个,在不同微乳头比例的样本中,各个维度的特征分布都非常均匀的回顾实验,所以他的参考度非常高。
这里可以看到,对于实性结节,5%左右的微乳头,如果是肺叶切除,和<5%微乳头的效果非常接近。但是微乳头>5%的时候,复发率就非常高,美中不足没有看到10%微乳头的情况,我猜应该是介于5%到20%之间。
第六篇:Impact of the micropapillary component on the timing of recurrence in patients with resected lung adenocarcinoma
鉴别早期肺腺癌中非主要微乳头或实性成分是否有意义?
European journal of cardio-thoracic surgery, impact factor 4.191
内容
这篇文章主要研究了不同分化肿瘤的对复发的风险程度。风险越高的分化,越容易复发。并且指出了是大概在24个月里,高风险肿瘤迎来复发的两个峰值。
分布
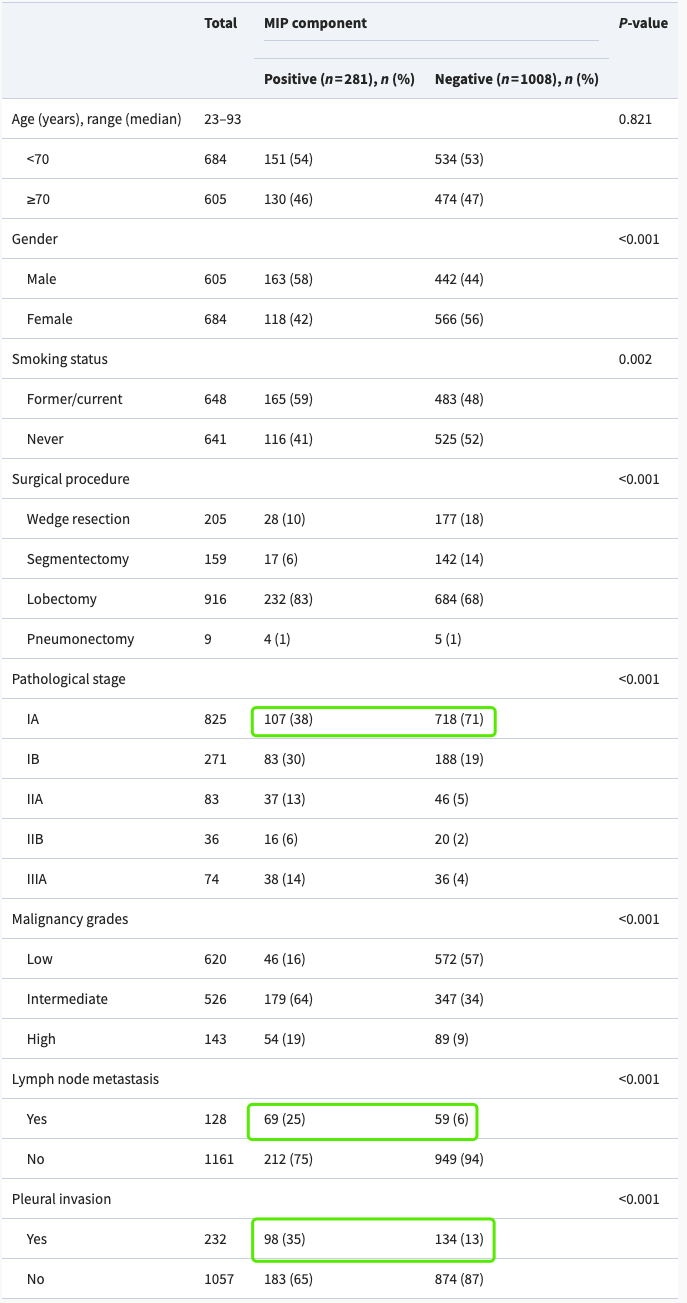
RFS&OS
RFS定义为手术后到随访中疾病复发或死亡的时间
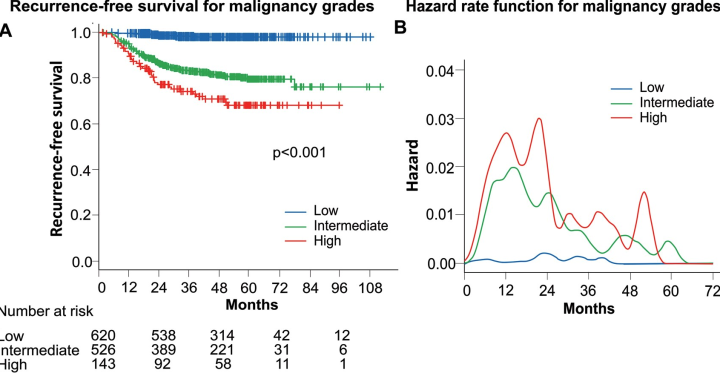
微乳头阴性和阳性的RFS
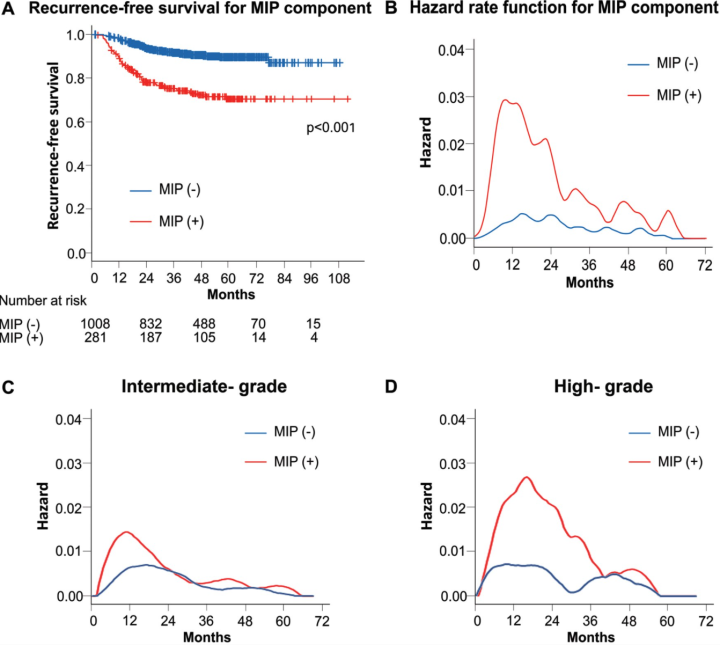
微乳头阴性和阳性,分布进行叶切,有限切除的RFS
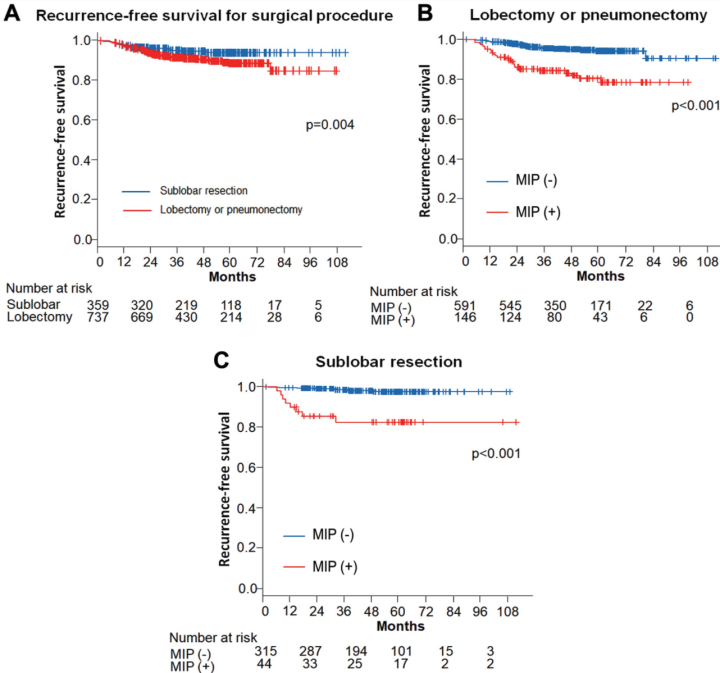
这里根据I期微乳头的存在,研究叶切和局限的效果时,我们发现阳性这组这里引入了很多IB期的患者(占比约50%),而阴性这组明显少于50%,所以也是不公平的比较。
单变量&多变量
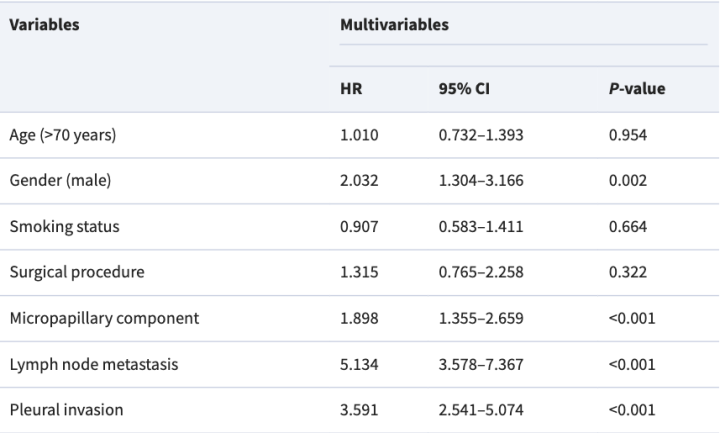
多变量
淋巴侵犯 5.134,胸膜侵犯 3.591,微乳头阳性 1.898。(所以可以看出,胸膜侵犯和淋巴结侵犯才的风险远比微乳头高)
分析
尚不清楚这篇文章的样本采样机制,但是由于在微乳头阴性和阳性中病理分期差异较大,所以无法说明复发的原因是微乳头造成。
但是这篇文章画出了手术后2年左右,高风险分化的肿瘤在2年内会有个复发高峰,还是非常值得注意的。尤其是提示对于1期的肺癌,术后一定要随访,趁早发现复发转移。
第七篇:Impact of Micropapillary Histologic Subtype in Selecting Limited Resection vs Lobectomy for Lung Adenocarcinoma of 2cm or Smaller
微乳头组织学亚型对 2cm 或更小的肺腺癌选择有限切除与肺叶切除的影响
JNCI-Journal of the National Cancer Institute. impact factor 13.56
内容
这篇文想要探讨的问题是,肿瘤在2cm以内,对于一些含有但不占优势的低分化肿瘤如微乳头和实体,不同的手术方式带来的不同预后。
分布
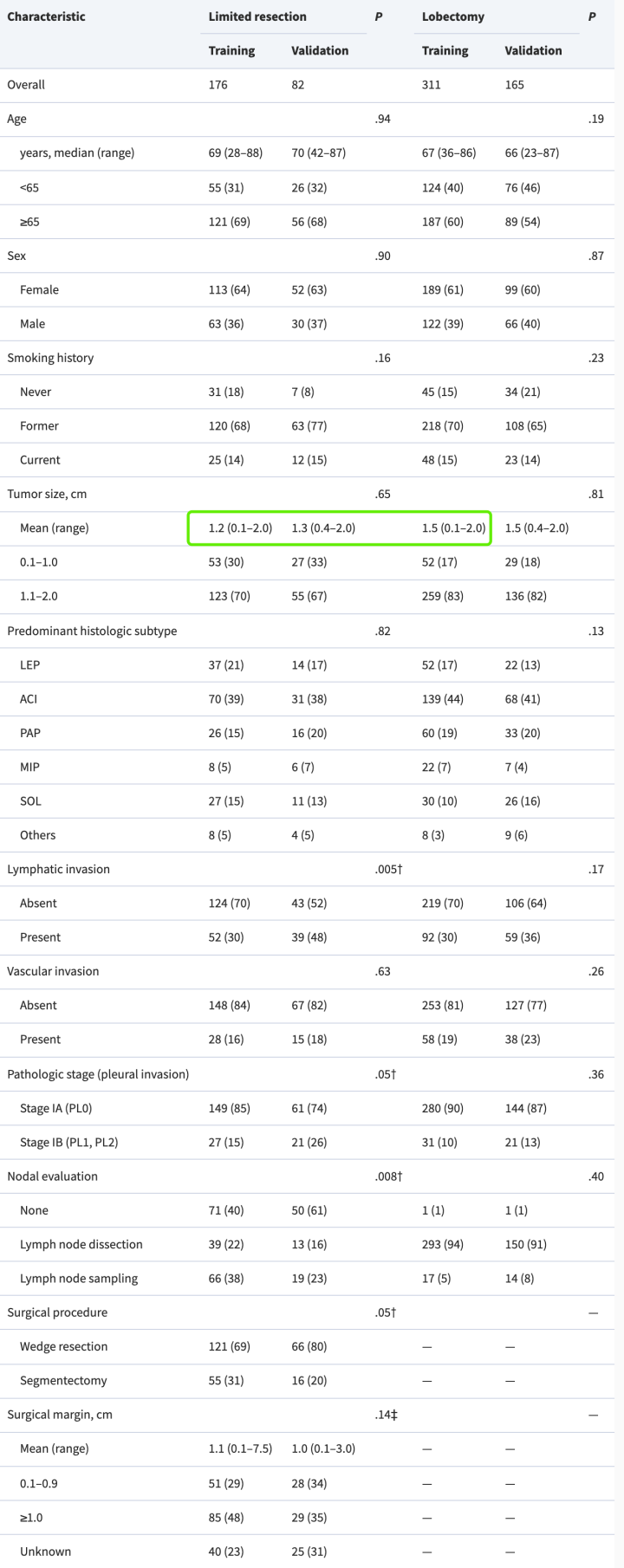
分布不均的维度(有限切除 : 肺叶切除)
结节大小:
1.2 :1.5
我们可以看到,这篇文章的样本在大部分维度的特征上分布的非常均衡,所以这篇文章的结果我认为具有指导意义。
CIR
CIR定为从手术后到发生复发的时间(和生存率相反)
AB是有限切除,CD是叶切
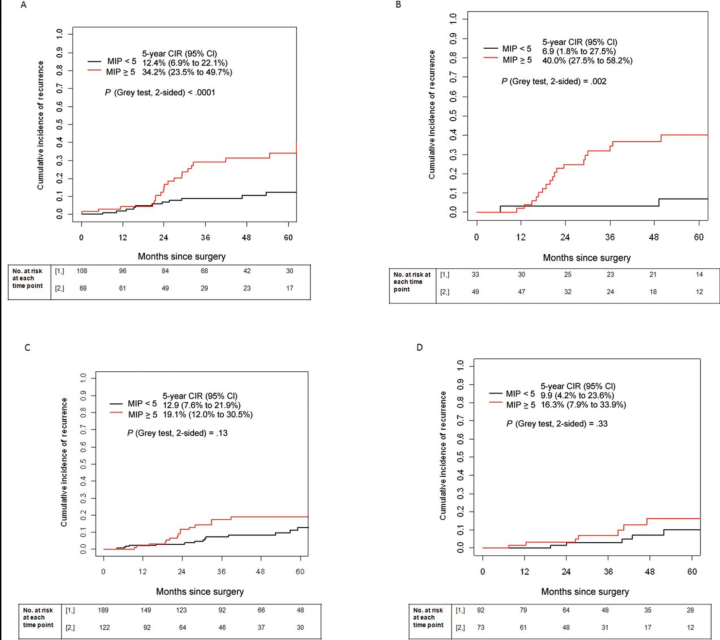
根据微乳头的含量,叶切和有限切除带来的5年CIR(可以看到如果是叶切,10%的微乳头好像也就提高了4%左右复发的概率)
单变量&多变量
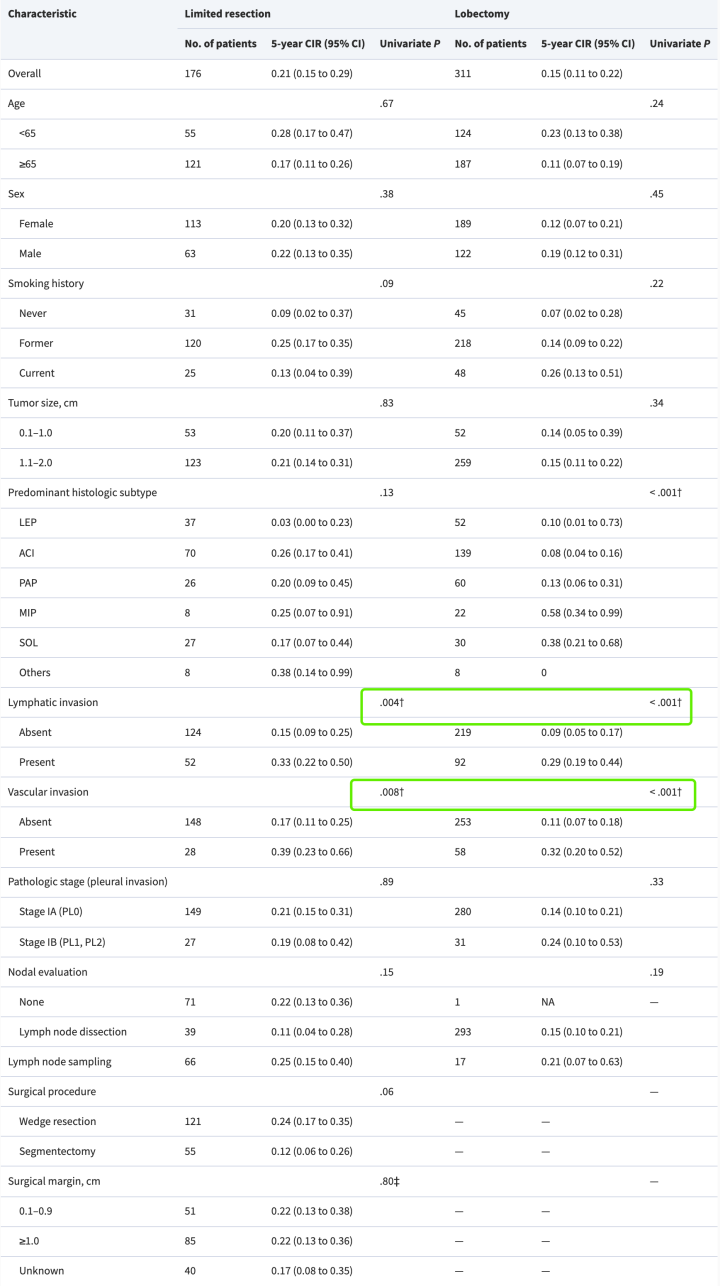
单变量
· 淋巴侵犯,血管侵犯
多变量
· 淋巴侵犯,血管侵犯,低分化亚型
分析
这篇文章的影响因子很高,研究了不同手术方式对于不同微乳头占比带来的预后影响。可以看到文章中数据的分布非常均衡,所以文章具有比较大的参考意义。那么对于少量微乳头的1A期,5~10%,会比微乳头阴性的复发概率高,但是如果是叶切,可以将复发概率减少。
复发转移猜想
那么到底是什么造成了微乳头的高危呢?有这么几个猜想(这次没时间去读文章了,下次更新)
微乳头的生物学性质造成转移风险高
比如容易产生癌细胞脱落,增值速度更快,可以释放对应免疫抑制蛋白等。(生物学性质) 微乳头病灶的基因产生突变,这种突变造成复发高。(比如微乳头是否由较强的驱动基因造成)
微乳头容易产生淋巴血管侵犯,或者淋巴结转移才导致了转移
微乳头容易造成血管侵犯,淋巴结转移才是导致复发转移的原因。(微转移,可统计微乳头组侵犯概率)
病情发展导致产生了微乳头
如果结节长大,侵犯了周围的组织,同时分化开始降低,此时发现的时候有微乳头并且淋巴侵犯。(判断微乳头组是否有更大的肿瘤尺寸,分期,侵犯等)
辅助治疗
目前对于1A期术后都不推荐做辅助治疗,因为没有证据显示有受益。对于1B期术后是推荐辅助治疗的,下面两篇文章可以作为辅助治疗获益的证据。(下次更新)
新的分期方式
微乳头是否需要对1期患者进行临床升级?
WCLC2021上有一些讨论,比如,有学者提出将微乳头阳性考虑到分期模型中,因为他们发现对于T1a-b-c期的患者,预后和T2a差不多,进行病理的临床升级(很熟悉,因为那么会医生也说我妈有10%微乳头,所以临床升级了)。注意这里并提示说微乳头的占比,后面我找了这位教授的资料但是没有相关文章。没有但是在session后的讨论中,有学者就认为在多变量分析中看到的微乳头的影响幅度可能不足以使其具有临床意义或考虑需要升级。(In his discussion of the results, Dr. Alatorre-Alexander noted that the magnitude of the effect seen in the multivariable analysis may not(be large enough to make it clinically meaningful or to consider that upstaging will be needed.)
根据高危亚型的占比,提出一种新的分期方式
1级:高分化腺癌:以贴壁为主的肿瘤,高危亚型(实性、微乳头状和/或复杂腺模式)没有或少于 20%。
2级:中度分化腺癌:腺泡或乳头状为主的肿瘤,高危亚型没有或少于 20% 的高级模式。
3级:低分化:任何具有 20% 或更多高危亚型的肿瘤。
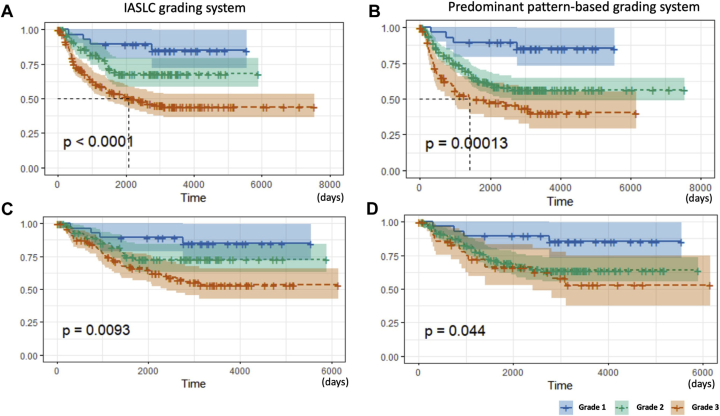
左边是作者提出的新的分期方案,右边是现有的分期方案。AB是所有的病例的生存结果,CD是对1期病例的生存结果。可以看到,新的分期在所有的病例中有很好的区分度。并且大家可以发现,如果你的高危亚型在20%以下,预后也没有特别特别的差。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8362286/
小结
我们可以看到,微乳头作为1期预后的高危因素是一个共识,因为存在微乳头往往伴随着更大更实性的肿瘤,更高的分期,更高的淋巴结转移概率,更高的气道散播,淋巴侵犯,血管侵犯的概率。
对于1B期以上的患者,微乳头带来的影响应该远没有淋巴结转移,直接侵犯带来的影响大。并且治疗方案也是确定的,可以通过靶向,化疗,放疗,免疫等方面。所以1B期以上的患者其实无需纠结微乳头的含量。
对于1A期的患者,如果存在大量微乳头>20%。那么请在医生的建议和个人的意愿下进行辅助治疗,如化疗或者靶向。
对于1A期的患者,如果存在少量微乳头<20%。微乳头的存在确实是一个高危的因素,但也不是说就一定会复发,尤其是当你是一个较小的肿瘤(比如<2cm),磨玻璃成分居多实性成分较少(CTR<0.5),纵膈窗不显影或者很少的实性成分,没有气道散播,没有可见脉管癌栓,并且采取了叶切而不是有限切除,那么我认为复发的概率也不是特别的大,还是符合1A期的均值。这时候无需后续的治疗,但是需要密切和科学的随访。(有些医生会建议进行辅助治疗,如有基因突变的患者,复用副作用较小的靶向2-3年,这个是超前于指南的,这个只能见仁见智,没有任何实验有证据,但真实世界中也有复用了以后长期不复发的例子(主要这个实验真不好做啊,那么长的周期)。但是我觉得靶向或免疫在早期肺癌中会作为巩固的治疗,已经有这样的趋势,比如Adura对于1B期及以后,且具有淋巴结转移的患者复用奥希替尼有较好的防止复发的效果。)
收藏
回复(55)参与评论
评论列表
 怕黑的毛衣372049549
怕黑的毛衣372049549 要有好心态
要有好心态 黄河石-3959
黄河石-3959 11111111113143
11111111113143 只想妈妈好好活着
只想妈妈好好活着 幸福的太阳4215
幸福的太阳4215 自由的野马5597
自由的野马5597 会撒娇的牛肉面2633
会撒娇的牛肉面2633