ES-SCLC一线治疗的“优等生”——梁斐教授从统计学角度解读ASTRUM-005研究
编者按:广泛期小细胞肺癌(ES-SCLC)长期以来是肺癌领域的治疗“洼地”,患者预后较差,中位生存期不足1年。近年来,免疫治疗在ES-SCLC领域取得诸多突破,尤其是近期在ASCO大会上大放异彩的斯鲁利单抗ASTRUM-005研究。本文中,复旦大学附属中山医院梁斐教授将从统计学角度解读ASTRUM-005研究,并通过ESMO临床获益评价量表,在当前诸多ES-SCLC一线治疗中寻找到优选方案。
01
ASTRUM-005研究的统计学设计
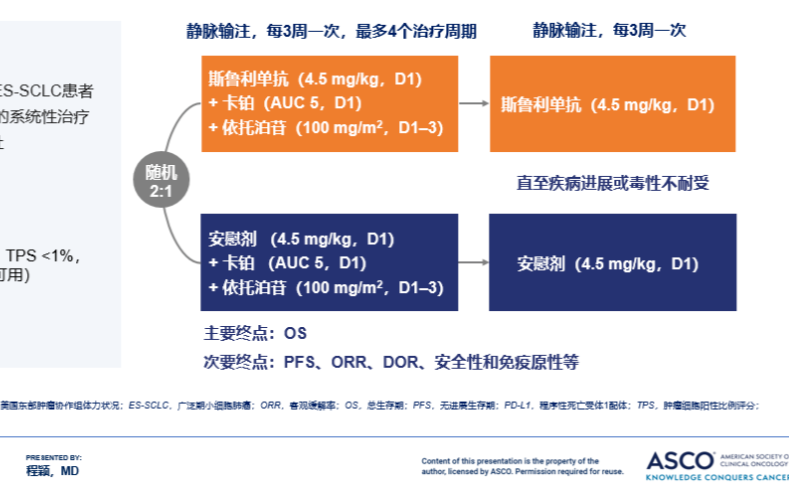
ASTRUM-005研究是一项随机、双盲、国际多中心、安慰剂对照的III期临床试验,旨在评价斯鲁利单抗或安慰剂联合化疗(卡铂+依托泊苷)用于广泛期小细胞肺癌(ES-SCLC)一线治疗的疗效和安全性。研究的主要终点是OS,次要终点包括PFS、ORR、DOR和安全性等。

目前,OS仍是公认的、能够直接评价患者获益的临床终点指标,而且是一个不依赖于研究者主观评估的客观指标,测量方法简单,数据精确。不同于EGFR突变和ALK重排的非小细胞肺癌,广泛期小细胞肺癌目前非常缺乏有效的后线治疗方案,患者整体的生存期较短。因此,广泛期小细胞肺癌以OS作为主要研究终点,既可以在短时间内得到确证性的结果,也不会受到后线治疗的明显干扰。
ASTRUM-005研究计划招募567例患者。假设安慰剂组的中位OS为10个月,假设脱落率为20%。在双侧α=0.05、HR=0.7下,要获得85%的把握度需观察到至少342例死亡事件。因此,预计的最终分析需要在累计观察到342例死亡事件后进行。
此外,ASTRUM-005研究预设了一次期中分析。期中分析(interim analysis)又称期间分析,是指在正式完成临床试验前,按事先制订的分析计划,比较处理组间的有效性和安全性所作的分析。期中分析的日程、安排、研究提前终止的标准等应当事先制订计划并在试验方案中阐明。合理设置期中分析的时间,提前终止临床试验,可使药物尽快上市,或者减少受试者有害暴露的时间。
根据目的可将期中分析分为:1)无效性期中分析(Futility Interim Analysis),基于期中分析的结果,宣布试验失败,提前终止研究;2)有效性期中分析(Efficacy Interim Analysis),基于期中分析的结果,宣布试验成功,提前终止研究。
对于有效性期中分析,宣布研究是否成功(达到统计学差异)的标准,不再是传统的双侧0.05或者单侧0.025,而是基于期中分析α消耗函数所确定的界值来决定。有效性期中分析的好处是在药物效果特别好的情况下,可以提前宣布研究成功,使得药物尽快上市,造福患者。风险是每进行一次分析都会消耗α,如果期中分析没有成功,则最终分析成功的难度会增加。
ASTRUM-005研究计划进行一次期中分析和最终分析(O'Brien-Fleming型α消耗函数):
当死亡事件数达到226人时,将进行期中分析(α=0.012;双侧);
当死亡事件数达到342人时,将进行最终分析(α=0.046;双侧)。
02
ASTRUM-005研究结果解读
在ASTRUM-005研究的期中分析中,对照组中位OS 为10.9个月,斯鲁利单抗组15.4个月,HR=0.63(95%CI: 0.49-0.82),P<0.001,P值远远小于预设界值0.012。
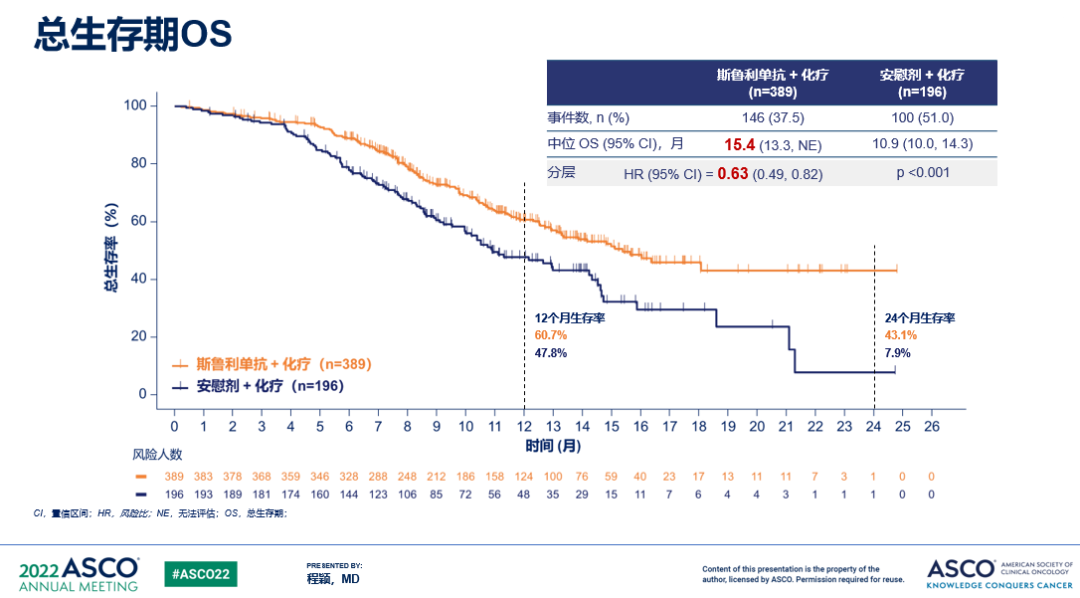
在PFS方面,对照组中位PFS为4.3个月,斯鲁利单抗组为5.7个月,HR=0.48(95%CI: 0.38-0.59),也观察到了明显的获益。
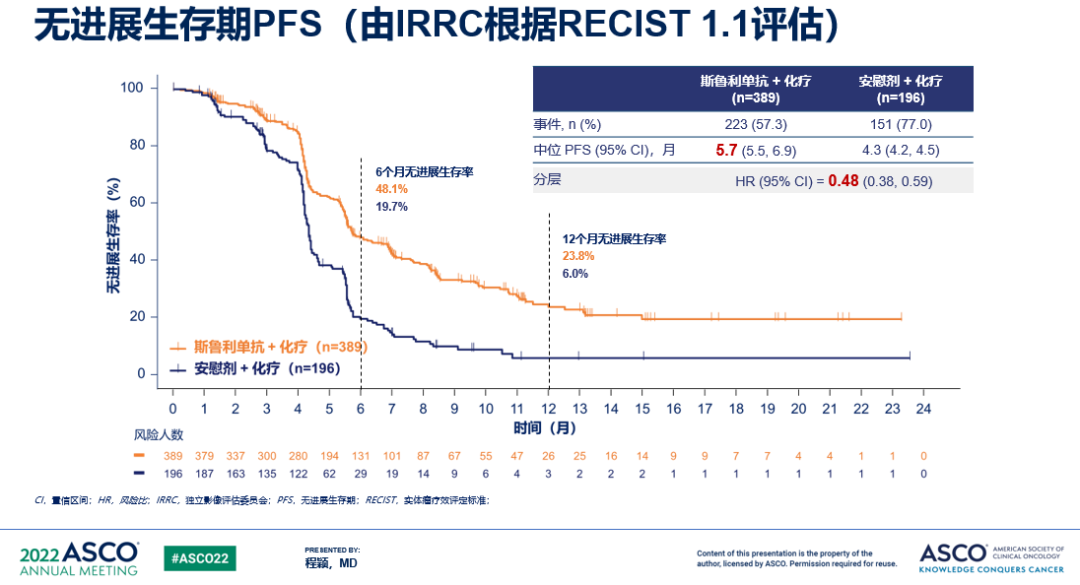
有临床专家会有疑问,为何中位PFS仅延长了1.4个月,而OS的延长幅度却达到了4.5个月。
首先是对PFS获益的评价,在免疫治疗时代由于存在生存曲线分离晚和长拖尾的效应,中位值对于评价PFS的获益不是非常客观,因此更应该关注HR以及6/12个月PFS率等指标。另外一个原因是免疫治疗存在假性进展的情况,部分患者在进展后继续接受免疫治疗仍然存在获益。
在之前的IMPower-133研究以及Caspian研究中,我们都看到了在中位PFS延长只有不到一个月甚至没有任何延长的情况下,中位OS有两个月左右的延长。在ASTRUM-005研究中,12个月PFS率是23.6% vs 6.0%,HR=0.48,从数值上看优于先前研究的PFS结果,这也支持ASTRUM-005研究的OS结果。
03
不同研究结果的比较
在没有头对头RCT的情况下,跨研究比较不同药物的效果是需要谨慎的。但是随着同一病种可选择药物的不断增加,临床医生也需要有客观的工具来衡量各个药物的临床获益大小。
为了量化抗肿瘤药物的临床价值,近几年ASCO和ESMO分别开发了临床获益量表,用来评价各个治疗方案临床价值的大小。临床获益量表综合了疗效、毒性、生活质量以及价格等各个方面临床获益量表选取的疗效评价指标,代表了ESMO和ASCO对于各个疗效评价指标的认可程度。
下图是ESMO的临床获益评价量表(ESMO-Magnitude of Clinical Benefit Scale version 1.1,MCBS1.1)。对于对照组中位生存期≤12个月的临床研究,在不考虑安全性和生活质量的情况下,药物的临床获益分为四个等级:Grade 1-4,4代表最高,1代表最低。达到Grade 4的要求需要满足以下两条中的任何一条:1)HR(置信区间下限,而不是点估计)≤0.65且中位OS延长≥3个月;2)2年OS率提高≥10%。

ESMO的临床获益评价量表目前已经广泛应用于ESMO的各大指南中,下图是ESMO的小细胞肺癌指南,其中度伐利尤单抗和阿替利珠单抗这两个PD-L1抑制剂都是I类推荐,证据级别是A级。后面还有“MCBS 3”的字样,表示基于ESMO MCBS1.1的量表。这两个方案的MCBS得分都是3分。
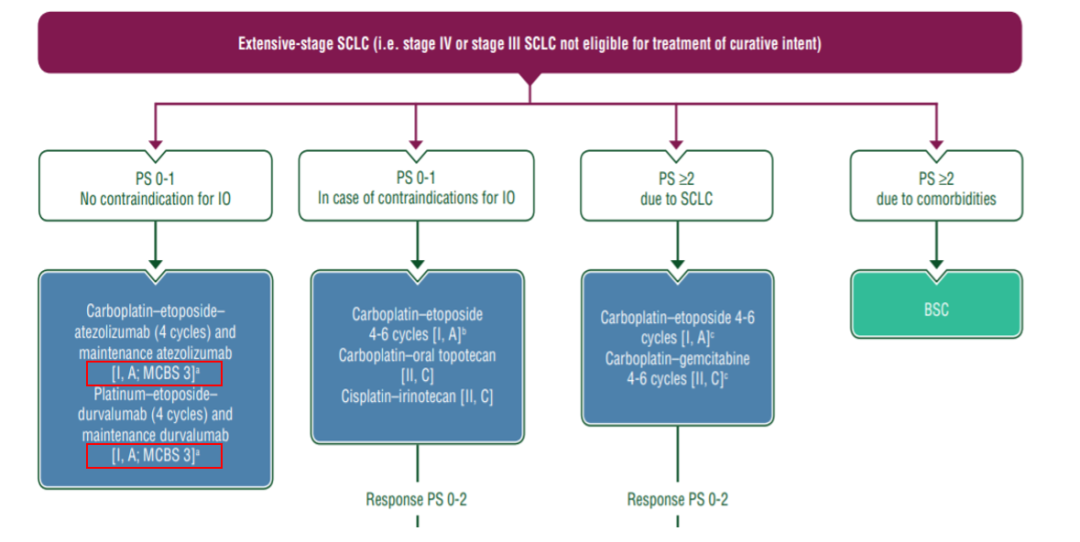
目前,在广泛期小细胞肺癌一线治疗领域,国内外已有数个免疫联合治疗研究取得突破。虽然这些研究的治疗方案、基线特征等存在差异,无法跨研究直接比较不同研究结果,但在ASTRUM-005研究中,斯鲁利单抗的HR下限为0.49(≤0.65)且中位OS延长了4.5个月(≥3个月),2年OS提高了35.2%(≥10%)。从ESMO MCBS1.1量表来看,无论是基于HR和中位OS的延长以及2年OS率的提高程度,斯鲁利单抗的MCBS得分都可以到4分,也是目前唯一一个可以达到MCBS 4分的方案(注:阿得贝利单抗的对照组OS超过了12个月,根据ESMO MCBS1.1量表12个月<OS≤24个月要求,需要HR≤0.7且OS延长≥5个月或3年OS率提高10%才能评为4分)。

04
总 结
从统计学角度来看,ASTRUM-005研究的期中分析结果取得令人鼓舞的结果,主要终点OS的P值远远小于预设的0.012的界值;斯鲁利单抗用于ES-SCLC一线治疗可较对照方案延长OS 4.5个月,死亡风险降低37%,2年OS率提高35.2%,OS的获益程度全部满足ESMO MCBS1.1评估量表的4分等级,可作为ES-SCLC一线治疗的优选方案。
本文来源:肿瘤瞭望
声明:本资料中涉及的信息仅供参考,请遵从医生或其他医疗卫生专业人士的意见或指导。
热门药品
相关资讯