北京时间 10 月 7 日下午 5 点 30 分,2019 年诺贝尔生理学或医学奖揭晓获奖名单,来自哈佛医学院达纳-法伯癌症研究所的威廉·凯林( William G. Kaelin, Jr.),牛津大学和弗朗西斯·克里克研究所的彼得·拉特克利夫( Peter J. Ratcliffe)以及美国约翰霍普金斯大学医学院的格雷格·塞门扎(Gregg L. Semenza)摘得殊荣,以表彰他们在细胞如何感知和适应氧气变化机制方面所作出的贡献。
▲William G Kaelin 教授(左)、Peter J Ratcliffe 教授(中)、以及 Gregg L Semenza 教授(右)
三位科学家在分子水平上阐明了感受氧气含量的基本原理,揭示了其中重要的信号机制,为贫血、心血管疾病、黄斑退行性病变以及肿瘤等多种疾病开辟了新的临床治疗途径。
生物体感受氧气浓度的信号识别系统是生命最基本的功能,然而学界对此却所知甚少。氧气是众多生化代谢途径的电子受体,科学界对氧感应和氧稳态调控的研究开始于促红细胞生成素(erythropoietin, EPO)。
20 世纪 90 年代初,Semenza 和 Ratcliffe 开始研究缺氧如何引起 EPO 的产生。他们发现了一个不仅会随着氧浓度的改变发生相应的改变,还可以控制 EPO 的表达水平的「开关」,如果将其 DNA 片段插入某基因旁,则该基因会被低氧条件诱导表达。他们发现这个反应的「开关」是一种蛋白质,叫做缺氧诱导因子 (Hypoxia-inducible factors, HIF),但其功能远不止开关那么简单。
1995 年,Semenza 和博士后王光纯化了 HIF,明确 HIF 编码基因,发现 HIF 由两种不同的 DNA 结合蛋白组成(HIF-1α 和 ARNT),并证实了 HIF-1 是通过红细胞和血管新生介导了机体在低氧条件下的适应性反应。
随后, Semenza 和 Ratcliffe 又扩展了低氧诱导表达基因的种类。他们发现,除了 EPO, HIF-1 在哺乳动物细胞内可以结合并激活涉及代谢调节、血管新生、胚胎发育、免疫和肿瘤等过程的众多其他基因。
作为一种关键的调控蛋白,在缺氧环境下,HIF-1 会启动基因表达。当细胞转变为高氧条件时 HIF-1 的数量急剧下降。那么推动 HIF-1 破坏的原因是什么?答案来自一个意想不到的方向。
希佩尔-林道综合征 (Von Hippel–Lindau disease,VHL 综合征)是一种罕见的常染色体显性遗传性疾病。VHL 病人由于 VHL 蛋白的缺失会以多发性肿瘤为特征, 涉及脑、骨髓、视网膜、肾脏、肾上腺等多个重要器官,
肿瘤学家 William Kaelin 一直试图弄清楚其病理,他发现典型的肿瘤有异常形成的新生血管,同时也有较多的 血管内皮生长因子 (VEGF) 与促红细胞生成素(EPO)。因此他自然而然地想到,缺氧通路是否在这种疾病里有着某种作用。
1996 年,对于患者细胞的分析表明,一些原本应当在富氧环境下消失的基因,却意外地有着大量表达。而导入具有正常功能的 VHL 蛋白,则能逆转这一现象。进一步的研究表明,VHL 蛋白的特殊能力,来源于与之结合的一些特定蛋白,这包括了某种泛素连接酶。在这种酶的作用下,不被细胞所需要的蛋白会被打上「丢弃」的标记,并被送往蛋白酶体中降解。
有趣的是,人们马上发现在富氧环境下,HIF-1 的组成部分 HIF-1α,正是通过这一途径被降解。1999 年,Ratcliffe 教授团队又发现,HIF-1α的降解需要 VHL 蛋白参与。Kaelin 教授也随之证明,VHL 与 HIF-1α会直接结合。再后来,诸多研究人员逐渐还原了整个过程——原来在富氧的环境下,VHL 会结合 HIF-1α,并指导后者的泛素化降解。
为什么 HIF-1α只会在富氧环境下被降解呢?研究人员对 HIF-1α与 VHL 的结合区域做了进一步的分析,并发现倘若移除一个脯氨酸,就会抑制其泛素化。这正是 HIF-1α的调控关键!在富氧环境下,氧原子会和脯氨酸的一个氢原子结合,形成羟基,而这一步反应需要脯氨酰羟化酶的参与。由于这步反应需要氧原子的参与,因而比较容易理解,为何 HIF-1α不会在缺氧环境下被降解。
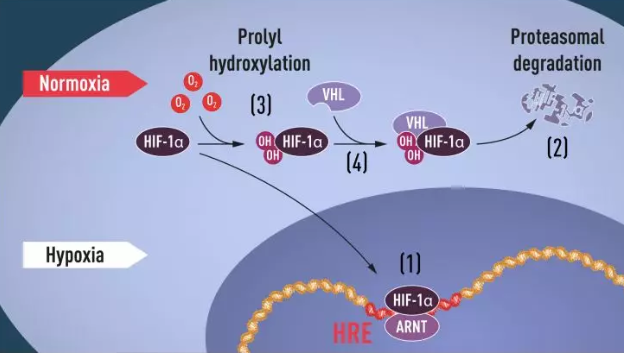
当氧水平低(低氧)时,HIF-1α 被保护免于降解,积聚在细胞核中,与 ARNT 及低氧调节基因中的特定 DNA 序列(HRE)结合(1);在正常的氧气水平下,HIF-1α 被蛋白酶体迅速降解(2);氧气通过向 HIF-1α 添加羟基(OH)来调节降解过程(3);随后,VHL 蛋白可以识别 HIF-1α 并与之形成复合物,从而导致其以氧依赖性方式降解(4)。
HIF 控制着人体和大多数动物细胞对氧气变化的复杂又精确的反应,三位科学家一步步揭示生物氧气感知通路。不仅在基础科学上有其价值,还有望带来创新的疗法。比如倘若能通过调控 HIF-1 通路,促进红细胞的生成,就有望治疗贫血;而干扰 HIF-1 的降解,则能促进血管生成,治疗循环不良。
另一方面,由于肿瘤的生成离不开新生血管,如果我们能降解 HIF-1α或相关蛋白 ,就有望对抗恶性肿瘤。目前,已有类似的疗法进入了早期临床试验阶段。
我们再次祝贺这三名科学家获得诺贝尔生理学或医学奖,是对他们所做成就的最佳认可!
William G. Kaelin Jr.
1957 年出生于纽约,取得了杜克大学的博士学位,William Kaelin Jr 在约翰霍普金斯大学和达纳-法伯癌症研究所接受了内科和肿瘤学的专科培训,同时在达纳-法伯癌症研究所建立了自己的实验室,并与 2002 年正式成为哈佛医学院的正教授,从 1998 年开始,其就成为了霍华德休斯顿医学院的研究员。
Sir Peter J. Ratcliffe
1954 年出生于英国兰开夏郡,其在剑桥大学学习医学,并在牛津大学接受了肾病学的专业培训,同时在牛津大学建立了自己独立的研究小组,并于 1996 年成为正教授,目前 Sir Peter J. Ratcliffe 是 Francis Crick 研究所的临床研究主任,牛津 Target 发现研究所的主任以及路德维希癌症研究所的研究成员。
1956 年出生于纽约,其获得了哈佛大学的学士学位,并于 1984 年获得了宾夕法尼亚大学费城医学院的医学博士学位,同时在杜克大学接受了儿科专家的培训,并在约翰霍普金斯大学进行了博士后研究,建立了自己的研究团队,1999 年 Gregg L. Semenza 成为了约翰霍普金斯大学的正教授,从 2003 年开始担任约翰霍普金细胞工程研究所血管研究计划小组的主任。